查看更多

 明星产品
明星产品
 关注我们
关注我们

扫码关注我们
了解更多信息
骨肉瘤(OS)是最常见的骨科恶性肿瘤,OS患者的常见治疗选择为手术切除、放疗和化疗。然而,化疗后耐药和术后远处转移仍然是导致预后不良、治疗失败的关键因素。目前仍需通过阐明OS的发展机制,寻找一种新的早期诊断特征来探索OS的治疗策略。外泌体是微小的细胞间囊泡,其通过携带各类调控分子既促进肿瘤发展转移,也在抑制肿瘤进展方面也发挥了重要作用。近日,广西医科大学第一附属医院薄占东团队在Molecular Cancer(IF=37.3)上发表文章“Exosome-mediated miR-144-3p promotes ferroptosis to inhibit osteosarcoma proliferation, migration, and invasion through regulating ZEB1”,对外泌体中的miRNA-144-3p与OS病例特征的相关性和调控铁死亡的机制进行了具体阐述。在该研究中,作者使用了汉恒生物提供的慢病毒和腺病毒进行miR-144-3p和ZEB1的敲低和过表达,并使用汉恒生物提供的双荧光素酶检测试剂盒进行miR-144-3p与ZAB1结合验证。
首先,作者通过分析GEO中与OS相关的数据集,发现miR-144-3p在OS患者中表达下调,miR-144-3p低表达患者具有更短的生存时间,通过qPCR检测发现OS细胞株和成骨细胞及OS患者癌旁组织中miR-144-3p普遍下调,表明miR-144-3p是OS有价值的预后生物标志物。作者应用miRDB数据库根据靶标评分排名预测下游基因ZEB1 mRNA可能为靶mRNA,进一步的双荧光素酶检测结果表明二者间存在结合作用。OS细胞株、成骨细胞和OS患者癌旁组织的qPCR和IHC结果表明ZEB1表达显著上升,其高表达与OS患者预后较差相关。
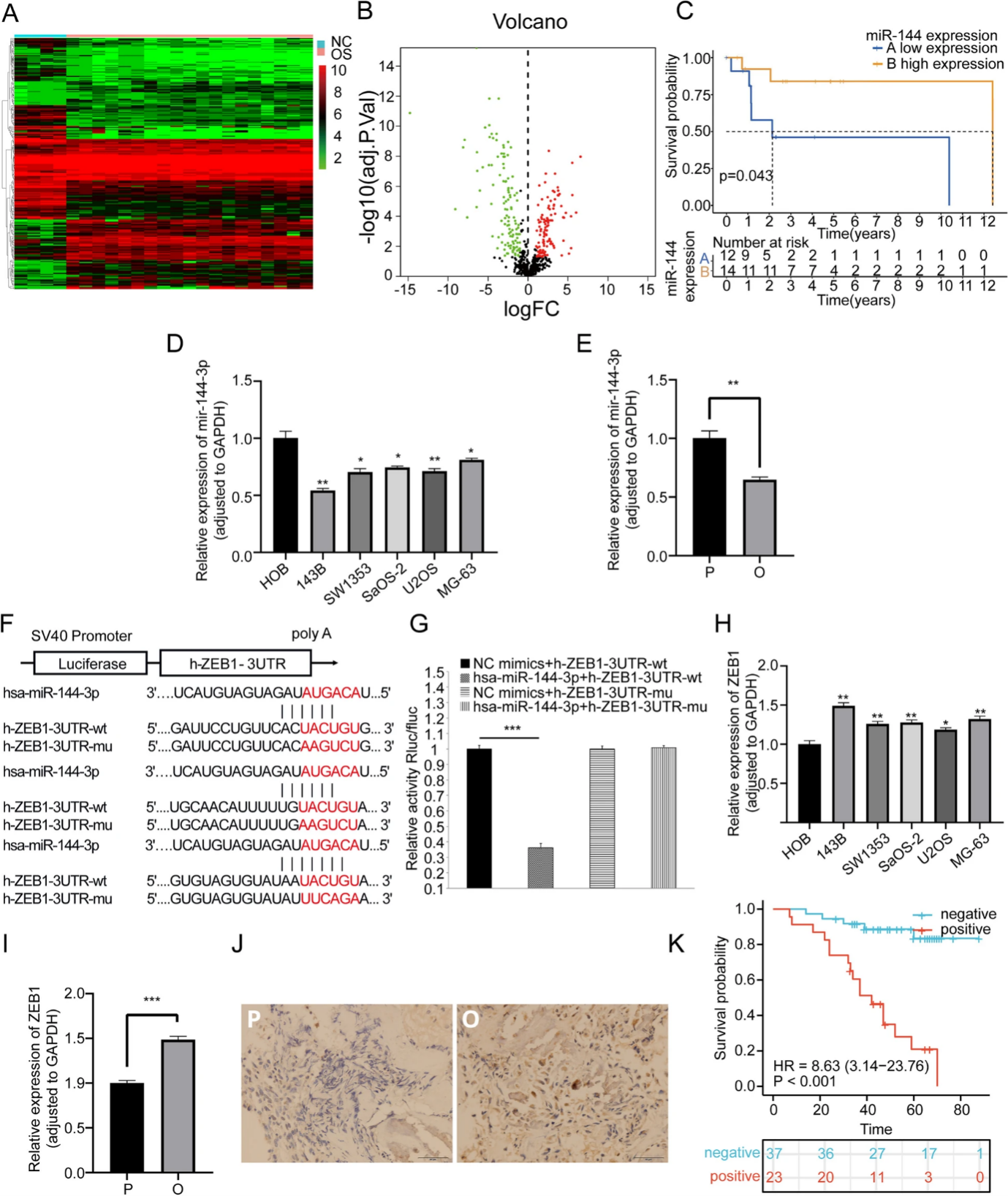
图1. miR-144-3p为OS关键 miRNA
随后,作者从h143B细胞中分离了外泌体并检测,发现外泌体特征蛋白在外泌体裂解液中高表达,将红光标记的外泌体与OS细胞共培养,可以在胞内观察到明显的红色荧光染色,这证实了外泌体可以作为载体将生物分子运输到细胞中。作者进行了OS组织外泌体微阵列,结果显示人OS组织外泌体中miR-144-3p的表达同样呈现显著降低。为验证miR-144-3p对ZEB1的调控作用,作者在h143B细胞中敲低或过表达miR-144-3p或ZEB1,发现ZEB1的表达与miR-144-3p呈负相关。
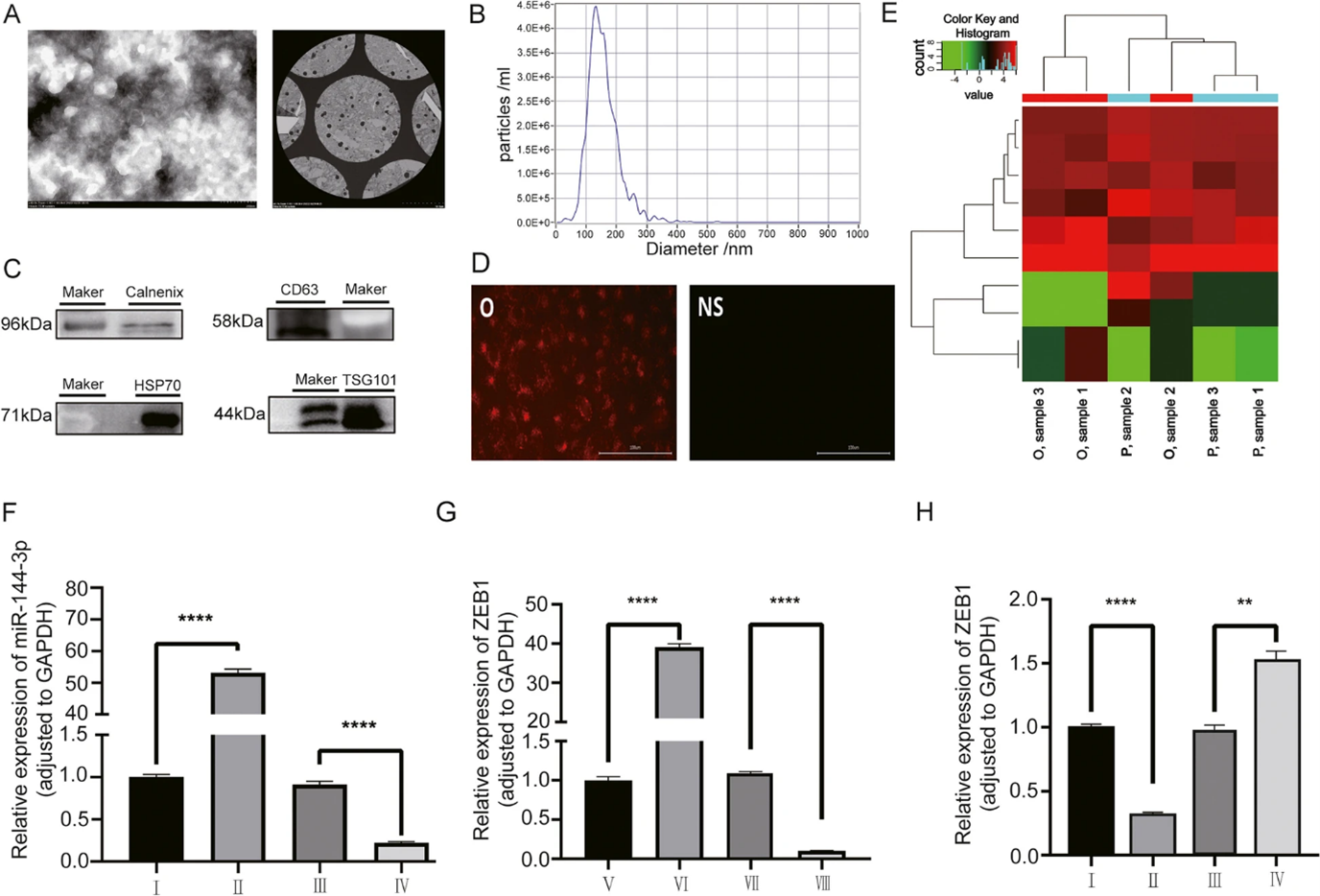
图2. h143B细胞miR-144-3p/ZEB1轴
接下来,作者验证了MiR-144-3p对OS细胞表型的影响,CCK8和跨孔测定结果显示miR-144-3p的过表达显著降低OS细胞活力、侵袭和迁移能力。裸鼠成瘤实验中,miR-144-3p过表达组的OS体积在核磁共振影响和直接测量结果中均小于NC组。
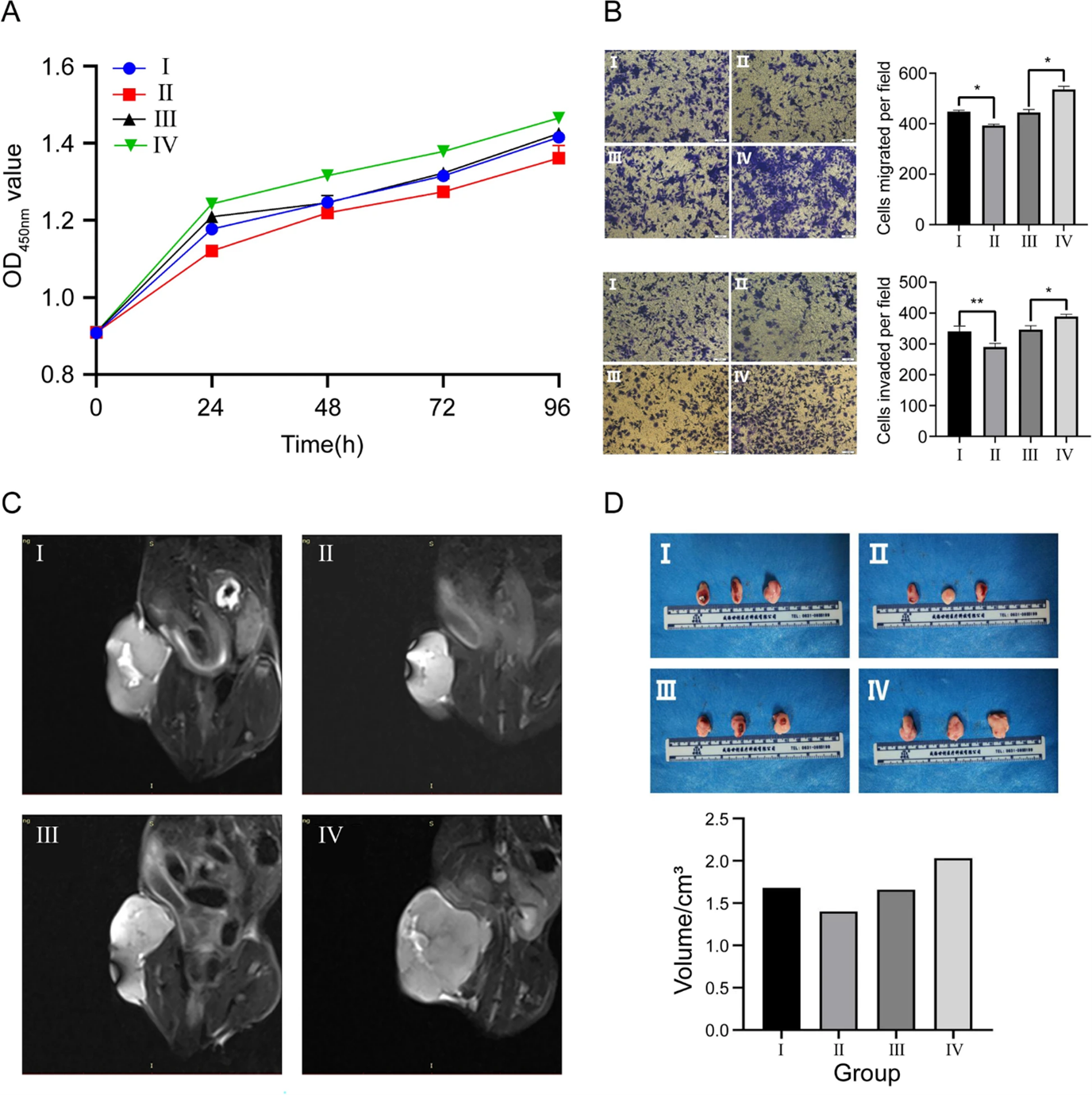
图3. MiR-144-3p 抑制操作系统增殖、侵袭和迁移
为了研究miR-144-3p是否通过铁死亡机制抑制OS生长,作者应用TEM、GSH等方式检测相关指标的改变。miR-144-3p过表达组表现为更显著的线粒体铁死亡畸变形态、较低的GSH / GSSG比率、升高的Fe2+水平、MDA水平和ROS水平。OS细胞和CDTX模型组织的WB、RT-qPCR和IHC结果显示miR-144-3p的表达与促铁死亡分子ACSL4呈正相关、与抗铁死亡分子xCT和GPX4负相关。
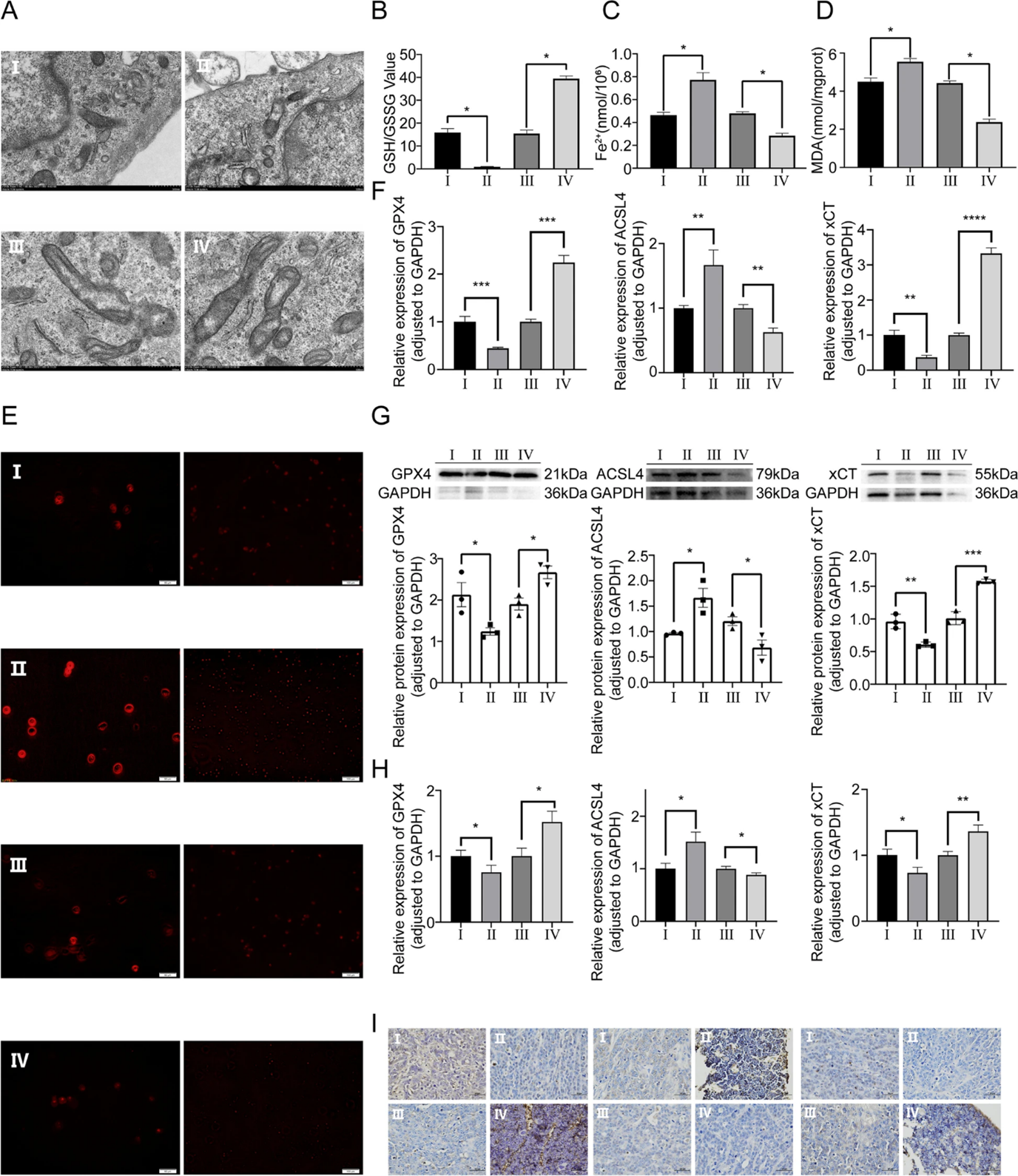
图4. MiR-144-3p正向调控细胞内铁死亡
随后,作者探究了ZEB1对体内和体外OS发展的影响。ZEB1过表达后OS细胞的活力、迁移和侵袭显著上升,肿瘤体积显著增加。ZEB1与线粒体铁死亡特异性形态改变、Fe2+水平、MDA和ROS,与GSH/GSSG比值正相关。OS细胞和CDTX模型组织的WB、RT-qPCR和IHC结果显示ZEB1的过表达导致ACSL4的表达水平降低,xCT和GPX4的表达水平升高。这表明ZEB1可以积极调节OS进展,且通过调节谷氨酰胺代谢抑制铁死亡,Fe2+稳态,MDA水平和ROS水平。
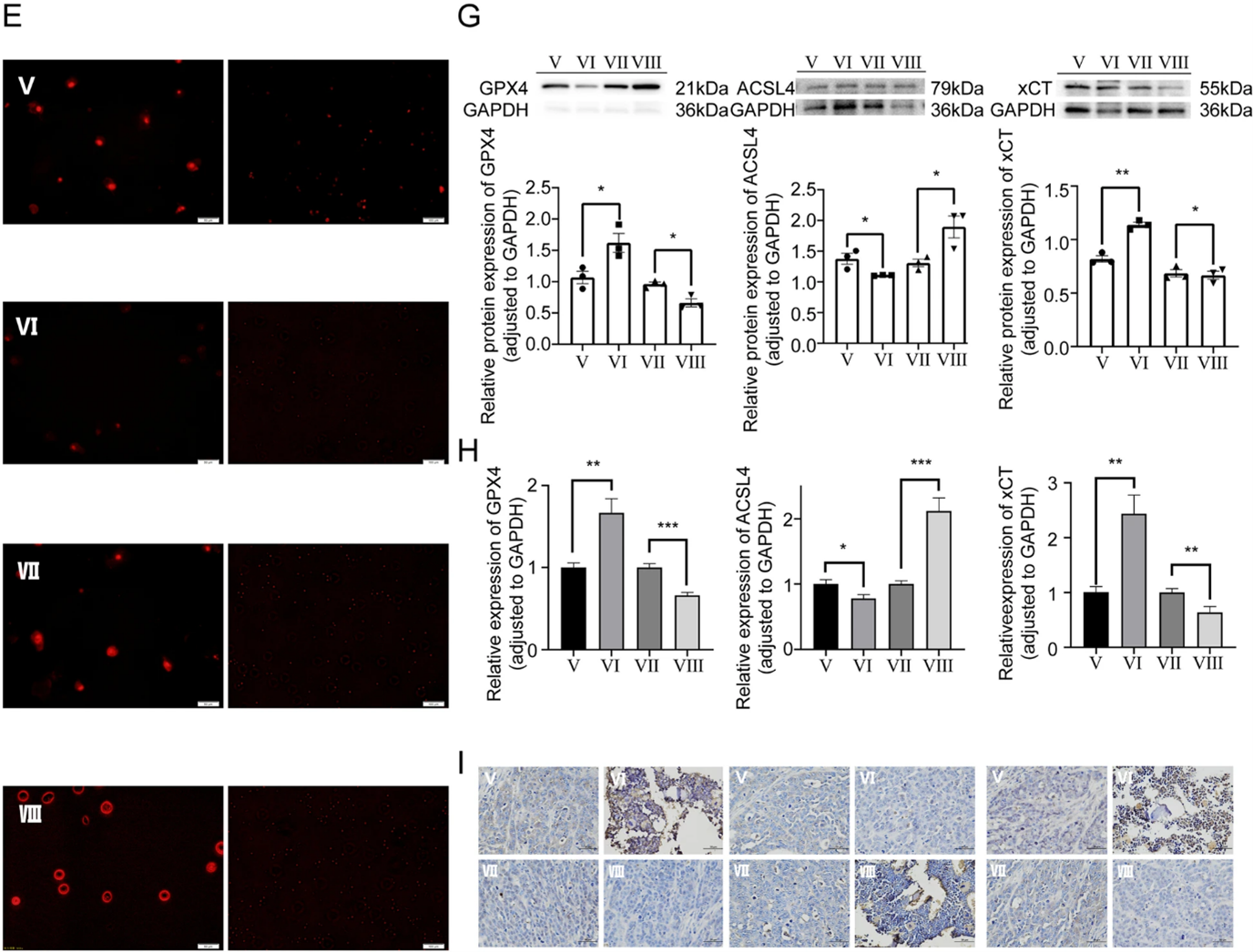
图5. ZEB1正向调节OS发展,其表达与铁死亡水平呈负相关
最后,作者设计了一个基于转染分组的功能挽救实验来验证miR-144-3p/ZEB1轴的功能和铁死亡机制。CCK-8测定和跨孔测定的结果表明ZEB1的过表达可以挽救miR-144-3p的肿瘤抑制作用,体内实验表明,miR-144-3p表达的增加可以通过调节ZEB1抑制OS生长。ZEB1可以恢复miR-144-3p对铁死亡相关途径的作用,包括线粒体形态, GSH/GSSG比值,Fe2+,MDA和ROS水平。ZEB1在体外实验和体内实验中挽救了由miR-144-3p改变的铁死亡相关分子表达。以上结果表明ZEB1可以通过调节铁死亡来挽救miR-144-3p对OS的影响。
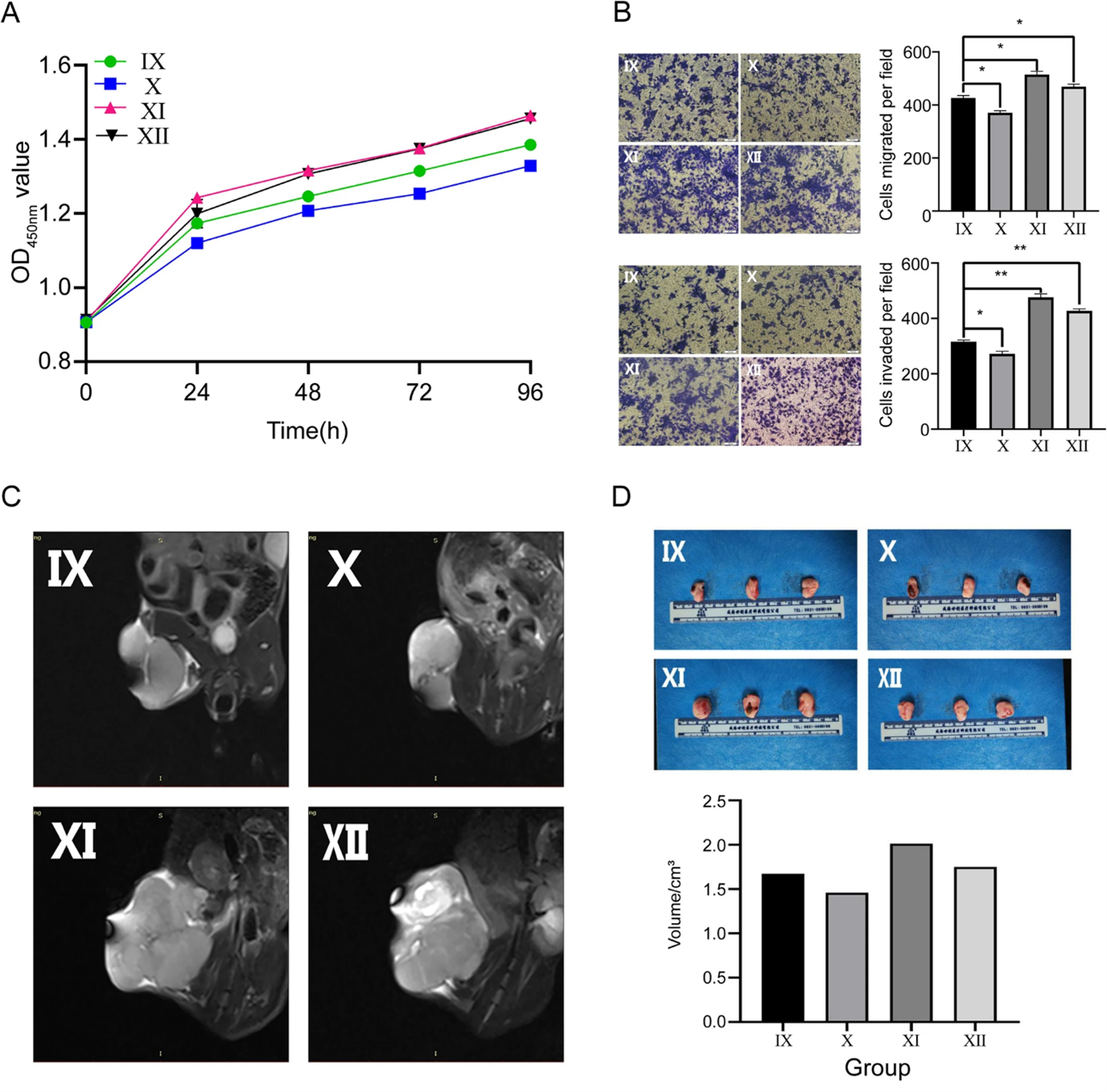
图6. ZEB1挽救miR-144-3p引起的增殖、侵袭和迁移改变
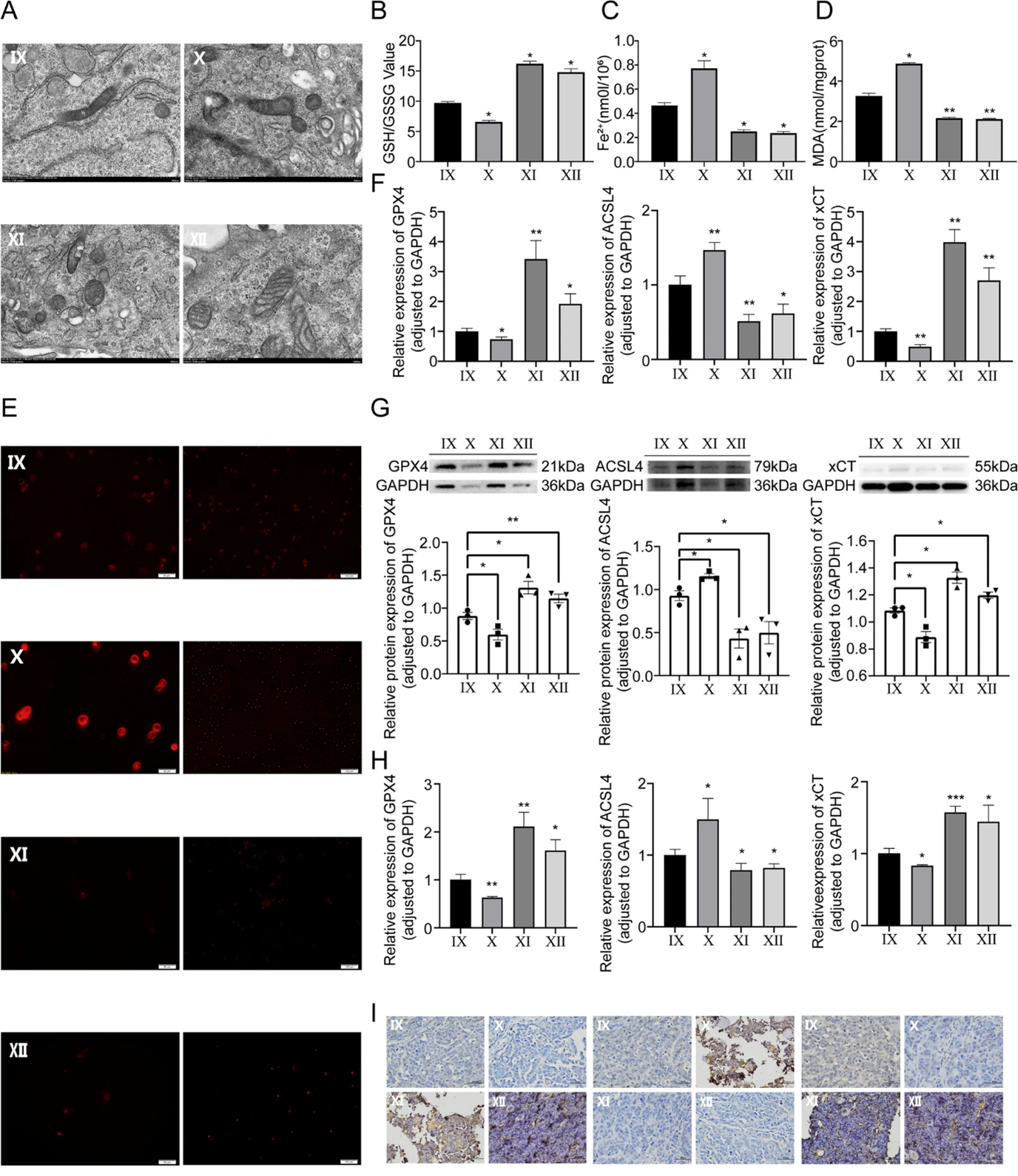
图7. ZEB1恢复miR-144-3p引起铁死亡变化
作者通过临床组织、体外细胞实验和体内CDTX模型等一系列实验证明了外泌体中的miR-144-3p和ZEB1可以通过调节铁死亡机制来调控OS的发育,这证实铁死亡相关的miRNA作为OS的抗癌治疗靶点或诊断生物标志物具有巨大潜力,但依然存在如样本规模相对较小等局限,这限制了研究的准确性。综上所述,该研究已证明miR-144-3p/ZEB1轴的治疗潜力,并为进一步揭示和阐述miRNA、铁死亡与OS之间的关系,探究抗癌治疗靶点或诊断性生物标志物打下基础。

查看更多

查看更多

查看更多

联系我们

返回顶部