查看更多

 明星产品
明星产品
 关注我们
关注我们

扫码关注我们
了解更多信息
骨肉瘤是一种高发于20岁以下青少年儿童的原发性恶性骨肿瘤。由于微转移灶的存在,仅采用根治性手术治疗的效果往往有限。自20世纪70年代以来,以MAP方案为代表的联合化疗的广泛应用,患者总体生存率已从约20%提高至约70%。尽管如此,该肿瘤仍普遍表现出化疗耐药性,约30-40%的患者化疗效果不佳或复发,成为当前临床治疗的主要挑战。近年来,随着对骨肉瘤分子特征认识的不断深入,其诊疗理念正逐步由传统模式向个体化治疗转变。因此,系统揭示骨肉瘤化疗耐药的分子机制,并鉴定其关键调控因子,对于优化治疗策略具有重要科学意义。

2025年7月19日,哈尔滨医科大学杨磊教授与袁野教授团队在Cell Death & Differentiation(IF=15.4)在线发表题为“MARCH8/NSUN6/ROS-mediated DNA damage positive feedback loop regulates cisplatin resistance in osteosarcoma”的研究论文。该研究首次揭示m⁵C甲基转移酶NSUN6(NOP2/Sun RNA甲基转移酶家族成员6)表达水平与骨肉瘤进展呈正相关,并阐明了其在顺铂耐药中的核心作用。汉恒生物有幸为本研究提供慢病毒Lenti-shNSUN6,在143B人骨肉瘤细胞中沉默NSUN6的表达,为揭示NSUN6的功能提供了关键工具。
下面,我们一起来看看具体的研究内容。
1.NSUN6高表达与骨肉瘤进展呈正相关
为探究m⁵C甲基化在骨肉瘤中的潜在作用,作者检测了人骨肉瘤细胞中总RNA的m⁵C修饰水平,发现骨肉瘤细胞系(特别是143B和U2OS)的m⁵C修饰水平显著高于正常人骨髓间充质干细胞(hBMSCs)。通过生物信息学分析发现,骨肉瘤组织中m⁵C修饰的关键催化酶NSUN2、NSUN6和NSUN7的表达水平升高,其中NSUN6的上调最为显著。数据库分析显示NSUN6在高分级骨肉瘤中高表达,且与患者不良预后相关。WB和qpcr实验也证实NSUN6在骨肉瘤细胞系和组织中的mRNA及蛋白水平均显著升高,提示其可能作为促癌因子参与骨肉瘤进展。
作者进一步做了功能实验,发现沉默NSUN6可显著降低细胞内m⁵C修饰水平,抑制骨肉瘤细胞增殖和克隆形成能力,并促进细胞凋亡。体内实验显示,敲低NSUN6能显著抑制小鼠模型中肿瘤的生长,表现为荧光强度减弱、肿瘤体积缩小和重量减轻。这些结果证明NSUN6通过调控m⁵C修饰在骨肉瘤进展中发挥重要作用,沉默NSUN6能在体内外有效抑制骨肉瘤细胞活性。

图1. NSUN6的表达水平与骨肉瘤恶性程度呈正相关
2.MARCH8通过保守结构域与NSUN6相互作用并介导其降解
为阐明NSUN6调控骨肉瘤发展的机制,作者对TARGET数据库中88例骨肉瘤样本进行差异分析,发现NSUN6高表达组显著富集于泛素连接酶结合通路。实验证实,相较于hBMSCs,143B和U2OS细胞中NSUN6蛋白泛素化水平降低,说明NSUN6在骨肉瘤中的表达上调可能源于泛素化修饰的减少。使用蛋白酶体抑制剂MG132处理可有效阻断NSUN6降解,表明该蛋白主要通过蛋白酶体途径被调控。
通过生信预测及实验验证,发现E3泛素连接酶MARCH8为NSUN6的互作蛋白。免疫荧光显示二者在细胞内共定位,分子对接模拟提示结合依赖盐桥和氢键,免疫共沉淀实验则证实了内源及外源表达条件下的直接结合。临床相关性分析显示,MARCH8高表达与患者良好预后呈正相关,且骨肉瘤组织中MARCH8与NSUN6表达水平呈显著负相关。综上所述,MARCH8可能通过结合NSUN6并促进其泛素化降解,在骨肉瘤中发挥抑癌作用。
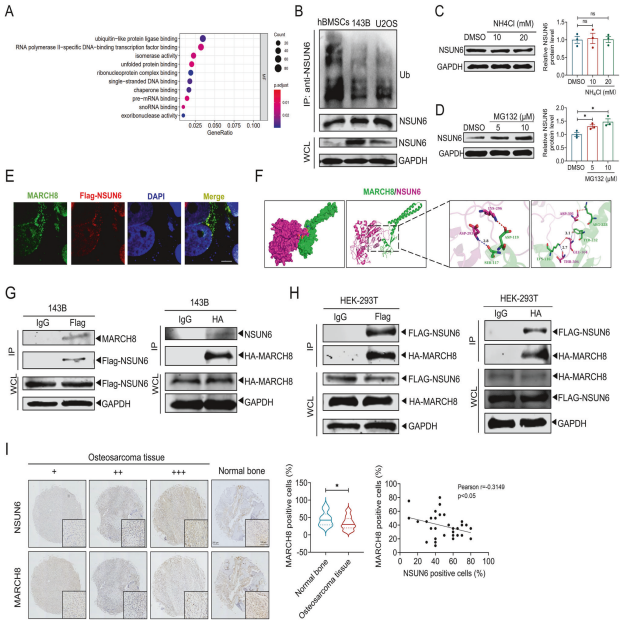
图2. MARCH8与NSUN6相互作用并调控其在骨肉瘤细胞中的泛素化
3.MARCH8催化NSUN6多聚泛素化降解
在HEK-293T和143B细胞系中,过表达MARCH8可显著增强NSUN6的泛素化水平,而其敲低则产生相反效果。进一步实验表明该过程依赖于K48型泛素链,且蛋白酶体抑制剂MG132能够逆转MARCH8介导的NSUN6降解。通过质谱分析和位点突变验证,最终确定NSUN6蛋白的K271和K462位点是MARCH8介导泛素化的关键靶点。这些结果共同表明MARCH8通过催化NSUN6第271和462位赖氨酸的K48连接型泛素化,促进其经蛋白酶体途径降解,从而调控NSUN6的蛋白稳定性。
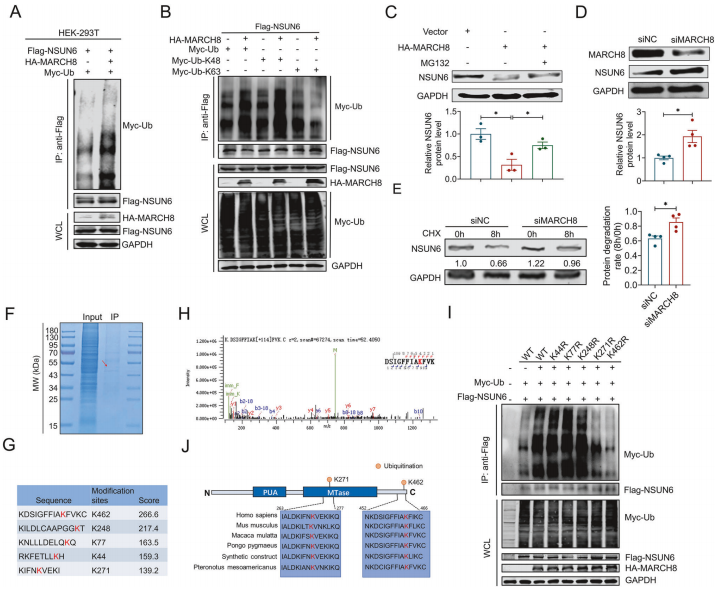
图3. MARCH8通过泛素-蛋白酶体途径介导NSUN6降解
4.NSUN6缺失抑制过氧化物酶体的合成并诱导ROS积累
为深入探究NSUN6在骨肉瘤发病机制中靶向的生物学通路,作者利用TARGET数据库中骨肉瘤mRNA表达数据进行了GSEA富集分析,发现NSUN6高表达显著富集于过氧化物酶体合成通路。NSUN6能正向调控过氧化物酶体标志蛋白ABCD3和过氧化氢酶(CAT)的表达,并促进过氧化物酶体生成。敲低NSUN6会导致细胞内及线粒体活性氧(ROS)积累,且ROS抑制剂NAC可逆转由此引起的细胞活力下降。进一步研究表明,MARCH8介导的NSUN6降解会抑制ABCD3和CAT表达,减少过氧化物酶体数量并增加ROS水平,最终抑制细胞增殖能力,而这些效应均可通过过表达NSUN6逆转。这些结果共同表明:MARCH8通过降解NSUN6抑制过氧化物酶体合成并升高ROS水平,进而削弱骨肉瘤细胞活力。
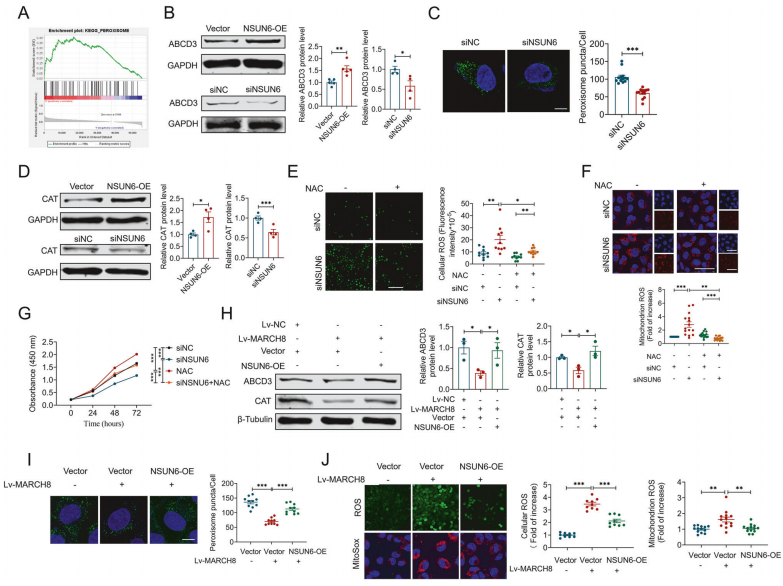
图4. NSUN6调控过氧化物酶体的合成和ROS的产生
5.NSUN6通过m⁵C-YBX1轴稳定PEX1/PEX3 mRNA,调控过氧化物酶体合成
为鉴定NSUN6调控过氧化物酶体合成调控中的靶基因,作者筛选了10个相关基因,发现NSUN6可上调PEX1、PEX3、PMP70和PPARα的mRNA水平。进一步研究表明,NSUN6通过催化PEX1和PEX3 mRNA的m⁵C修饰增强其稳定性,从而上调相应蛋白表达,而这一过程依赖于m⁵C阅读器蛋白YBX1的介导;NSUN6敲低可降低PEX1/PEX3 mRNA的m⁵C修饰水平及YBX1结合能力,而过表达NSUN6则呈现相反效应。更重要的是,在NSUN6过表达背景下敲低YBX1会逆转PEX1/PEX3 mRNA稳定性和蛋白表达的增加。这些结果提示,NSUN6通过m⁵C-YBX1依赖机制调控过氧化物酶体合成,进而参与ROS积累过程。
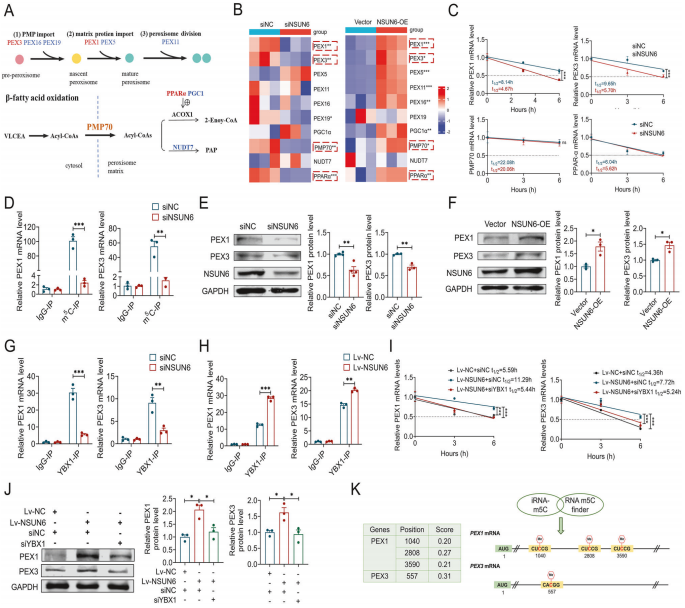
图5. NSUN6以m⁵C-YBX1依赖的方式增强PEX1和PEX3的RNA稳定性
6.敲低NSUN6会促进DNA损伤,进一步促进其泛素化降解
鉴于ROS积累可诱发DNA损伤,作者研究了NSUN6在此过程中的作用。敲低NSUN6会诱导ROS积累并上调DNA损伤标志物γ-H2AX,而抗氧化剂NAC处理可逆转这一效应。进一步实验表明,H₂O₂处理不仅能浓度依赖性地增加γ-H2AX水平,还会同时降低NSUN6蛋白表达,增强NSUN6与MARCH8的结合及其泛素化修饰。MARCH8敲低可阻断H₂O₂介导的NSUN6降解,证实该过程依赖MARCH8介导的泛素化途径。这些结果共同表明,由NSUN6下调触发的ROS积累和DNA损伤,形成了一个正向反馈循环,该循环通过增强NSUN6与MARCH8之间的相互作用,进而促进NSUN6的泛素化降解,从而放大其在骨肉瘤细胞中的调控效应。
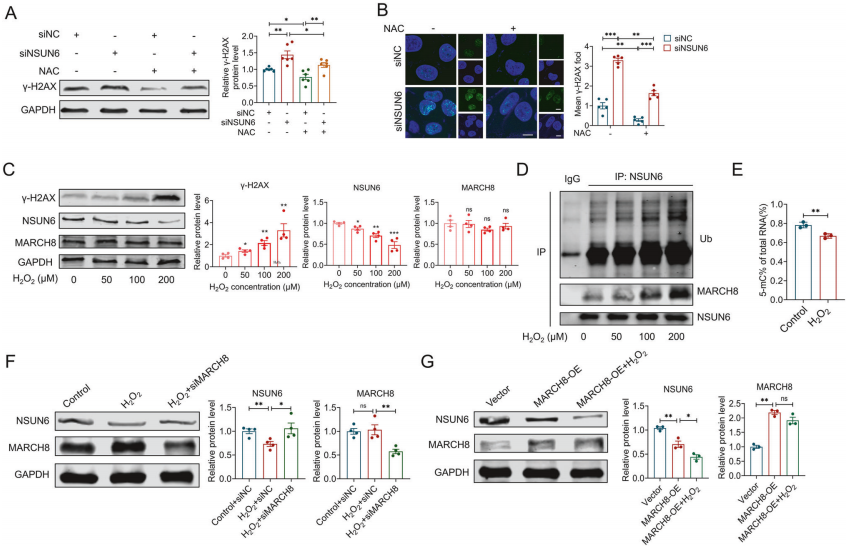
图6. NSUN6敲低引起的DNA损伤诱导其自身泛素化与降解
7.敲低NSUN6可增强骨肉瘤细胞对顺铂的化疗敏感性
为探讨NSUN6在顺铂耐药中的作用,作者开展了一系列功能实验。结果显示,过表达NSUN6能减轻顺铂诱导的DNA损伤(γ-H2AX水平下降),并提升细胞存活率和克隆形成能力。相反,沉默NSUN6则导致顺铂处理后的细胞活力明显下降。在皮下移植瘤模型中,NSUN6敲低联合顺铂治疗显著抑制了肿瘤生长、减小肿瘤体积/重量,并增加肿瘤细胞凋亡。机制上,NSUN6缺失通过促进细胞内ROS积累和增强DNA损伤,进而提高细胞对顺铂的敏感性。这些结果充分表明NSUN6通过调控ROS-DNA损伤轴介导骨肉瘤的顺铂耐药,靶向NSUN6可能成为逆转骨肉瘤化疗耐药的新策略。
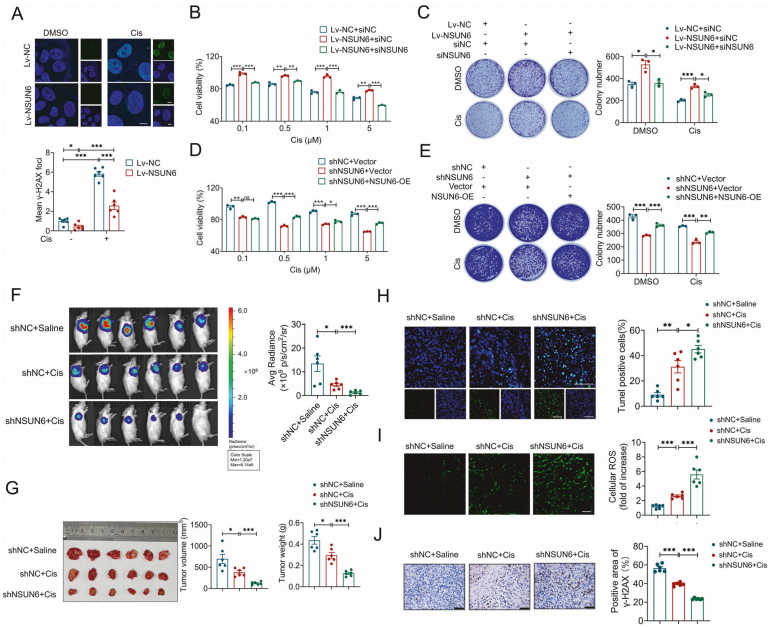
图7. NSUN6敲低可增强骨肉瘤细胞对顺铂的敏感性
8.NSUN6通过PEX1/PEX3介导的过氧化物酶体合成促进骨肉瘤的顺铂耐药性
为探究NSUN6介导的顺铂耐药是否依赖于PEX1/PEX3调控的过氧化物酶体合成,作者在稳定过表达NSUN6的143B细胞中敲低了PEX1或PEX3,发现敲低二者均能逆转NSUN6促进的细胞增殖和克隆形成能力。体内实验进一步表明,过氧化物酶体合成抑制剂NNC 55-0396可显著抑制NSUN6过表达导致的肿瘤生长增强。在顺铂处理条件下,敲低PEX1/PEX3功能或使用NNC 55-0396抑制剂均能增强肿瘤细胞对顺铂的敏感性,表现为细胞凋亡增加和克隆存活下降。这些结果充分证明NSUN6通过调控PEX1/PEX3介导的过氧化物酶体合成通路,缓解ROS诱导的细胞损伤,从而促进骨肉瘤的顺铂耐药。
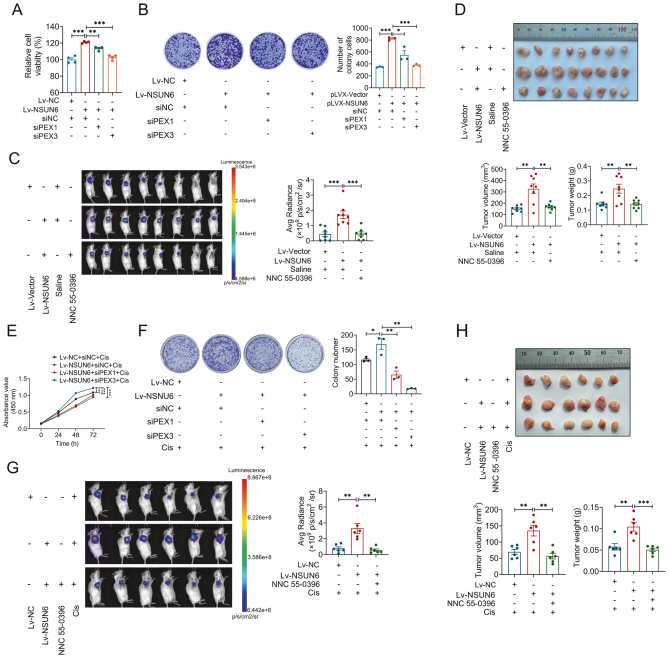
图8. PEX1与PEX3调控NSUN6介导的骨肉瘤增殖过程及顺铂敏感性
总结
综上所述,本研究首次阐明了MARCH8-NSUN6-YBX1-PEX1/PEX3反馈环路,该机制调控着骨肉瘤的进展和化疗耐药性。机制上,NSUN6作为m⁵C甲基转移酶,通过YBX1依赖的方式稳定PEX1/PEX3 mRNA,促进过氧化物酶体合成,进而清除细胞内ROS、缓解DNA损伤,赋予肿瘤细胞顺铂耐受能力。而这种ROS介导的DNA损伤随后会激活MARCH8对NSUN6的泛素化降解,从而形成一个正反馈循环。该环路不仅揭示了m⁵C修饰调控骨肉瘤化疗耐药的新机制,更为临床预后判断及克服顺铂耐药提供了潜在生物标志物和治疗靶点。

查看更多

查看更多

查看更多

联系我们

返回顶部