查看更多

 明星产品
明星产品
 关注我们
关注我们

扫码关注我们
了解更多信息
肝纤维化是导致肝脏疾病死亡的重要病理过程,包括代谢功能障碍相关脂肪性肝炎(metabolic dysfunction-associated steatohepatitis,MASH),而目前针对肝纤维化的治疗手段却非常有限。研究发现,肝内皮细胞(endothelial cells,ECs)和血管周围肝星状细胞(hepatic stellate cells,HSCs)中Rho关联的含卷曲螺旋蛋白激酶2(ROCK2)的上调会导致血管微环境功能障碍,并触发促纤维化血管旁分泌信号,预示着ROCK2可能是成药靶点。

2026年03月06日,四川大学丁楅森、曹中炜,中国医学科学院北京协和医学院王辰院士,泰德制药王红军、赵焰平,中国解放军总医院蔡芸,四川大学华西医院易成作为共同通讯作者在Cell在线发表标题为“Selective targeting of endothelial and perivascular angiocrine ROCK2 treats liver fibrosis”的研究报告,发现了血管ROCK2是一个促纤维化靶点,并开发了选择性靶向血管分泌的ROCK2抑制剂新药TDI01,为人类患者提供了一种治疗肝纤维化的方法。值得注意的是,在本研究中,作者使用了汉恒生物提供的腺相关病毒HBAAV2/8-alb-mir30-m-Rock2-ZsGreen,对小鼠肝细胞中Rock2基因进行了特异性敲低。

接下来,让我们一起来了解一下这篇文章吧。
首先,作者对人类肝脏进行了转录组分析。GEO数据库中编号为GSE193066的RNA测序数据显示,在人类MASH肝脏中,“Rho GTPase循环”通路显著富集。另一数据集GSE173735的分析同样表明,肝纤维化患者中富集了与Rho GTP酶相关的信号。这些通路与ROCK家族密切相关,而ROCK是激酶抑制剂的理想靶点。ROCK包括ROCK1和ROCK2两种亚型,其中ROCK2优先表达于肝内皮细胞和肝星状细胞,而ROCK1则广泛表达。在纤维化肝脏中,ROCK2在内皮细胞和肝星状细胞中表达上调,而ROCK1无明显变化,提示ROCK2可能在这些细胞中选择性表达增强。进一步检测发现,ROCK2蛋白人纤维化肝脏中随病情呈阶段性增加,免疫共染色显示,ROCK2及磷酸化ROCK2主要定位于肝窦内皮细胞,并在α-SMA+血管周围肝星状细胞中上调,而在其他细胞类型如CD45+免疫细胞和HNF4α+肝细胞中表达较低。ROCK2在人纤维化肝脏的内皮和血管周围区域的选择性上调表达,使其成为抗纤维化的潜在靶点。为探究ROCK2上调的机制,作者又分析了相关转录因子和受体的表达情况。结果显示,纤维化肝脏的内皮细胞或肝星状细胞中诱导了多个已知调控ROCK2的转录因子表达,如ZNF143、SMAD4、SRF、TEAD4、TEAD1和YAP1。同时,一些可上调ROCK2的受体(包括EPHA4、ESR1、F2R、LPAR1、NRP1、P2RY12和RTN4R)在纤维化肝细胞和肝星状细胞中也显著上调。这些因子的异常诱导可能促进了ROCK2在纤维化肝脏内皮细胞和肝星状细胞中的上调。
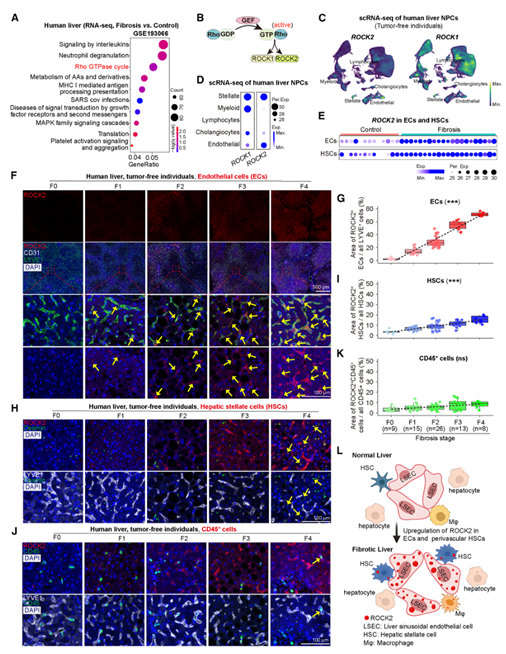
图1. ROCK2在人纤维化肝脏的血管内皮细胞及血管周围肝星状细胞中表达上调
随后,作者分析了CCl₄诱导的小鼠肝纤维化模型中ROCK2的表达情况,发现ROCK2在内皮细胞和肝星状细胞中表达上调。通过构建不同细胞类型特异性ROCK2敲除小鼠,发现内皮细胞或肝星状细胞中敲除ROCK2可减轻肝纤维化和肝损伤,而敲除造血细胞或肝细胞中的ROCK2则无明显效果,这与通过AAV在模型动物肝细胞中特异性敲低ROCK2看到的结果一致。在MASH模型中同样证实,内皮细胞和肝星状细胞的ROCK2缺失能改善肝纤维化和脂肪变性,在肝细胞敲低ROCK2则无此作用。这些研究表明,内皮细胞和肝星状细胞中ROCK2的上调是促进肝纤维化的关键因素。相比结构复杂难以靶向的Rho GTP酶,ROCK激酶更易被药物抑制,因此ROCK2激酶有望成为抗纤维化治疗的理想靶点。ROCK2在纤维化肝脏的内皮细胞和星状细胞中特异性上调,且对血管重塑作用更显著,选择性抑制ROCK2可能减少副作用。然而,现有ROCK抑制剂选择性及效能不足,亟需开发高选择性的下一代ROCK2抑制剂,并严格评估其抗纤维化效果。
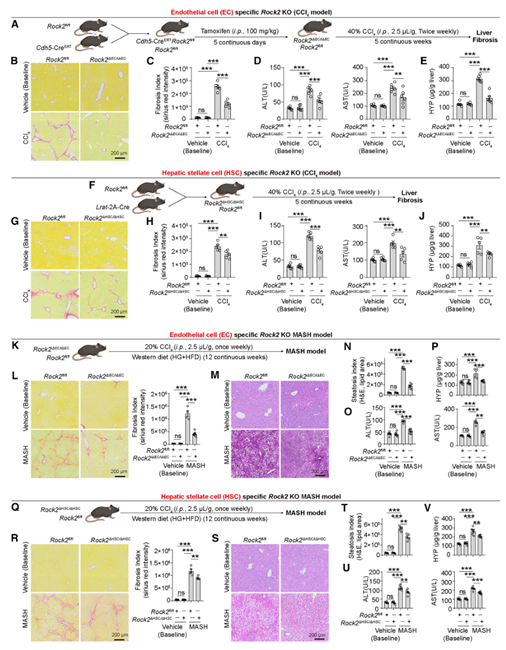
图2. 内皮细胞和肝星状细胞中敲除特异性ROCK2的基因可减轻小鼠模型肝纤维化和损伤
于是,作者开始寻找一种能够高效选择性抑制ROCK2的药物。基于ROCK2的晶体结构和已有的抑制剂信息,设计并合成了686个化合物,然后利用HTRF技术从中筛选那些只抑制ROCK2、不影响ROCK1的化合物。经过测试,找到了126个能有效抑制ROCK2的候选物,其中47个对ROCK2具有强抑制效果(IC50低于45 nM)。在这126个候选抑制剂里,有41个对ROCK1的抑制效果远弱于对ROCK2的(选择性指数>200)。结合这两个标准,筛选出了37个既高效又特异的化合物。接着,在小鼠中测试了这些化合物的药代动力学,有8个表现不错。随后评估了它们对人脐静脉内皮细胞和肝窦内皮细胞的毒性,其中TDI01470在很高浓度下细胞毒性极低(IC50>20 μM),它对心脏毒性也很低。在大鼠中进一步测试其药代动力学,口服15mg/kg具有较好吸收效率且生物利用度达到了56%。因此,选定TDI01470(分子式:C26H21F2N7O)作为最终候选药物,并命名为TDI01。它对ROCK2有极高的选择性,是ROCK1的598倍(对ROCK2的IC50为10.31 nM,对ROCK1的IC50达6159 nM)。基于此,TDI01有望通过高效特异性抑制ROCK2成为治疗纤维化疾病的新药。
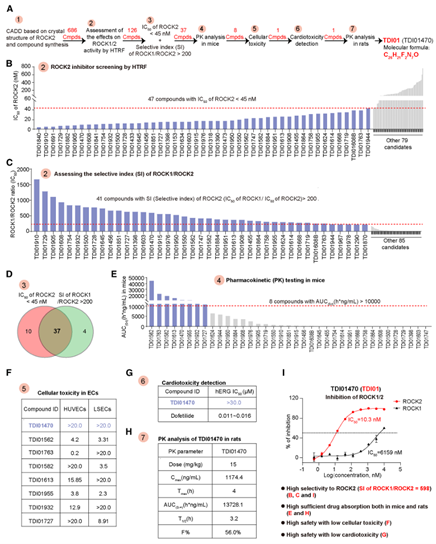
图3. 具有最佳药代动力学特性和安全性的ROCK2选择性抑制剂TDI01的鉴定
接下来,作者使用生物层干涉技术分析了TDI01与ROCK2和ROCK1激酶结构域的结合情况。结果显示,TDI01与ROCK2呈高亲和力结合(KD=65.56 nM),而与ROCK1在高达60 μM浓度下仍几乎无结合。使用生物素标记的TDI01进行pull-down实验并结合定量蛋白质组学分析,发现ROCK2是其作用最强的靶蛋白,Western blot也证实TDI01特异性结合ROCK2而非ROCK1。在细胞实验中,TDI01能剂量依赖性地抑制ROCK2活性,且在过表达ROCK2的细胞中抑制作用增强。通过冷冻电镜解析TDI01结合ROCK2的结构,发现ROCK2呈二聚体构象,TDI01结合于其ATP结合口袋附近的疏水区域,与F233残基形成π-π堆积作用。TDI01的结合使ROCK2呈现非活性状态的“DFG-out”构象,并导致αC螺旋发生位移。机制研究表明,ROCK2中的L210残基对维持这种构象变化和TDI01的特异性结合至关重要,而在ROCK1中对应的F194残基则因空间位阻阻止了这种变化。进一步通过L210F点突变实验验证了该残基的关键作用:L210F突变完全阻断了TDI01与ROCK2的结合,在ROCK2基因敲除细胞中,只有回补野生型ROCK2而非L210F突变体,才能恢复与TDI01的结合及其对ROCK2活性的抑制作用。这些结果阐明了TDI01通过识别ROCK2中L210残基实现选择性结合与抑制的分子机制。
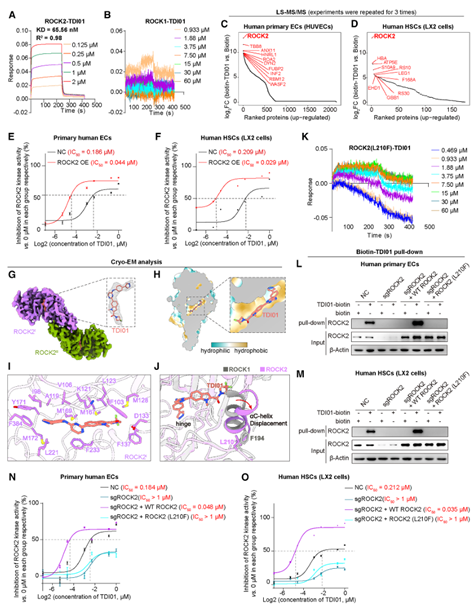
图4. TDI01作为ROCK2选择性抑制剂的特性表征
TDI01在多种临床前肝纤维化模型中均显示出显著的治疗效果。在CCl4诱导的小鼠肝纤维化模型及代谢相关脂肪性肝炎小鼠模型中,TDI01干预能够有效降低血清转氨酶水平与肝脏羟脯氨酸含量,并减轻肝纤维化程度及脂肪变性。鉴于迷你猪在模拟人类代谢紊乱方面较啮齿类动物具有更高的临床相关性,本研究进一步在CCl4诱导及代谢相关脂肪性肝炎迷你猪模型中评估了TDI01的疗效。药代动力学分析显示,单次口服5 mg/kg TDI01后,药物浓度在给药后4小时达峰(543.65 ng/mL),呈现非线性剂量依赖特征,支持每日一次给药方案。在为期9个月的治疗中,TDI01显著降低了肝脏硬度、胶原沉积及羟脯氨酸含量,并改善肝小叶炎症与脂肪变性,疗效优于甲状腺激素受体β激动剂瑞美替罗。单细胞转录组测序分析进一步揭示,TDI01可通过上调窗孔相关基因(如NOS3、PPARG、GATA4等)并抑制毛细血管化相关基因(如MMP2、COL1A1、HIF1A等)的表达,恢复肝窦内皮细胞的窗孔结构,逆转肝窦毛细血管化,从而发挥抗纤维化作用。以上结果表明,TDI01通过靶向ROCK2信号通路改善肝窦内皮细胞功能,在代谢相关脂肪性肝炎相关肝纤维化模型中具有明确的治疗潜力。
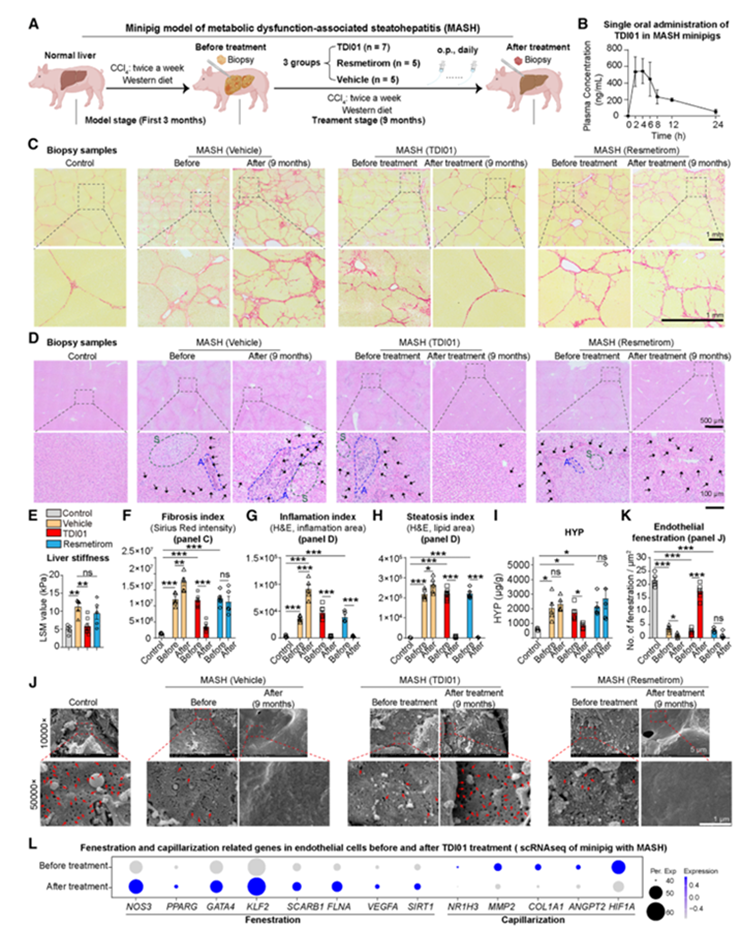
图5. TDI01可减轻小鼠和迷你猪模型中的肝纤维化
随后,作者又开展了一项针对肝纤维化患者的剂量递增临床试验(ChiCTR2400082056),以评估TDI01的安全性与初步疗效。低剂量组(200 mg)共纳入6例经病理活检确诊的患者,现已完成治疗及中期分析。结果显示,未见严重不良事件,药物吸收代谢特征与健康人群相当。治疗后,多数患者肝脏硬度值下降,部分患者的无创纤维化指标(S指数、GPR等)及肝功能指标(ALT、AST、ALB)有所改善。综上,低剂量TDI01在肝纤维化患者中显示出良好的安全性和抗纤维化潜力。
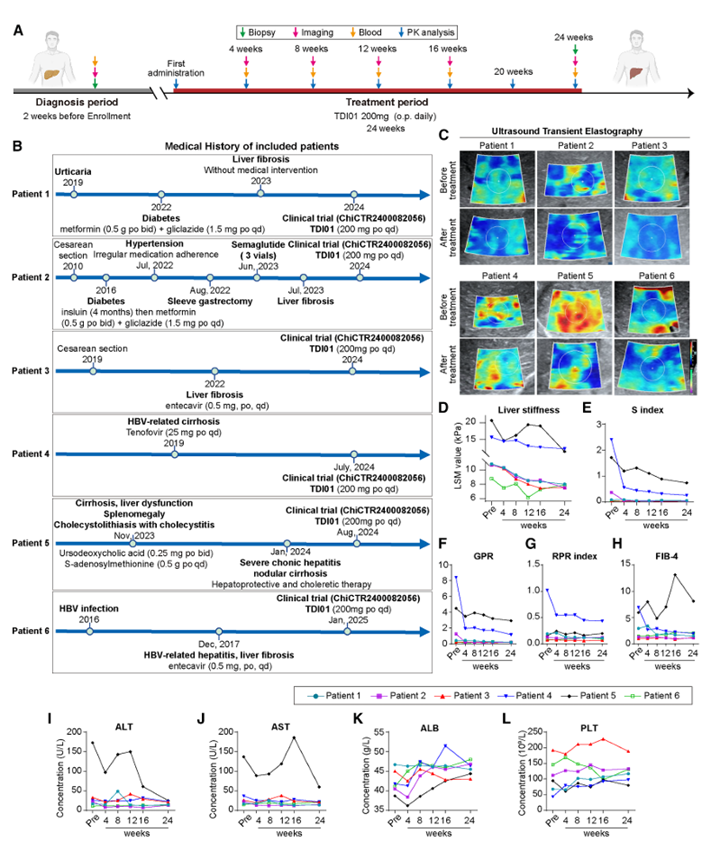
图6. 扩展的临床试验数据显示TDI01在6名受试患者中减轻了肝纤维化
在为期24周的治疗后,对6名患者进行了肝脏活检。结果显示,TDI01治疗显著减少了患者1-5的肝脏胶原沉积,并改善了纤维化分期和炎症,其中两位基线为肝硬化的患者也表现出组织学改善。机制上,TDI01选择性抑制了ROCK2活性。治疗期间未见严重不良事件,仅发生轻微不良反应。量临床实验初步表明TDI01在低剂量下安全有效,具有治疗肝纤维化的潜力。
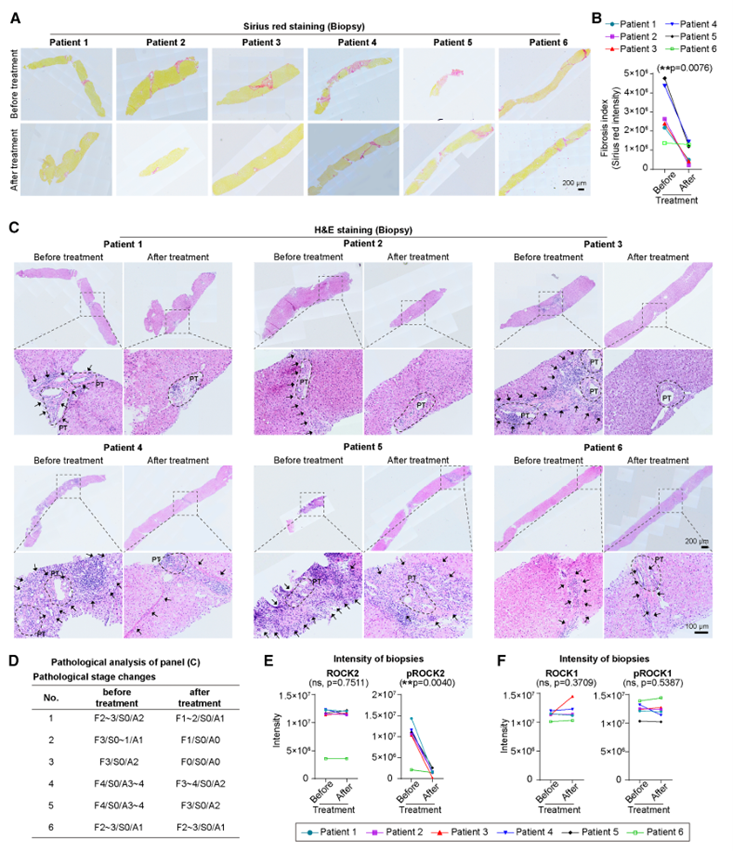
图7. 扩展临床试验活检样本表明TDI01通过抑制ROCK2活性改善纤维化
综上所述,该研究确定了ROCK2是一个肝脏纤维化的治疗靶点,并开发了ROCK2特异性抑制剂药物TDI01。与当前的其它类型ROCK抑制剂相比,TDI01的选择性指数显著更高。因此,这种具有更优的安全性和药代动力学特性的ROCK2选择性抑制剂在治疗肝纤维化方面具有独特的临床潜力。

查看更多

查看更多

查看更多

联系我们

返回顶部