查看更多

 明星产品
明星产品
 关注我们
关注我们

扫码关注我们
了解更多信息
2025年10月30日,北京大学药学院曾克武与屠鹏飞团队在《iMeta》期刊上发表题为“Homoharringtonine suppresses acute myeloid leukemia progression by orchestrating EWSR1 phase separation in an m6A-YTHDF2-dependent mechanism”的研究论文。该研究阐述了传统用于治疗慢性髓系白血病(CML)的药物高三尖杉酯碱(HHT)的全新作用机制:它通过驱动EWSR1蛋白发生液-液相分离,进而以m6A-YTHDF2依赖性方式抑制急性髓系白血病(AML)的进展。值得注意的是,在本研究中,作者使用了汉恒生物提供的lenti-shEWSR1敲低慢病毒及其对照慢病毒,成功构建了NB4细胞稳转株,为后续机制研究奠定了可靠基础。

AML是一种起源于骨髓造血干细胞的恶性血液肿瘤,其特征是骨髓中异常白血病细胞的快速增殖,并因分化成熟受阻而抑制正常造血功能,通常病情进展迅猛、预后较差。在临床治疗中,尤其是急性早幼粒细胞白血病(APL)亚型,三氧化二砷联合全反式维甲酸已成为标准疗法。然而,针对其他更为复杂的AML亚型,目前仍多依赖联合化疗方案。研究表明,当HHT与砷剂及全反式维甲酸联用时,可产生显著的协同抗白血病效应。不过,HHT在AML中的作用靶点尚未完全明确。通过评估HHT相关靶基因的表达水平,有望识别出对HHT治疗更敏感的AML患者亚群。
本文通过蛋白质组学与生物物理学方法,鉴定出EWS RNA结合蛋白1(EWSR1)是HHT的关键作用靶点,并阐明HHT通过结合EWSR1促进其寡聚化及液-液相分离(LLPS),进而招募m6A识别因子YTHDF2,干扰m6A依赖的mRNA降解过程,最终破坏白血病细胞稳态、抑制AML增殖的作用机制。该研究提示HHT可作为靶向EWSR1的小分子药物,为EWSR1高表达的AML患者提供了精准治疗的新方向。
下面,我们一起来了解具体的研究内容:
1.EWSR1被鉴定为AML中HHT的细胞靶点
为明确高HHT的直接作用靶点,作者使用生物素标记的HHT探针筛选人类蛋白质组微阵列,并以信噪比(SNR > 3)量化结合信号,初步获得42个高置信度候选蛋白。进一步结合同位素标记定量蛋白质组学分析,发现EWSR1在所有候选蛋白中富集最为显著,提示其为HHT的关键潜在靶标。临床数据分析显示,EWSR1在AML患者中呈显著高表达且与不良预后相关。此外,EWSR1蛋白水平与HHT的半数抑制浓度(IC50)呈负相关,表明EWSR1高表达的AML患者可能对HHT更为敏感,这提示EWSR1表达与AML细胞对HHT的治疗反应存在潜在关联。
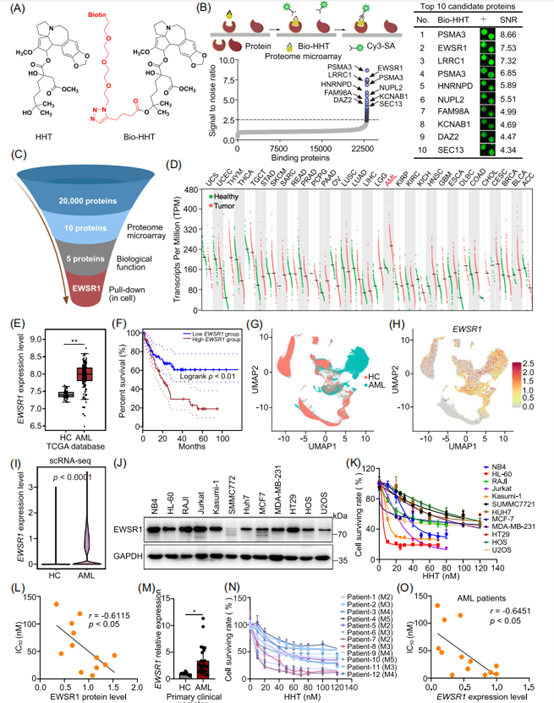
图1. EWSR1被鉴定为AML中HHT的细胞靶点
2.EWSR1的RNA识别结构域介导HHT结合
为验证HHT与EWSR1之间的相互作用,作者采用表面等离子共振(SPR)与微量热泳动(MST)技术,证实二者具有显著的结合亲和力。为进一步明确结合区域,作者将EWSR1蛋白分为N端区域(氨基酸1-300)与C端区域(氨基酸301-656,含RNA识别结构域)。下拉实验显示,HHT特异性结合于EWSR1的C端区域;随后的MST与SPR实验进一步证实,HHT与EWSR1-C端存在特异性相互作用。这些结果共同证明,EWSR1的RNA识别结构域是HHT结合的关键区域。
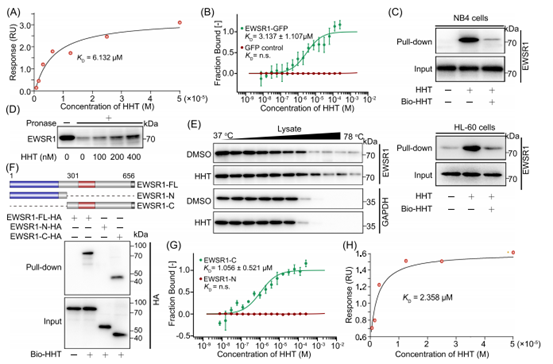
图2. HHT结合EWSR1的RNA识别结构域
3.HHT通过氢键与EWSR1的RNA识别基序结合
为深入解析HHT与EWSR1的结合机制,作者合成了HHT光亲和标记探针(HHT-PAL),并聚焦于EWSR1-C端(尤其是RNA识别基序)进行研究。实验显示,HHT-PAL与EWSR1-C在紫外照射下发生共价交联,经液相色谱-串联质谱(LC-MS/MS)分析鉴定出两个分子量增加的特定肽段,其交联位点位于EWSR1的RNA识别基序(353–453)内。
分子对接进一步发现,HHT可与EWSR1的T393、P396、M397和I400残基形成氢键,并与H399存在π-π堆叠作用。后续作者构建了EWSR1-C单点及多点突变体,并通过MST与下拉实验验证:T393A、P396A、I400A及Mut4突变体的结合能力显著降低,而M397A突变体与野生型结合力相当。该结果证实T393、P396与I400是HHT在EWSR1 RRM结构域中的关键结合位点,且HHT可能通过多重氢键与EWSR1结合,进而调控下游信号通路。
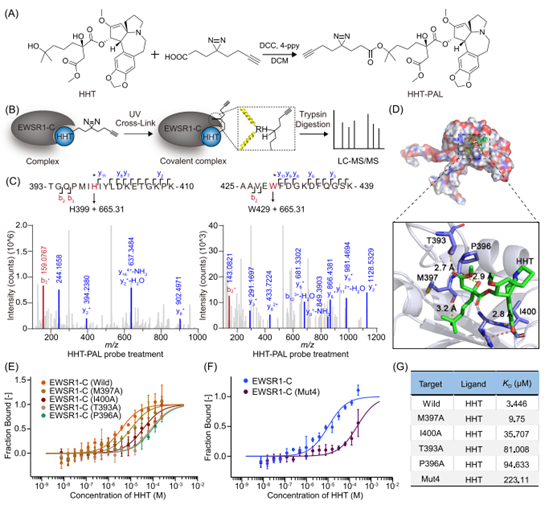
图3. HHT通过氢键与RNA识别基序相互作用
4.HHT促进EWSR1蛋白的液滴形成
前期研究提示EWSR1易于发生液-液相分离并在细胞内形成蛋白凝聚体。作者通过生物信息学分析发现,EWSR1的N端转录激活域及C端富含RGG的区域均属于内在无序区域。过表达GFP标记的EWSR1后,可在细胞内观察到动态斑点,荧光漂白恢复(FRAP)显示其在80秒内出现荧光恢复,且斑点可发生融合;经1,6-己二醇处理后斑点数量显著减少,证实其具有液态特性。进一步利用光诱导相分离系统(融合光敏蛋白Cry2)证明,EWSR1-N与EWSR1-C均能形成液滴。FRAP实验发现,HHT处理可显著降低EWSR1及EWSR1-C液滴的荧光恢复速率,并促进EWSR1-C凝聚体的形成,提示HHT可能在体外驱动EWSR1-C的构象转变与相分离进程。
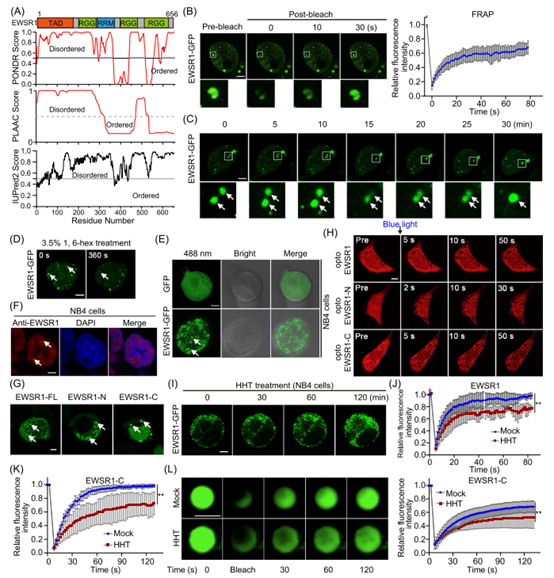
图4. HHT促进EWSR1蛋白的液相分离
5.HHT 通过变构机制促进EWSR1相分离
为阐明HHT调控EWSR1相分离的分子机制,作者构建了基于双分子荧光互补(BiFC)的报告系统,将荧光蛋白片段VN173与VC155分别融合于EWSR1-C端,获得EWSR1-VN与EWSR1-VC载体。共转染后,EWSR1可通过自相互作用重建荧光,证实其能形成同源二聚体或寡聚体;而HHT以浓度依赖的方式增强该相互作用。色氨酸荧光分析显示,HHT可降低EWSR1-C的荧光强度,提示其诱导蛋白构象变化。圆二色谱分析进一步表明,随HHT浓度升高,EWSR1-C的α-螺旋含量降低,可能促进蛋白聚集。氢-氘交换质谱(HDX-MS)分析发现,HHT显著提高了两条关键肽段(NKRTGQPMIHIYL与FAWRTECNQ)的氘交换速率,其中NKRTGQPMIHIYL肽段对RNA识别及HHT结合至关重要。综上,HHT可通过变构效应促进EWSR1寡聚化,进而加速其相分离与液滴形成。
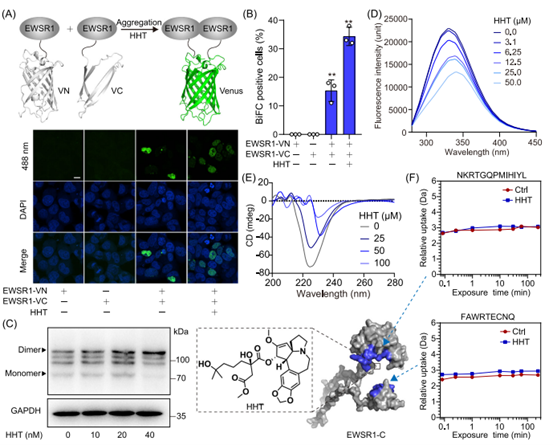
图5. HHT通过变构调节促进EWSR1相分离
6.HHT增强EWSR1-YTHDF2相互作用以抑制m6A识别
接下来,作者通过蛋白质组学分析及免疫共沉淀(Co-IP)实验,鉴定出EWSR1的底物蛋白YTHDF2,且两者表达呈正相关。体外实验表明HHT能够增强EWSR1的C端区域与YTHDF2 的YTH结构域相结合,分子对接也支持这一结论。鉴于YTHDF2在识别并降解m6A修饰RNA中的关键作用,作者推测EWSR1相分离可能通过募集YTHDF2干扰其正常功能。实验证实,在HHT作用下,EWSR1可作为YTHDF2介导的m6A识别的负调控因子。此外,m6A点杂交实验及时序分析发现,HHT处理使细胞整体的m6A水平呈浓度和时间依赖性升高,这可能是由于YTHDF2功能被破坏后,m6A修饰的RNA无法被有效降解而导致积累。这些结果共同表明,EWSR1是HHT调控YTHDF2 m6A识别功能的核心靶点。
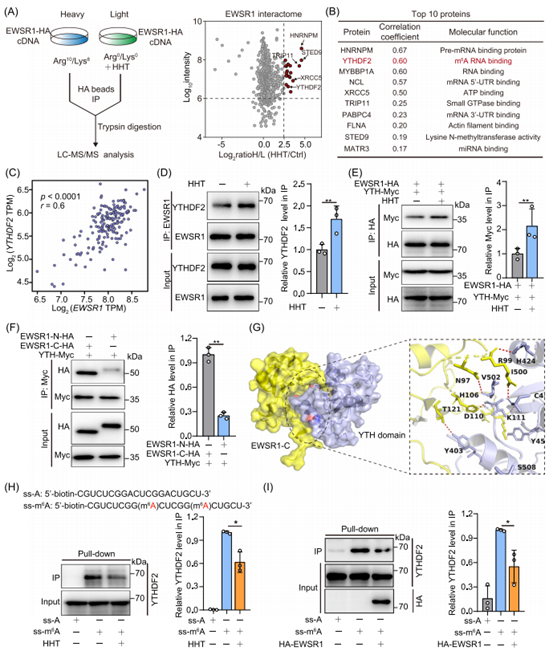
图6. HHT增强EWSR1-YTHDF2相互作用,限制m6A识别
7.HHT通过EWSR1-YTHDF2轴稳定m6A修饰的转录本
基于EWSR1参与RNA代谢的已知功能,作者在NB4细胞中进行了系列实验。RNA测序显示,HHT处理引起6036个基因上调和5862个基因下调,差异基因富集于线粒体自噬等通路;而在EWSR1敲低细胞中,检测到2121个基因上调和1421个基因下调。对比发现,HHT处理组与EWSR1敲低组共有2872个基因的表达变化重叠,进一步支持EWSR1是HHT的功能靶点。同时,HHT处理后多个TNFRSF家族基因显著上调。甲基化RNA免疫沉淀测序(MeRIP-seq)显示,m6A修饰上调的基因富集于TNF通路,而下调的m6A修饰基因则与自噬和AMPK信号通路相关。qRT-PCR结果进一步表明,HHT能抑制TNFRSF1B和HMOX1 mRNA的降解,并减少它们与YTHDF2的结合。这些发现提示,HHT通过增强EWSR1-YTHDF2互作,抑制YTHDF2对m6A修饰靶基因(如TNFRSF1B和HMOX1)的识别与降解,从而促进白血病细胞凋亡。
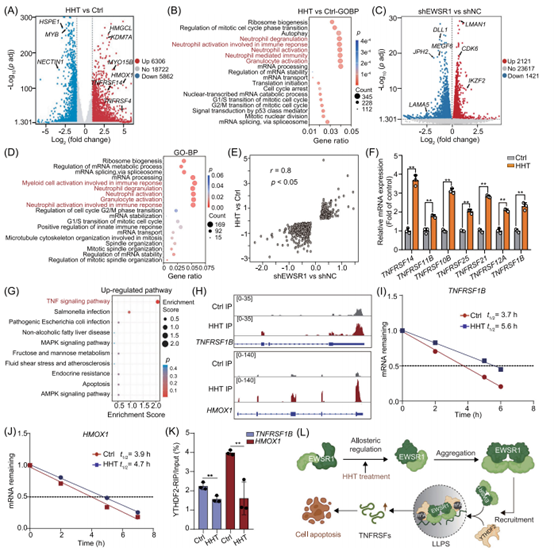
图7. HHT通过EWSR1-YTHDF2轴调节m6A修饰RNA的稳定性
8.EWSR1作为体内急性髓系白血病(AML)的治疗靶点
最后,作者构建了稳定敲低EWSR1的NB4和Kasumi-1细胞系,并将其移植至NOD/SCID与NOG免疫缺陷小鼠中建立AML模型。通过流式细胞术与生物发光成像(BLI)动态监测白血病进展,并给予HHT治疗(0.5 mg/kg,尾静脉注射,持续4周)。结果显示,在对照组小鼠中,HHT能有效抑制白血病进展并显著延长小鼠生存期;然而在EWSR1敲低模型中,HHT未能进一步抑制疾病或延长生存期,说明EWSR1是HHT发挥疗效的必要条件。小鼠存活曲线亦表明,HHT治疗与EWSR1敲低均可显著延长其生存期,但二者联合并未产生叠加效应。综上所述,该研究在体内水平证实EWSR1是HHT抗AML作用的直接靶点。
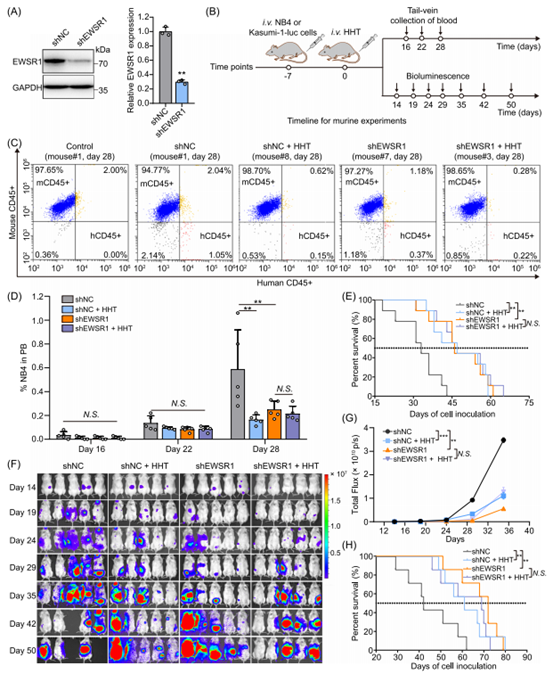
图8. 用HHT靶向EWSR1抑制AML体内进展
总结
综上所述,本研究确立了EWSR1作为HHT治疗AML的关键靶点,揭示了HHT通过调控EWSR1液-液相分离抑制AML进展的分子机制,并进一步阐明了EWSR1-YTHDF2-m6A轴在AML发生发展中的重要调控作用。这一发现不仅为HHT的临床应用提供了直接机制依据,也为针对不同遗传背景的AML患者开发靶向EWSR1的精准治疗策略提供了新思路。

查看更多

查看更多

查看更多

联系我们

返回顶部