查看更多

 明星产品
明星产品
 关注我们
关注我们

扫码关注我们
了解更多信息
胰腺癌(PC)是一种高致死性的消化道肿瘤,预后极差,5年生存率仅约10%。缺氧是包括PC在内的实体瘤的典型微环境特征,可诱导肿瘤细胞发生葡萄糖代谢重编程,促进肿瘤进展。环状RNA(circRNA)可在缺氧条件下被诱导表达,部分circRNA具有编码蛋白的能力,参与肿瘤的恶性进程。然而,PC中与缺氧相关的circRNA编码的蛋白质仍未得到充分表征和阐释。

2025年11月11日,重庆大学附属人民医院/重庆医科大学研究团队合作在期刊《Molecular Cancer》(IF=33.9)上发表了题为“A novel protein cPFKFB4 encoded by hsa_circ_0065394 strengthens PKM2-mediated glucose metabolic reprogramming to facilitate pancreatic cancer progression under hypoxia”的研究论文,在这项研究中,作者采用缺氧细胞培养系统筛选出高表达的hsa_circ_0065394,通过qRT-PCR、组织芯片、双荧光素酶报告基因实验、质谱分析和Western blot等方法验证其表达特征及编码蛋白cPFKFB4的能力,并利用体外功能实验(CCK-8、Transwell、糖酵解检测)和裸鼠移植瘤模型阐明其生物学功能;在机制层面,作者通过免疫共沉淀(Co-IP)、液相色谱-质谱联用(LC-MS)、RNA免疫共沉淀(RIP)、RNA剪接分析等技术手段发现,cPFKFB4通过特异性结合hnRNP G,破坏其与hnRNP A1的相互作用,从而增强hnRNP A1介导的PKM剪接向PKM2亚型转换,最终强化糖酵解并促进PC在缺氧条件下的增殖与转移。该研究不仅揭示了缺氧-circRNA编码蛋白-代谢重编程轴在PC进展中的新机制,也为开发针对cPFKFB4/PKM2通路的诊断标志物和靶向治疗策略提供了理论依据。
在本研究中,汉恒生物有幸为作者提供了以下产品:
慢病毒(hsa_circ_0065394过表达和敲低)建立hsa_circ_0065394过表达或敲低的PC稳转株;嘌呤霉素(Puro)筛选稳转株;细胞增殖检测试剂盒(CCK8)细胞增殖检测;双荧光素酶报告基因检测试剂盒(Dual-luciferase reporter assay)荧光素酶活性检测。
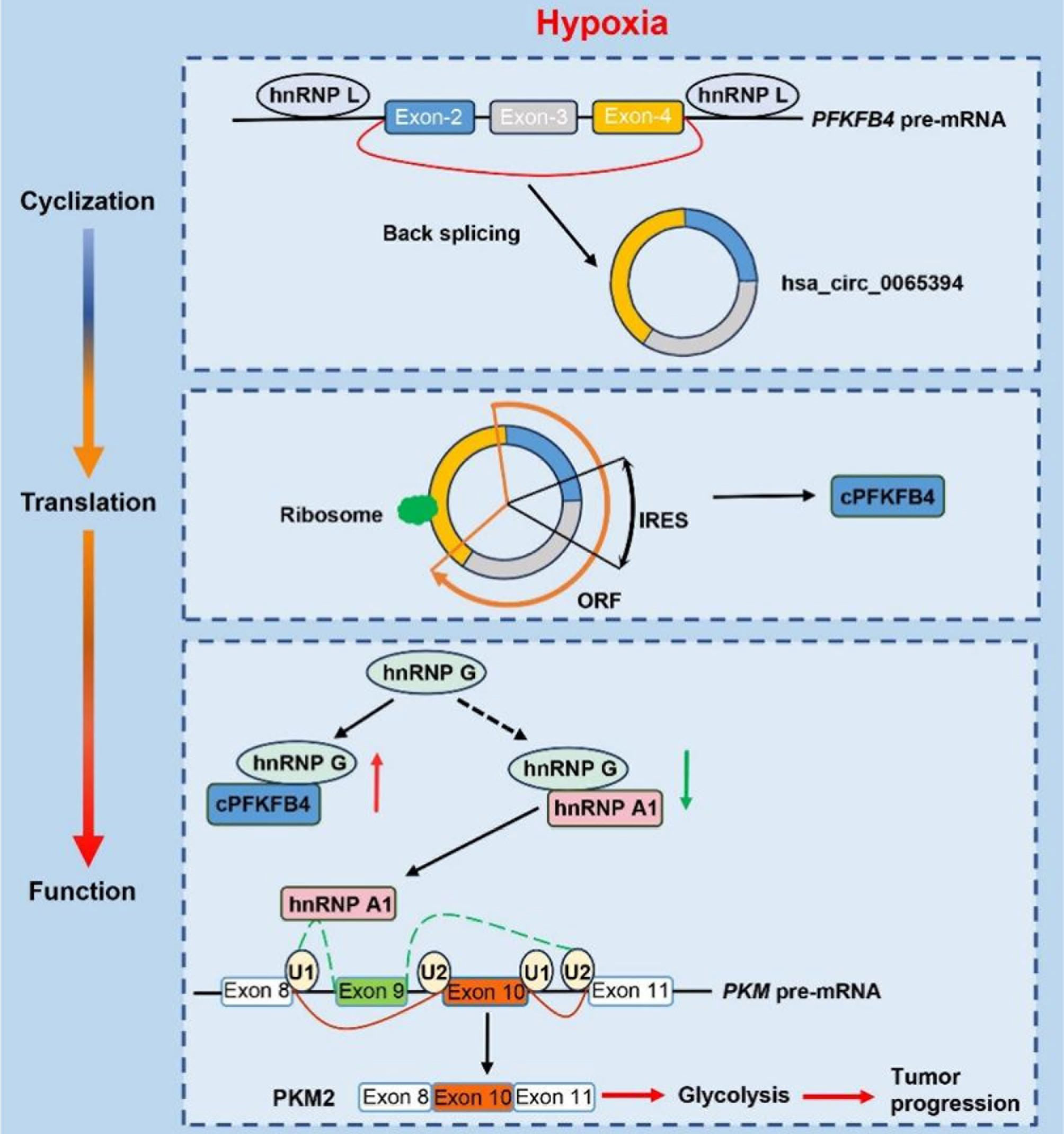
图1. cPFKFB4促进缺氧胰腺癌进展的机制示意图
接下来,我们一起看看本研究的主要结果:
缺氧条件下PC细胞中hsa_circ_0065394的鉴定
PFKFB4是调控糖酵解通量的核心酶,直接影响肿瘤细胞的能量代谢和氧化还原平衡,因此,作者推测:源自PFKFB4 基因的circRNA可能是驱动前列腺癌细胞适应缺氧微环境并持续恶变的关键分子。为从PFKFB4来源的circRNA中筛选出缺氧诱导的circRNA,作者在常氧和缺氧条件下培养的PC细胞中检测了五个来源于PFKFB4的circRNA的表达水平。在这些circRNA中,与常氧PC细胞相比,hsa_circ_0065394在缺氧细胞中表达上调最为显著,且丰度最高。Sanger测序证实,hsa_circ_0065394是由PFKFB4基因的第2、3、4号外显子头尾连接剪接形成的281个核苷酸的circRNA。PCR产物的琼脂糖凝胶电泳显示,只有使用背靠背引物(divergent primers)才能从cDNA中扩增出hsa_circ_0065394,排除了基因组重排和反式剪接的可能性。RNase R实验进一步证实,由于缺乏5'帽和3' poly(A)尾,hsa_circ_0065394能抵抗RNase R的降解。与正常细胞相比,在放线菌素D(Actinomycin D,ActD)处理的细胞中,hsa_circ_0065394的水平明显高于mRNA,表现出更长的半衰期。核质分离实验表明,hsa_circ_0065394同时分布于细胞核和细胞质中。总而言之,该研究结果表明,hsa_circ_0065394是一种在PC中丰富且稳定表达的缺氧响应性circRNA。
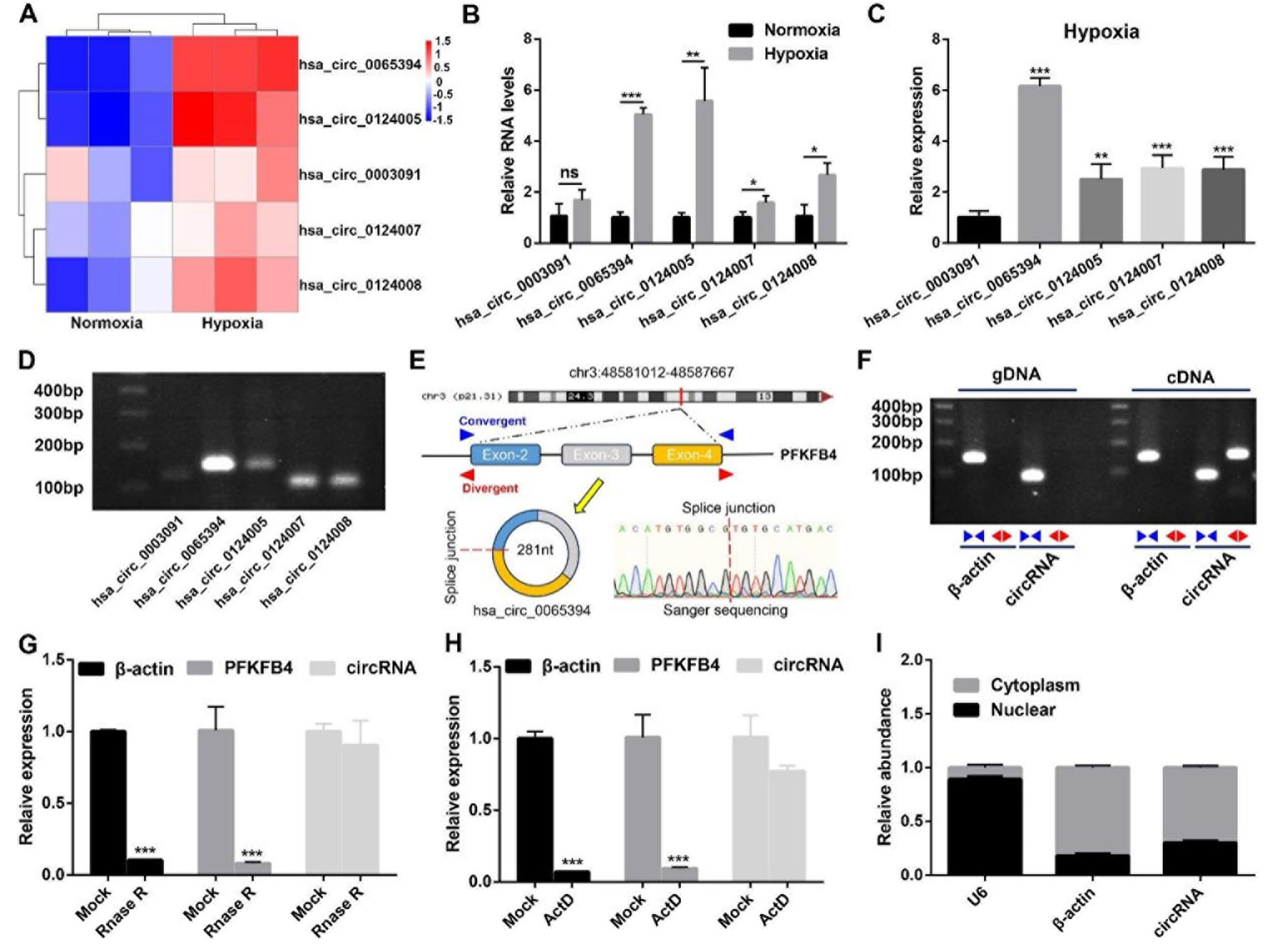
图2. 缺氧条件下PC细胞中hsa_circ_0065394的验证与表征
hsa_circ_0065394的生物发生
现有研究表明,外显子侧翼内含子中的反向互补序列(如Alu重复序列)和反向串联重复序列可促进circRNA的形成。为深入探究hsa_circ_0065394的环化机制,作者利用NCBI数据库筛选到位于其侧翼内含子区域的Alu重复元件AluYc和AluSx1。随后,作者构建了包含或缺失AluYc和AluSx1的缺失突变体,qRT-PCR结果表明,只有当AluYc和AluSx1同时存在时,才能显著上调hsa_circ_0065394的表达。越来越多的证据表明,一些RNA结合蛋白(RBPs)能与前体mRNA侧翼内含子序列中的特定位点结合,使下游和上游的剪接外显子在空间上彼此靠近,从而提高circRNA的环化效率。为探究RBPs是否参与了hsa_circ_0065394的环化过程,作者针对已知在circRNA生物发生中起重要作用的八种RBPs(ADAR、FUS、DHX9、QKI、ESRP1、hnRNP L、EIF4A1和EIF4A3)设计并合成了靶向siRNA,并用qRT-PCR检测了这些RBPs的敲低效率及各实验组中hsa_circ_0065394的表达谱。qRT-PCR结果显示,只有在转染hnRNP L siRNA的细胞中,hsa_circ_0065394的表达受到负向调控,这表明hnRNP L对hsa_circ_0065394的生物发生至关重要。随后,作者利用RBP map数据库预测了PFKFB4前体mRNA与hnRNP L的结合位点,并设计了特异性引物。接着,作者使用hnRNP L抗体进行的RIP实验表明,hnRNP L在B位点和C位点显著富集。上述结果表明,hnRNP L通过与PFKFB4前体mRNA的特定位点结合,加速了hsa_circ_0065394的生物发生。
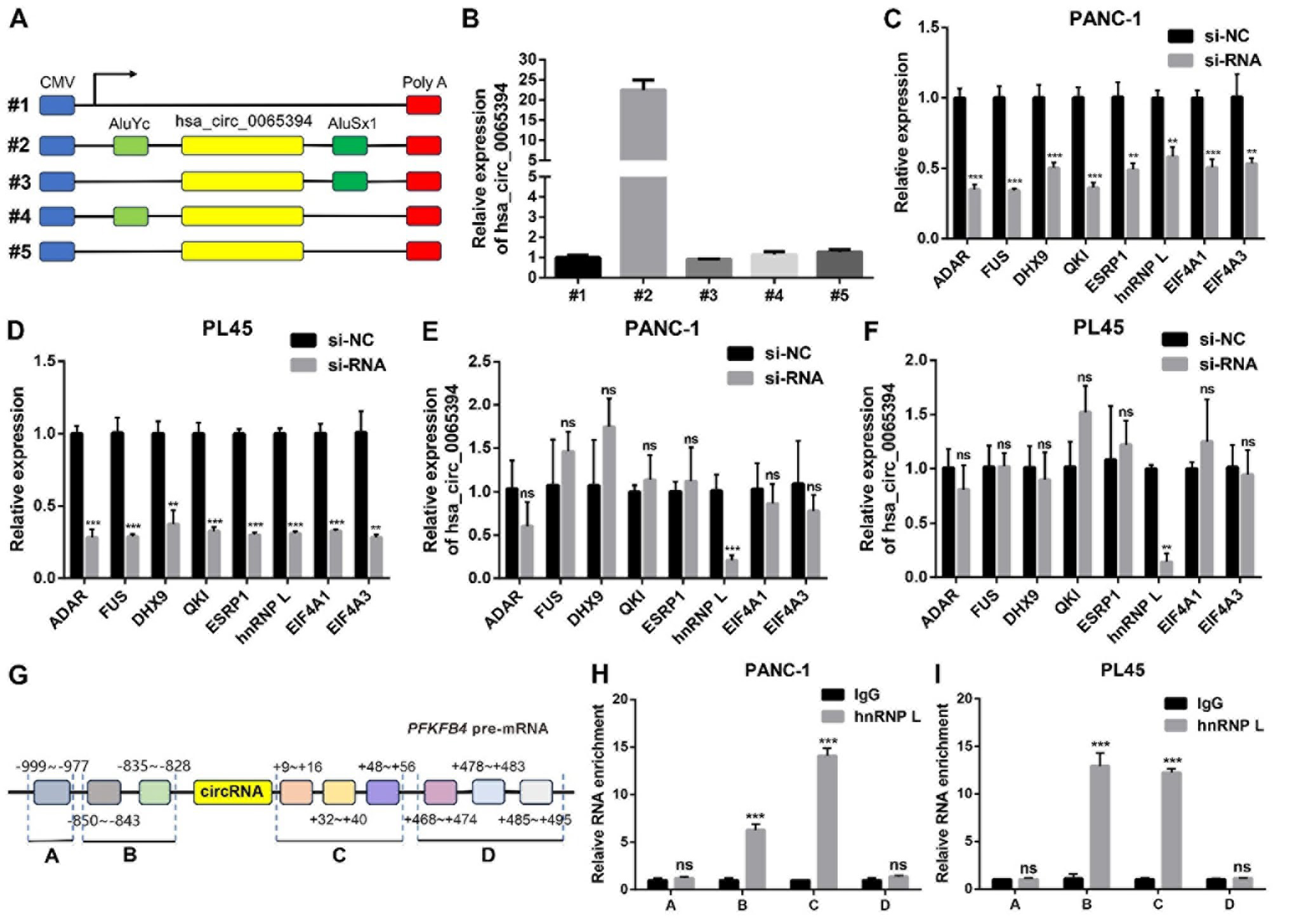
图3. hsa_circ_0065394的生物发生
hsa_circ_0065394在PC中上调
为了深入探究hsa_circ_0065394在PC中的表达模式,作者使用qRT-PCR评估了该circRNA在正常胰腺导管上皮细胞系及PC细胞系中的表达情况。结果发现,与HPDE6-C7细胞系相比,hsa_circ_0065394在绝大多数PC细胞中的表达均显著增强,尤其在PANC-1和PL45细胞中最为明显。因此,作者选择这两株细胞进行后续研究。此外,作者通过qRT-PCR检测了临床样本中PC组织及相邻组织中hsa_circ_0065394的表达情况,结果显示hsa_circ_0065394在癌组织中的表达显著高于癌旁组织。为评估hsa_circ_0065394在PC中的临床价值,作者结合患者预后信息进行了ROC(Receiver Operating Characteristic Analysis)分析,其曲线下面积(AUC)为0.677,提示hsa_circ_0065394在区分PC组织与非癌组织方面具有潜在应用价值。此外,临床样本组织芯片分析结果同样表明,hsa_circ_0065394在PC组织中表达上调。Kaplan-Meier生存分析显示,hsa_circ_0065394高表达患者的总体生存期显著短于低表达患者。相关性分析发现,hsa_circ_0065394高表达的PC患者其肿瘤体积大于低表达患者。总体而言,研究结果证实hsa_circ_0065394在PC中高表达,具有重要的临床诊断潜力,并参与PC的进展过程。
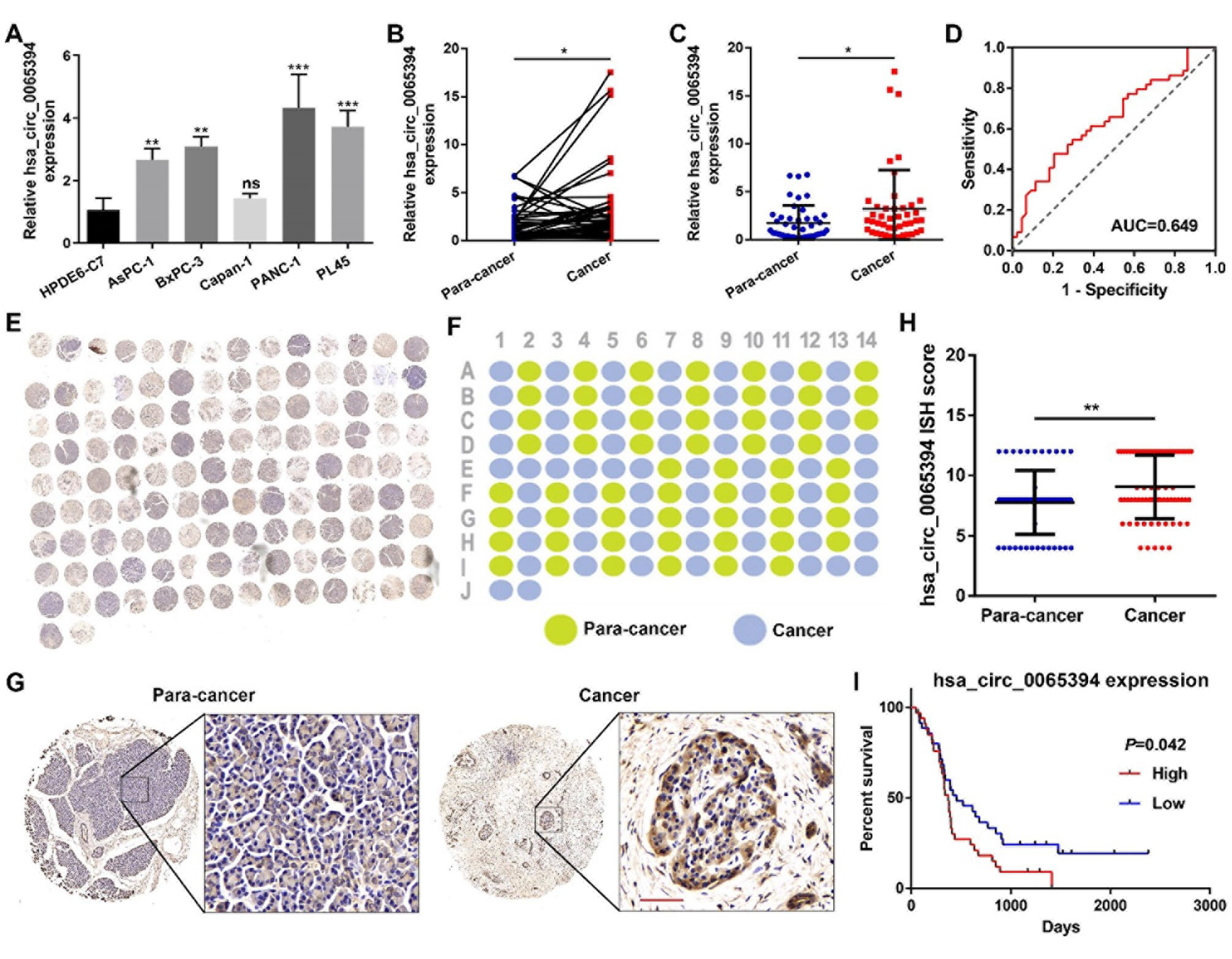
图4. hsa_circ_0065394在PC中的表达及临床特征
hsa_circ_0065394在缺氧条件下促进PC细胞的增殖、迁移和侵袭
为了阐明hsa_circ_0065394在缺氧条件下对PC细胞生物学功能的影响,作者采用三气培养箱模拟肿瘤缺氧微环境,并在此条件下进行体外功能实验。作者针对hsa_circ_0065394设计了过表达质粒(OE-circRNA)及干扰siRNA(siRNA-1和siRNA-2)。qRT-PCR结果显示,hsa_circ_0065394的过表达质粒和siRNA分别显著上调和下调PC细胞中hsa_circ_0065394的表达,且不影响其亲本基因PFKFB4的表达。CCK-8实验和平板克隆形成实验表明,hsa_circ_0065394的表达上调增强了缺氧条件下PC细胞的增殖能力,而下调则削弱了这一能力。此外,Transwell实验揭示,在缺氧条件下上调hsa_circ_0065394的表达显著提升了PC细胞的迁移和侵袭能力,而下调hsa_circ_0065394则产生相反的效果。这些结果证实了hsa_circ_0065394在缺氧条件下显著促进PC细胞的恶性进展。
为深入探究hsa_circ_0065394在体内肿瘤生长中的作用,作者将稳定过表达(LV-circRNA)或稳定敲低(LV-sh-1)hsa_circ_0065394的PC细胞系注射入裸鼠体内以构建异种移植瘤模型。与对照组比较,hsa_circ_0065394的过表达增加了肿瘤的体积、重量和生长速率,而敲低hsa_circ_0065394则产生了相反的结果。总之,这些数据表明hsa_circ_0065394在体内促进了PC细胞的生长。
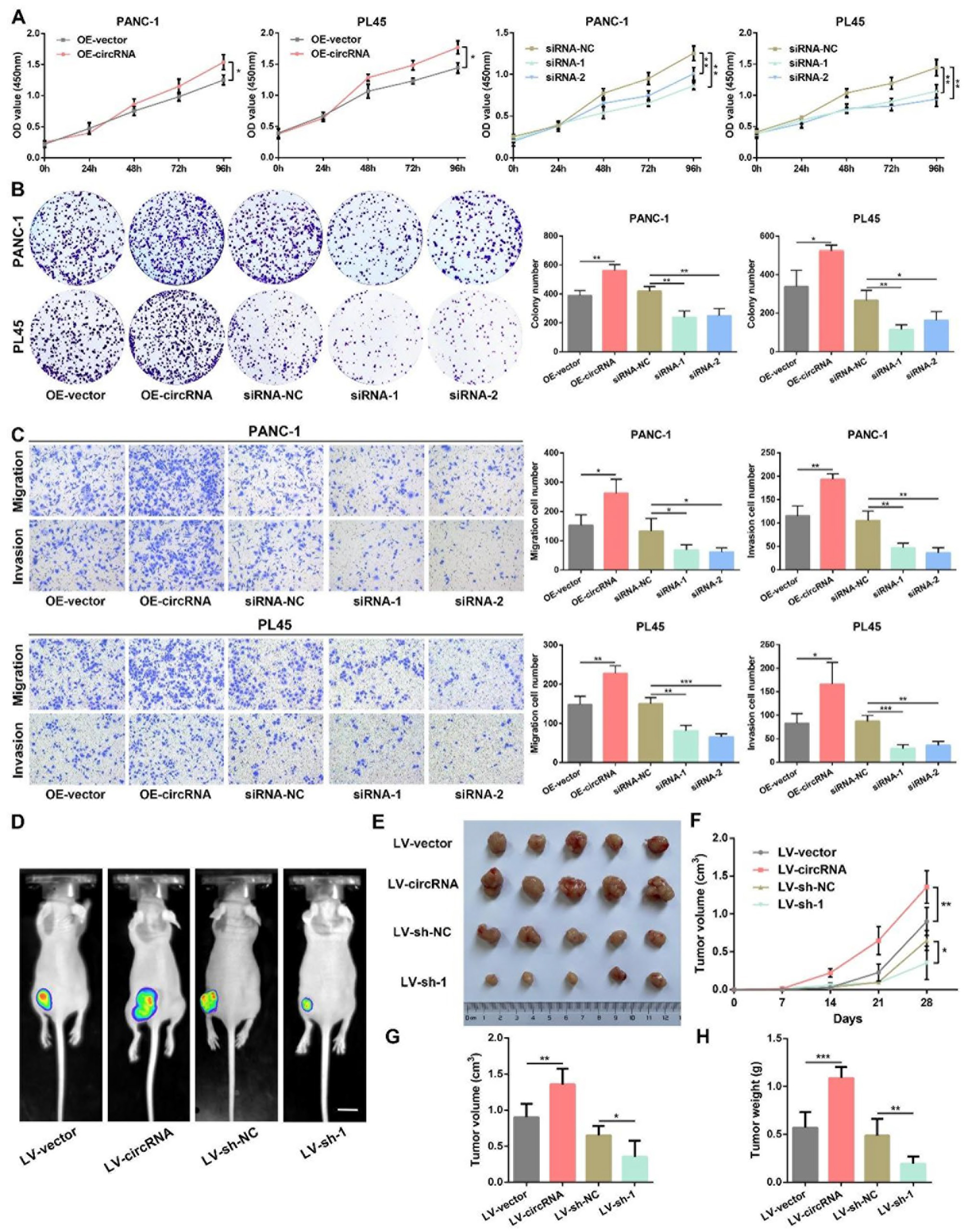
图5. hsa_circ_0065394在体内外均促进缺氧条件下PC的进展
hsa_circ_0065394编码一种新型的94个氨基酸蛋白-cPFKFB4
已有研究表明,一些具备起始密码子位点、开放阅读框(ORF)以及内部核糖体进入位点(IRES)的circRNA,可在特定条件下以不依赖帽子结构的方式翻译产生具有特殊功能的蛋白质或多肽。作者利用生物信息学工具预测了hsa_circ_0065394可能存在的ORF、IRES及其编码潜力。结果提示hsa_circ_0065394含有一个长度为285个核苷酸的ORF及一个跨越137-281个核苷酸的IRES。CPAT软件分析显示,hsa_circ_0065394具有翻译潜力。之后,作者通过同源重组克隆技术将3×FLAG标签融合插入hsa_circ_0065394的过表达载体中,构建的载体命名为F-cPFKFB4。WB结果显示:存在一个分子量约为25 kDa的带有FLAG标签的蛋白。此外,通过CO-IP结合银染技术,作者检测到了一个分子量约25 kDa处的特异性蛋白条带,与WB结果一致。进一步地,作者切取了目标凝胶区域及剩余凝胶进行LC-MS分析,发现并鉴定出F-cPFKFB4的一个特异性肽段片段(SFELLPDNEEGL)。随后,为验证hsa_circ_0065394的翻译是否由IRES介导的核糖体进入所启动,作者设计并构建了包含全长IRES序列或截短突变IRES序列的双荧光素酶报告载体。双荧光素酶报告基因检测结果显示,预测的IRES序列显示出显著的活性,而截短的IRES序列则无活性。之后,作者设计并构建了携带全长或截短IRES序列的翻译载体。WB结果验证了双荧光素酶报告基因实验的结果:仅包含完整IRES序列的载体能够翻译产生cPFKFB4,表明IRES序列必须保持完整才能驱动hsa_circ_0065394的翻译。综上所述,研究表明hsa_circ_0065394以IRES依赖的方式翻译产生一种新型的约25 kDa的蛋白(命名为:cPFKFB4)。
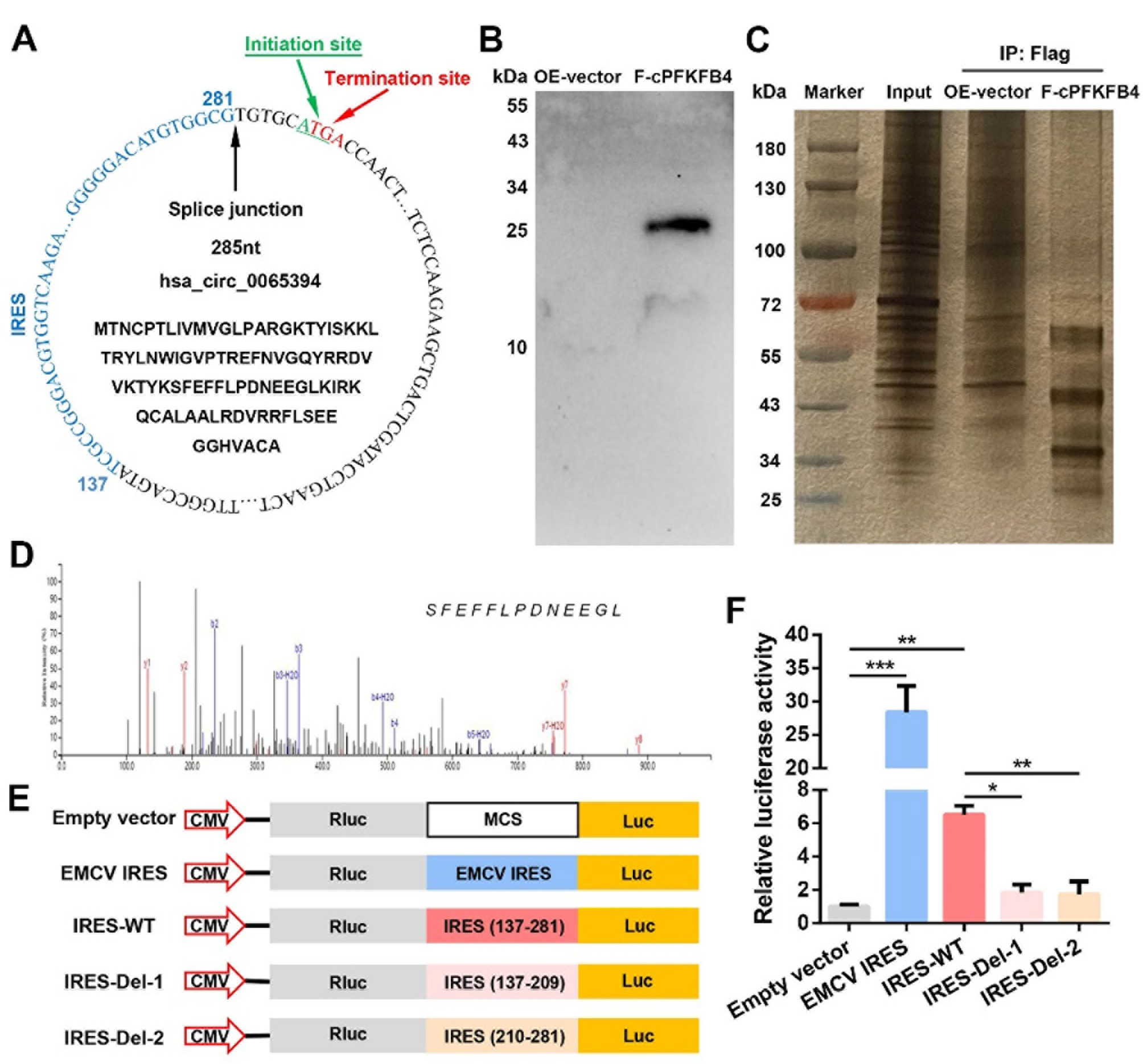
图6. hsa_circ_0065394 编码一种新型蛋白质,即cPFKFB4
cPFKFB4 在低氧条件下促进 PC细胞的增殖、迁移和侵袭
为了进一步探究cPFKFB4的生物学功能,作者将空载质粒、hsa_circ_0065394过表达质粒(OE-circRNA)或F-cPFKFB4质粒转染至PC细胞系中。CCK-8实验、克隆形成实验及Transwell实验的结果共同表明,hsa_circ_0065394及其编码的蛋白cPFKFB4均能在缺氧条件下促进PC细胞的增殖、迁移和侵袭。为了验证hsa_circ_0065394的生物学功能是否依赖于其编码蛋白cPFKFB4,作者在PC细胞中敲低hsa_circ_0065394的同时上调cPFKFB4的表达水平。体外功能实验结果显示,cPFKFB4能够恢复因敲低hsa_circ_0065394对细胞增殖、迁移以及侵袭所产生的抑制作用。这些研究结果表明,cPFKFB4能够独立影响PC细胞的恶性表型。更重要的是,hsa_circ_0065394对PC细胞生物学功能的调控作用依赖于其编码蛋白cPFKFB4。
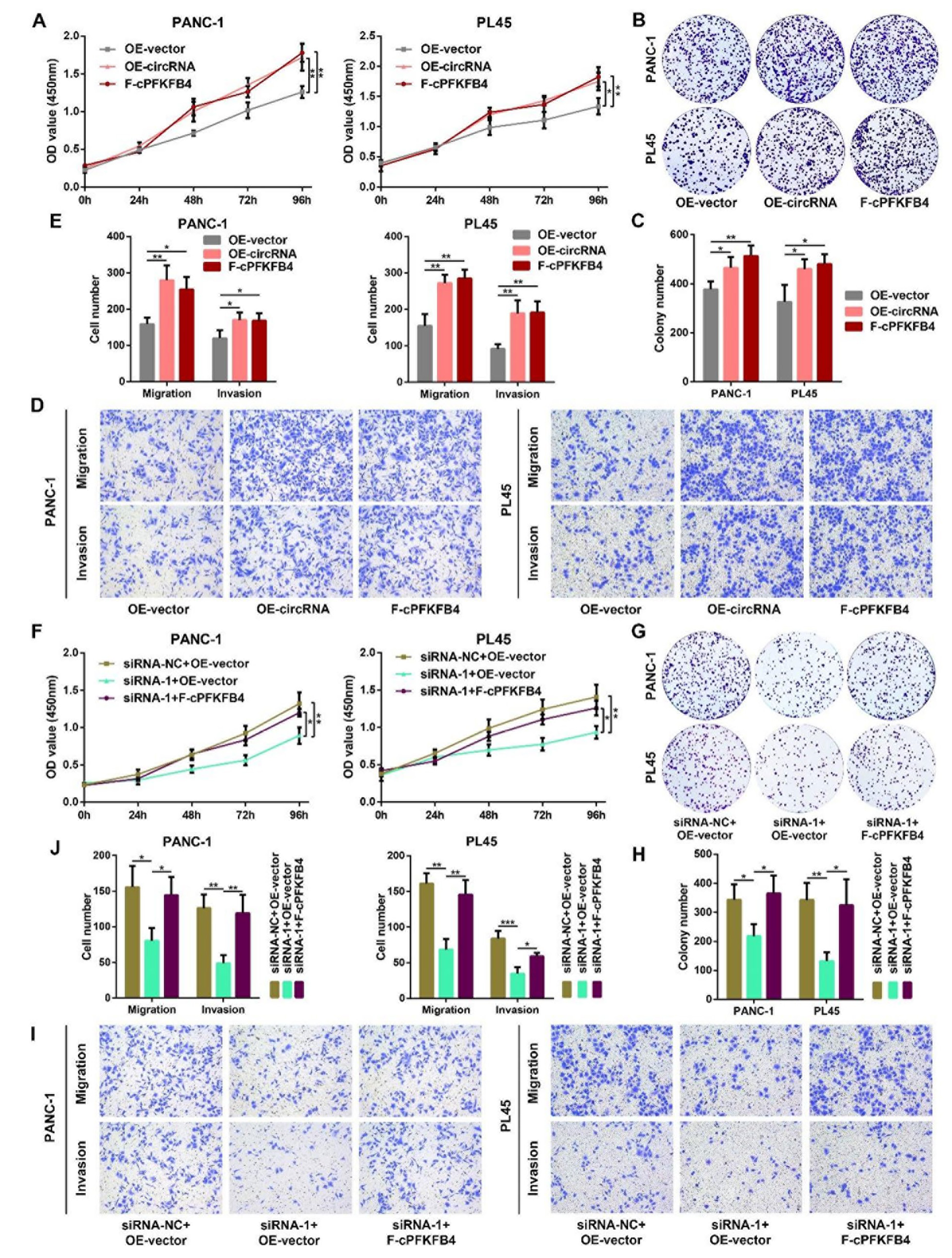
图7. cPFKFB4 在PC中的生物学功能
cPFKFB4特异性结合hnRNP G
为进一步阐明cPFKFB4在缺氧条件下促进PC细胞恶性进展的分子机制,作者进行了CO-IP和LC-MS实验,结果显示cPFKFB4可能与hnRNP G发生相互作用。之后,作者在转染F-cPFKFB4的PC细胞系中进一步进行CO-IP实验,证实FLAG抗体能显著富集cPFKFB4与hnRNP G。免疫荧光染色显示,在缺氧的PC细胞中,hnRNP G与cPFKFB4存在共定位现象。为进一步确定hnRNP G与cPFKFB4结合的特定位点,作者基于hnRNP G的已知结构域,设计并构建了5种带有HA标签的截短突变体质粒(HA-hnRNP G、HA-Mut 1、HA-Mut 2、HA-Mut 3、HA-Mut 4及HA-Mut 5)。CO-IP实验表明,cPFKFB4能与HA-Mut4和HA-mut5质粒结合,即cPFKFB4与hnRNP G的丝氨酸-精氨酸-甘氨酸-酪氨酸结构域(SRGY)与C端RNA结合结构域(C-RBD)结合。综上所述,cPFKFB4特异性结合hnRNP G的SRGY与C-RBD结构域。
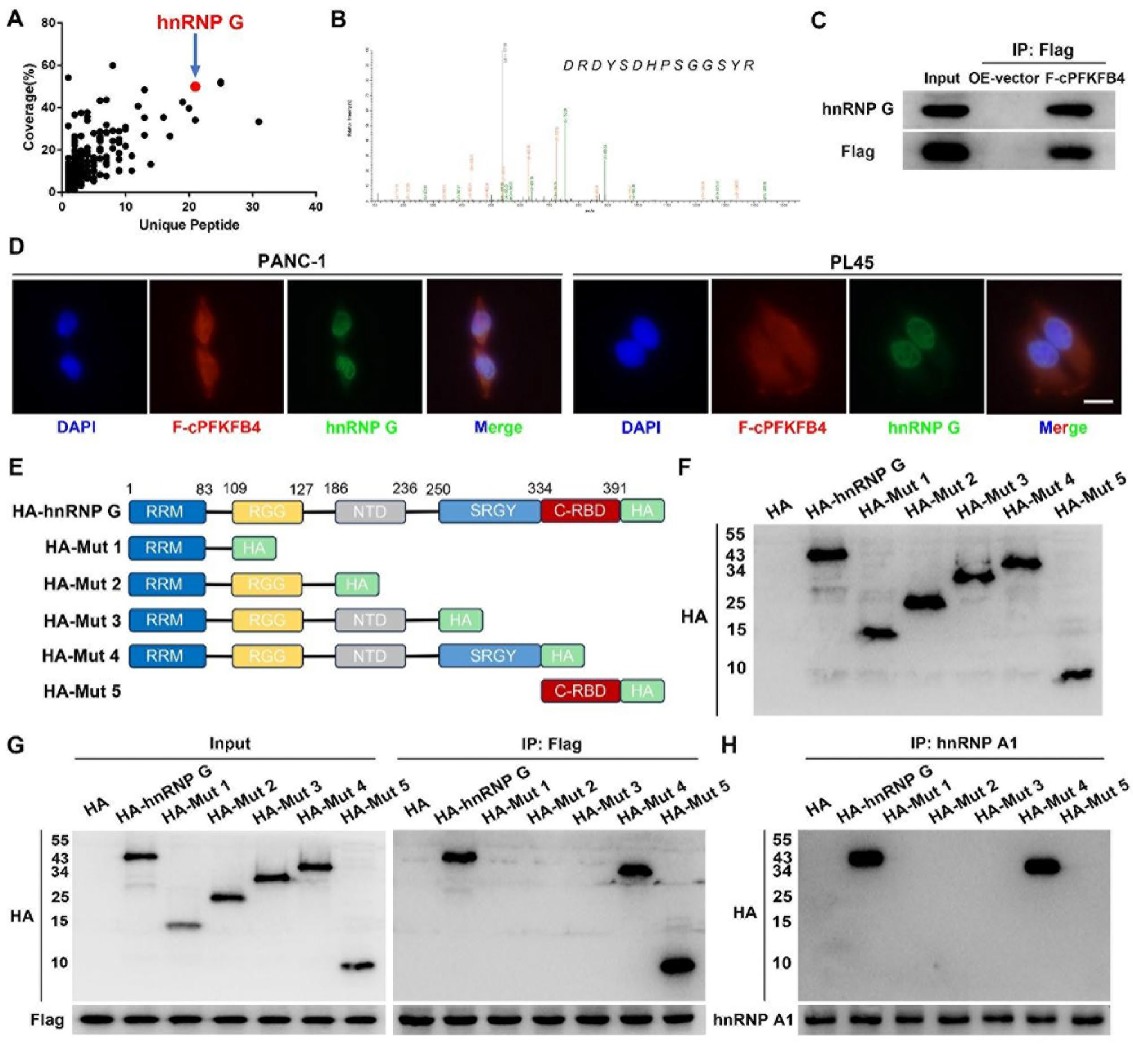
图8. 在缺氧条件下,cPFKFB4与hnRNP G相互作用
cPFKFB4抑制hnRNP G/hnRNP A1相互作用以调控PKM可变剪接
已有研究报道,hnRNP G与hnRNP A1之间的相互作用调控PKM的可变剪接,进而调节癌细胞的葡萄糖代谢。因此,作者在PC细胞中分别上调和下调cPFKFB4表达后进行CO-IP实验,以验证cPFKFB4对hnRNP G与hnRNP A1结合的影响。结果表明,过表达cPFKFB4削弱了hnRNP G与hnRNP A1之间的结合,而下调cPFKFB4则增强了二者之间的结合。随后的RIP实验显示,上调cPFKFB4增强了hnRNP A1与PKM前体mRNA的结合,而下调cPFKFB4则产生相反效应。qRT-PCR结果表明,cPFKFB4表达水平的变化并不影响PKM的转录水平。PKM可变剪接实验和WB结果证实,上调cPFKFB4增加了PKM2亚型并减少了PKM1亚型,而下调cPFKFB4则对PKM可变剪接产生了相反影响。接下来,作者在cPFKFB4与hnRNP G之间进行了回复实验。特别值得注意的是,PKM可变剪接实验表明,过表达hnRNP G能够逆转cPFKFB4对PKM2/1转录本比例的上调作用,而敲低hnRNP G则挽救了cPFKFB4敲低对PKM2/1转录本比例的下调效应。WB分析结果与上述实验发现一致。这些结果证实,cPFKFB4通过竞争性结合hnRNP G,破坏其与hnRNP A1的相互作用,从而促进PKM2的剪接和表达。
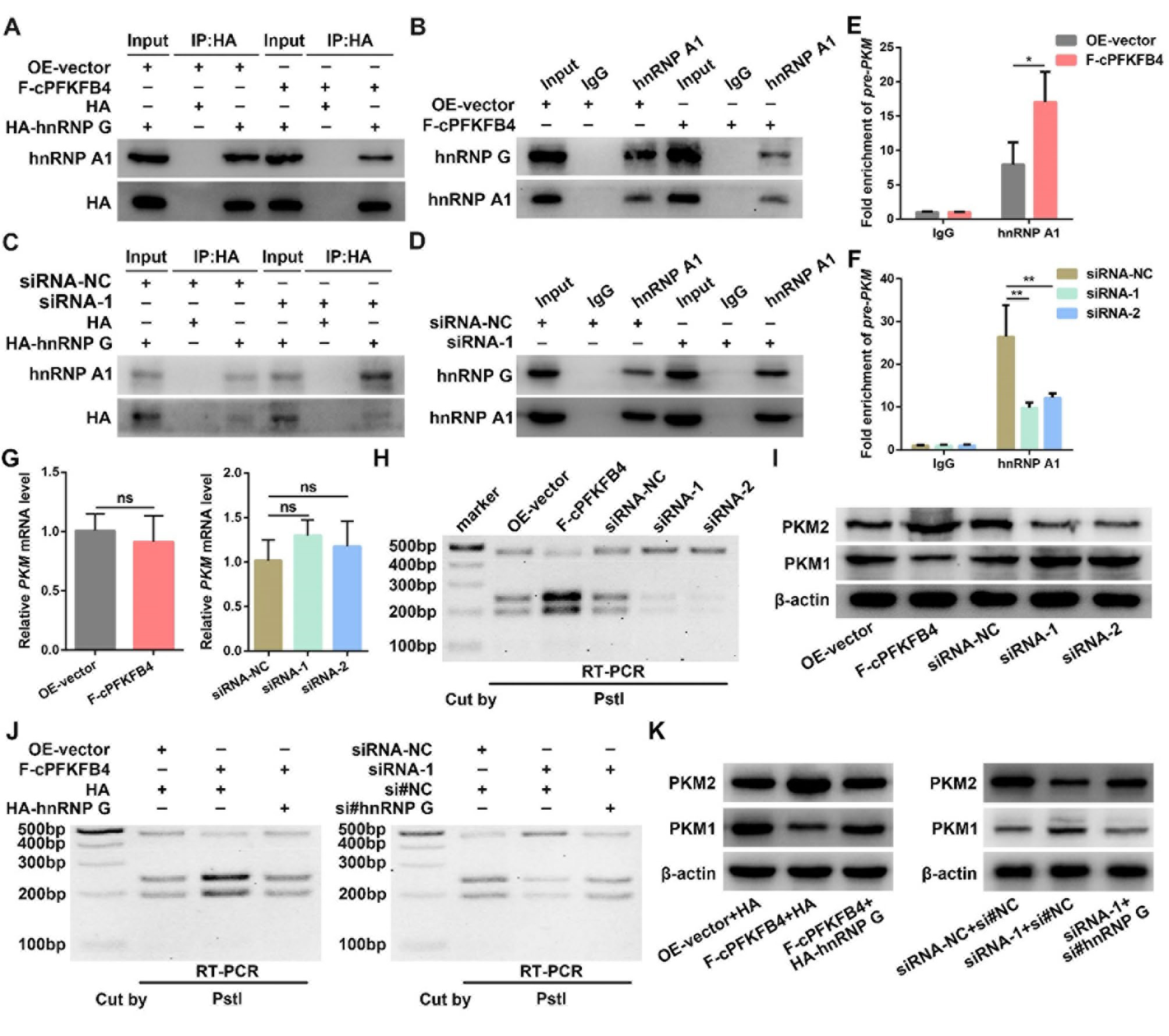
图9. cPFKFB4与hnRNP G/hnRNP A1 结合,以调节 PKM 的可变剪接过程
cPFKFB4在缺氧条件下通过hnRNP G增强PC细胞的糖酵解
PKM2在葡萄糖代谢重塑中发挥着至关重要的作用。因此,作者研究了cPFKFB4对PC细胞糖酵解代谢的影响。乳酸生成实验表明,在缺氧条件下,上调cPFKFB4显著增强了PC细胞的乳酸生成,而下调cPFKFB4则明显减少了乳酸生成。此外,在葡萄糖摄取和ATP生成实验中也观察到了类似的结果。这些糖酵解相关实验证明,cPFKFB4在缺氧条件下显著提升了PC细胞的糖酵解水平。
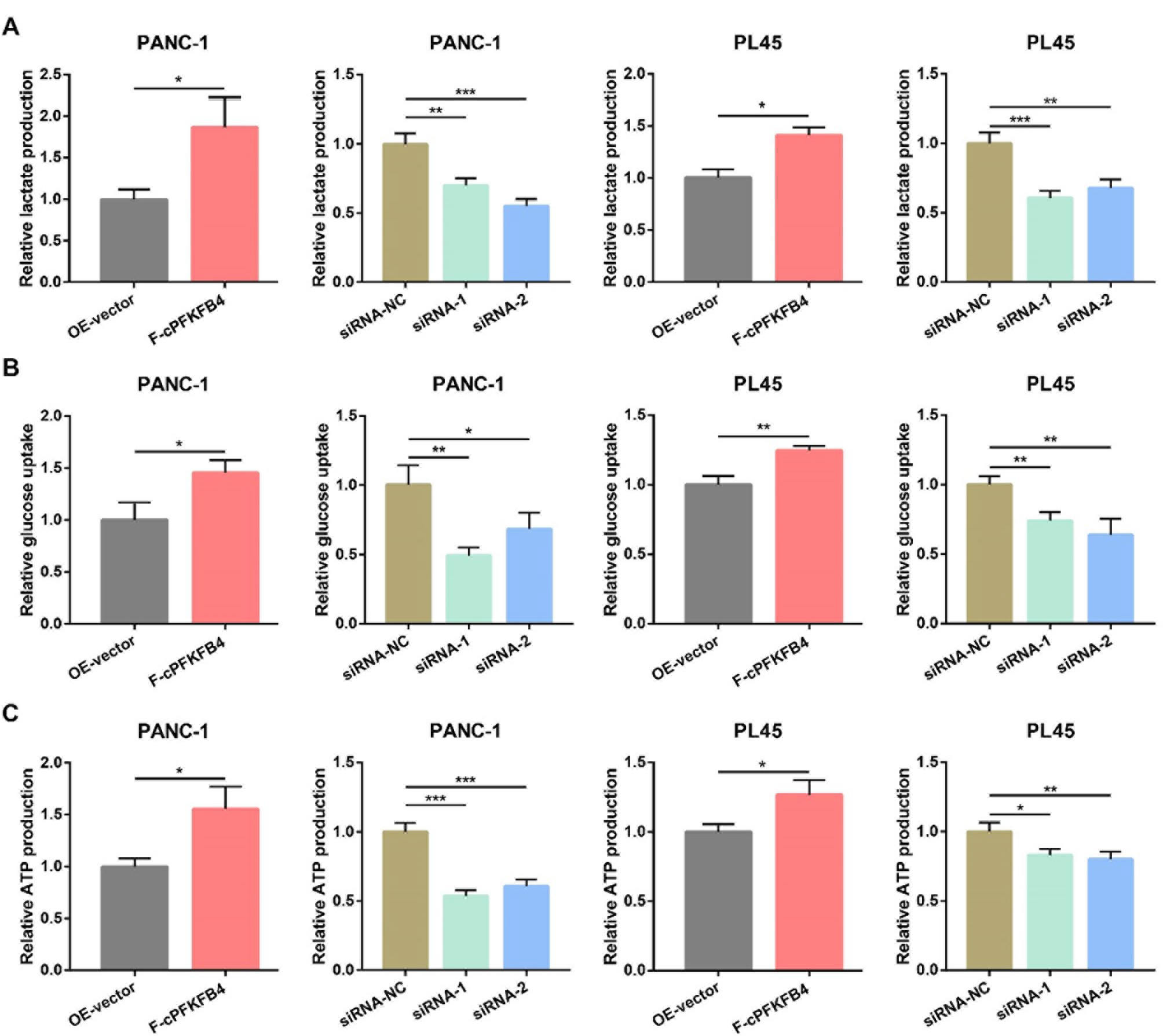
图10. cPFKFB4在缺氧条件下增强PC细胞的糖酵解
随后,作者通过回复实验来确定cPFKFB4是否通过hnRNP G影响PC细胞的糖酵解代谢。乳酸生成、葡萄糖摄取和ATP生成实验共同表明,cPFKFB4过表达对PC细胞乳酸生成、葡萄糖摄取和ATP生成的促进作用,而上调hnRNP G可逆转由cPFKFB4过表达引起的变化。此外,cPFKFB4敲低对PC细胞乳酸生成、葡萄糖摄取和ATP生成的抑制作用,可通过下调hnRNP G得到恢复。上述研究结果证实,cPFKFB4在缺氧条件下通过hnRNP G增强了PC细胞的糖酵解水平。
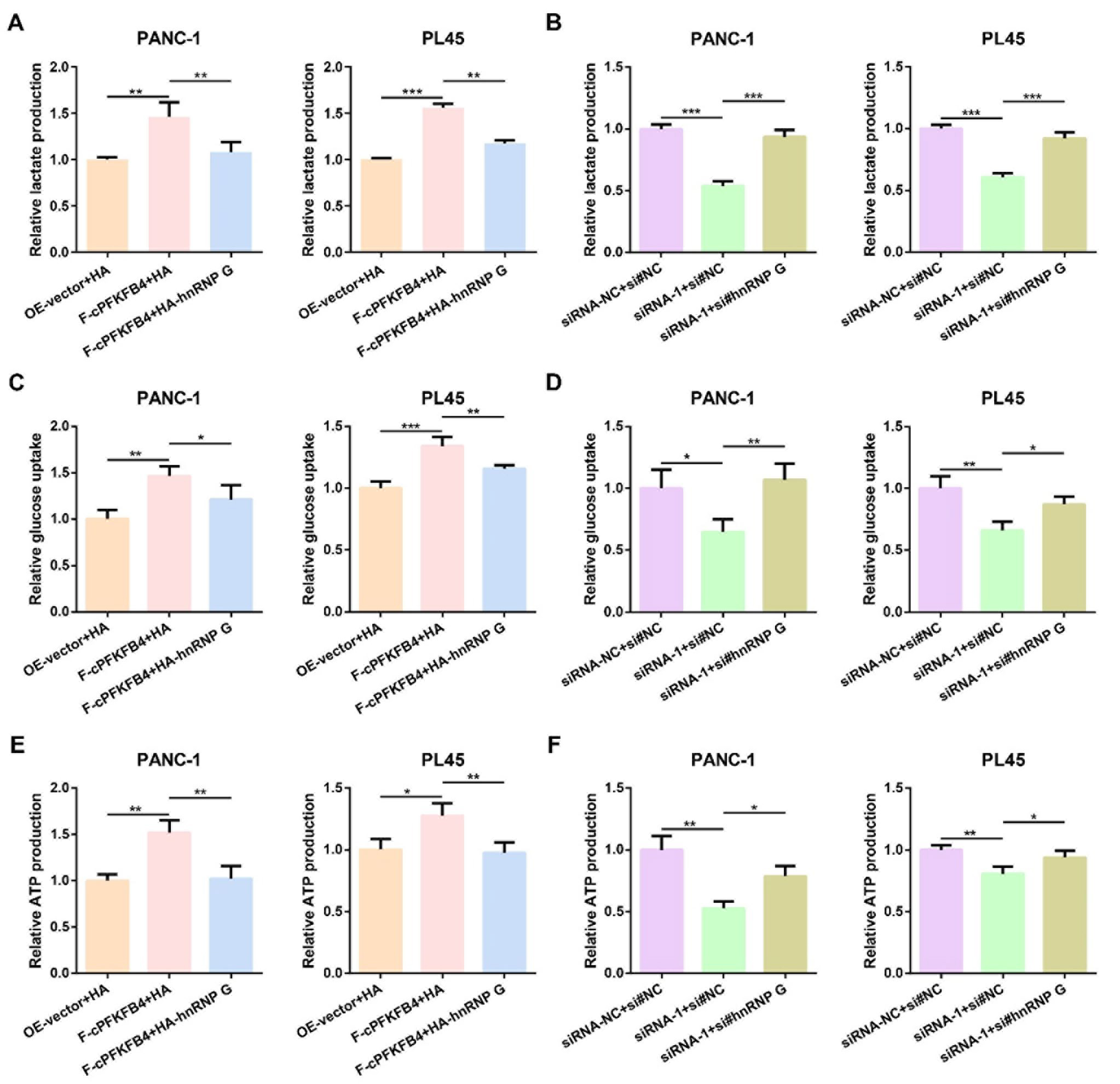
图11. cPFKFB4通过hnRNP G调控PC细胞的糖酵解
cPFKFB4在缺氧条件下通过PKM2增强PC细胞的恶性表型
葡萄糖代谢重编程是调控恶性肿瘤生长和侵袭的重要因素。因此,作者推测cPFKFB4可能通过影响PKM2介导的糖酵解来促进PC细胞的恶性表型。基于此,作者在cPFKFB4与PKM2之间开展了回复实验。体外细胞增殖实验表明,PKM2的敲低消除了cPFKFB4在缺氧条件下对细胞增殖的促进作用;相反,上调PKM2的表达则抵消了cPFKFB4敲低对细胞增殖的抑制作用。同样,在Transwell迁移和侵袭实验中,PKM2敲低阻断了cPFKFB4过表达诱导的PC细胞迁移和侵袭能力变化;反之,PKM2过表达则逆转了cPFKFB4敲低所产生的影响。综上,这些研究结果表明cPFKFB4的致癌效应依赖于糖酵解代谢的关键调控因子PKM2。
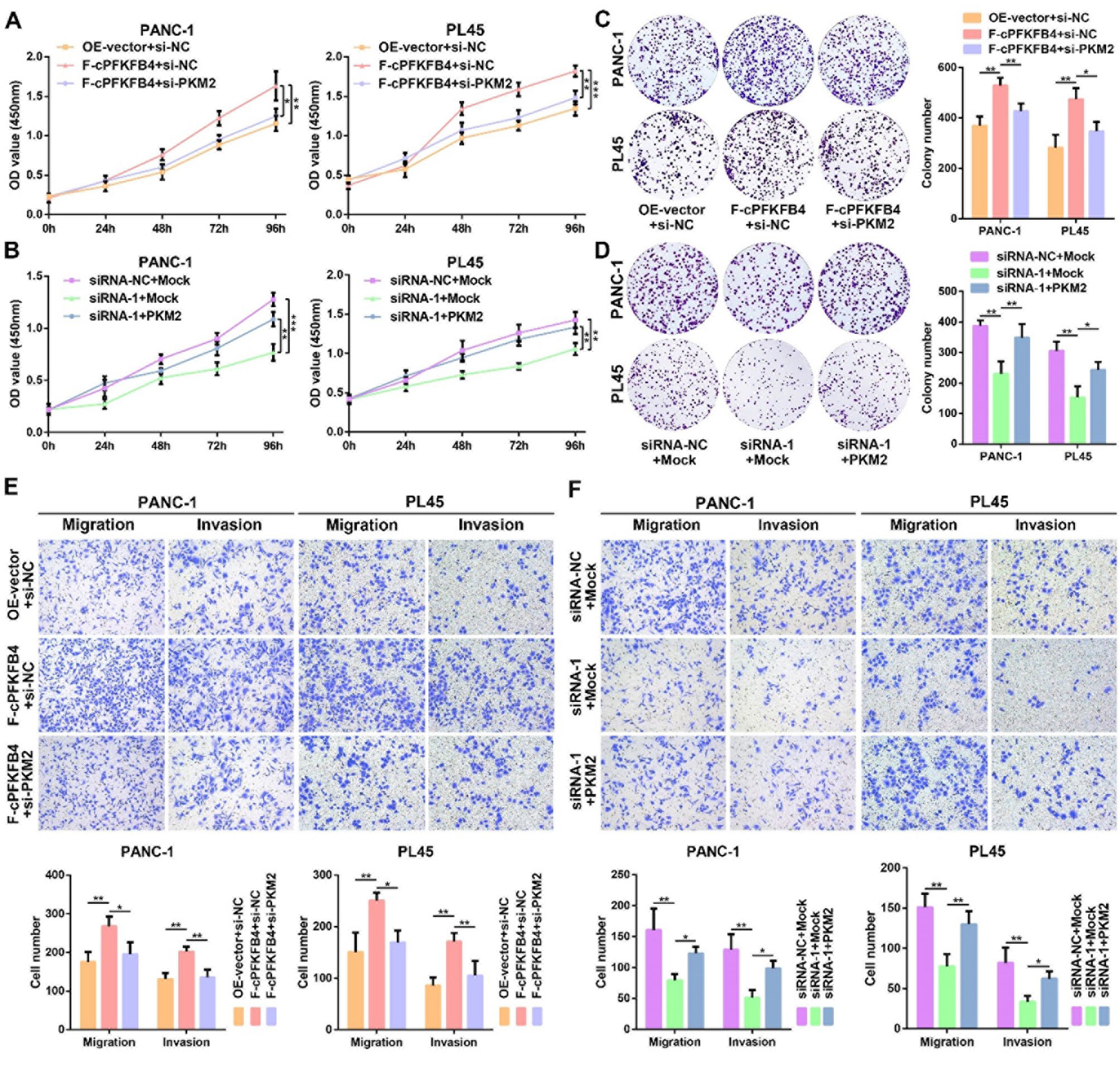
图12. cPFKFB4在缺氧条件下增强PKM2诱导的PC细胞侵袭性表型
cPFKFB4通过PKM2促进PC细胞在体内的生长
为了进一步明确cPFKFB4如何通过PKM2影响PC细胞的增殖,作者开展了动物实验。结果显示,cPFKFB4过表达对PC细胞体内生长的促进作用可被PKM2敲低所逆转。此外,cPFKFB4敲低对PC细胞体内生长的抑制作用可通过PKM2的过表达得以消除。同时,免疫组化结果显示,在肿瘤组织中,上调或下调cPFKFB4表达对Ki67和PKM2表达水平的影响,可分别通过下调或上调PKM2而逆转。总而言之,这些数据与体外实验结果一致,表明cPFKFB4以PKM2依赖的方式促进PC细胞在体内的生长。
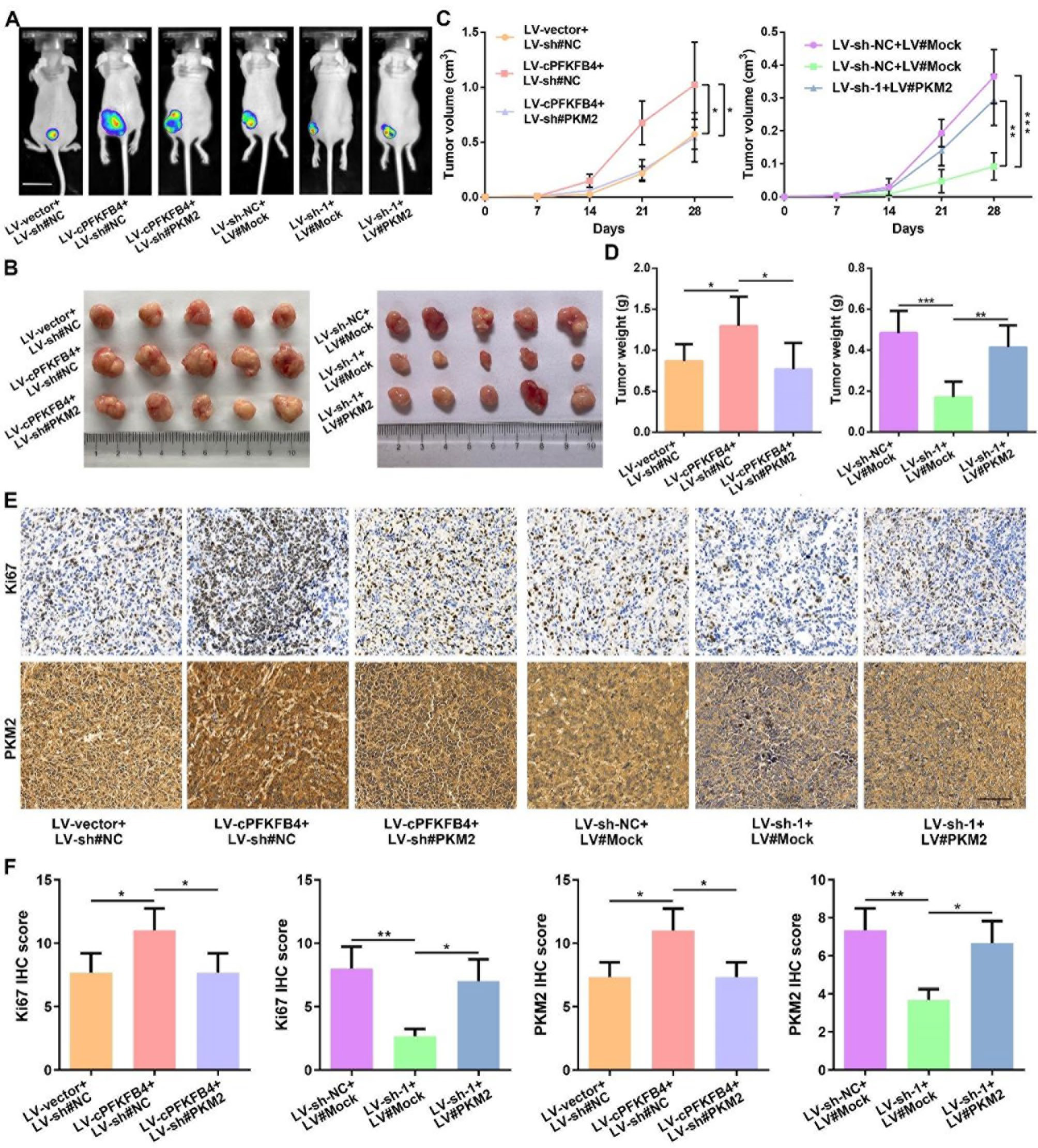
图13. cPFKFB4通过PKM2在体内促进PC生长
总结
综上所述,本研究发现了一种在PC中由缺氧诱导产生的circRNA:hsa_circ_0065394,其生物合成由Alu序列和hnRNP L介导。此外,hsa_circ_0065394通过不依赖于帽子结构的机制编码了cPFKFB4蛋白。在缺氧条件下,cPFKFB4通过通过竞争性结合hnRNP G,破坏其与hnRNP A1的相互作用,增强了hnRNP A1介导的PKM可变剪接,从而提升PKM2的表达水平,增强了PC细胞的糖酵解能力,并最终促进了PC的恶性进展。本文的研究结果为揭示缺氧、葡萄糖代谢重编程与PC之间的相互作用机制提供了创新性见解,并为开发PC的潜在生物标志物和治疗靶点开辟了新途径。

查看更多

查看更多

查看更多

联系我们

返回顶部