查看更多

 明星产品
明星产品
 关注我们
关注我们

扫码关注我们
了解更多信息
肥胖是一种以体内脂肪过度堆积或脂肪组织分布异常为特征的慢性代谢性疾病,它已成为全球首要的公共卫生问题之一,同时也是多种慢性疾病的共同病理基础因素。脂肪组织慢性炎症是一种源于脂肪组织、以脂肪过度堆积为特征的持续性的低度的全身炎症状态,可逐步累及肝脏、骨骼肌、胰岛、中枢神经系统等多个器官,在肥胖相关代谢并发症的发病机制中发挥关键作用,在这一病理过程中,脂肪细胞与脂肪组织内驻留免疫细胞的异常相互作用起着至关重要的调节作用,然而,这种异常相互作用的潜在调控机制仍然知之甚少。接下来介绍的这篇文章发现了在肥胖状态下,脂肪细胞以β2-微球蛋白(β2 microglobulin,B2M)调控肥胖相关的慢性炎症,为肥胖相关疾病的治疗提供了新靶点,我们一起来看看吧。

2025年12月3日,陆军军医大学吴玉章院士团队在Signal Transduction and Targeted Therapy(IF=52.7)发表题为“Adipocytes orchestrate obesity-related chronic inflammation through β2-microglobulin”的研究论文,该研究通过构建高脂饮食诱导的肥胖小鼠模型和脂肪特异性B2M敲除小鼠,结合转录组测序发现肥胖小鼠脂肪细胞中B2M显著上调,利用流式细胞术分析免疫细胞浸润,发现B2M缺失可减少CD8+T细胞活化和巨噬细胞M1极化。随后,通过免疫共沉淀和铁代谢检测等实验,揭示B2M通过HFE/TFR2复合物上调铁调素、抑制铁转运蛋白,导致脂肪细胞铁过载并最终诱发铁死亡。此外,通过原代脂肪细胞与CD8+T细胞的共培养实验,验证了B2M在细胞接触依赖下激活免疫反应的作用。最终得出结论:肥大脂肪细胞通过B2M依赖的双重通路:MHC I类抗原呈递激活CD8+T细胞,以及铁代谢紊乱诱导自身铁死亡并促进巨噬细胞M1极化,共同驱动肥胖相关的慢性炎症和代谢紊乱,而靶向敲低B2M可缓解这些表型,提示其具有潜在的治疗价值。
在此研究中,作者使用的脂肪特异性敲低B2M的腺相关病毒(AAV9-Fabp4-ZsGreen-miR30-shB2m)来自汉恒生物。
下面我们一起来具体了解下这篇文章吧。
B2M在肥大脂肪细胞中上
首先,作者通过对正常饮食(NCD)和高脂饮食(HFD)小鼠附睾脂肪组织(EpiWAT)中的脂肪细胞进行转录组分析,发现HFD组脂肪细胞中抗原加工与呈递通路、铁摄取与转运通路显著上调,B2M是这两条通路的关键交集因子。另外,体内外实验验证结论显示,在肥胖状态下,B2M表达特异性上调,提示B2M可能通过这两条通路调控脂肪细胞的免疫激活和铁稳态。
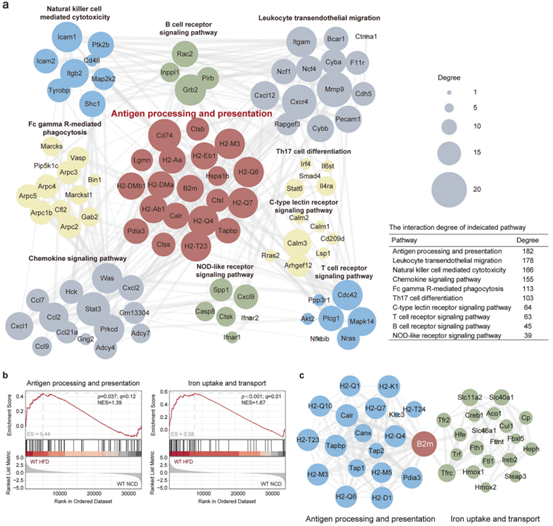
图1. B2M在肥大脂肪细胞中上调
脂肪细胞特异性B2M缺失保护小鼠免受肥胖及相关炎症和代谢紊乱的影响
为了评估脂肪细胞中B2M在HFD诱导的肥胖中的作用,作者构建了脂肪细胞特异性B2M敲除小鼠(B2mcKO)与对照小鼠(B2mf/f),两组小鼠均为HFD喂养。结果发现,与B2mf/f小鼠相比,B2mcKO小鼠的体重增长,而EpiWAT重量及占比、皮下脂肪和棕色脂肪组织的脂质沉积水平及脂肪细胞体积均显著较低,肝脏脂滴显著较少,且B2M敲除能缓解HFD诱导的肝损伤和糖脂代谢紊乱。另外,血清炎症因子检测显示,B2mcKO小鼠的系统性低度炎症得到抑制。总之,综上结果表明脂肪细胞中的B2M 在引发肥胖及相关炎症和代谢紊乱中起着关键作用。
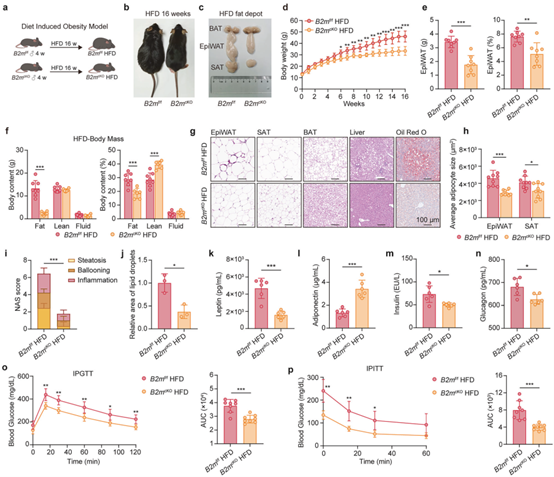
图2. 脂肪细胞特异性B2M敲除保护小鼠免受肥胖及相关炎症和代谢紊乱的影响
脂肪细胞特异性B2M敲除可以缓解HFD诱导的炎症反应
随后,作者使用流式细胞术分析以评估HFD喂养的B2mf/f和B2mcKO小鼠EpiWAT中驻留免疫细胞的数量,发现B2mcKO小鼠的CD45+免疫细胞数量显著低于B2mf/f小鼠,而且B2mcKO小鼠中M1/M2比值和CD8+ T细胞/CD8- T细胞比值显著低于B2mf/f小鼠。另外,作者发现HFD喂养的B2mcKO小鼠脂肪组织中产生炎症细胞因子的细胞数量也远低于B2mf/f小鼠。这些发现表明,脂肪细胞特异性B2M敲除可以缓解HFD饮食诱导的炎症反应,特别是通过抑制CD8⁺T细胞的激活以及免疫细胞向M1的极化,从而改善代谢功能障碍。
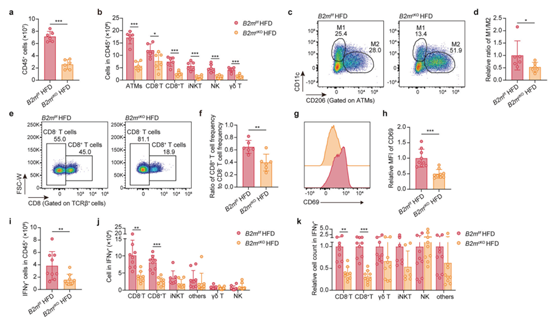
图3. 脂肪细胞特异性B2M敲除可以缓解HFD诱导的炎症反应
脂肪细胞激活CD8+T细胞依赖于B2M和直接细胞接触
接下来,作者通过基因富集分析发现,HFD喂养的B2mf/f小鼠脂肪细胞中,抗原加工与呈递通路显著上调,而B2mcKO小鼠中该通路的上调被抑制,提示B2M是该通路激活的关键分子。然后,作者检测了不同喂养条件下B2mf/f和B2mcKO小鼠EpiWAT来源的脂肪细胞中MHC-I分子的表达,发现HFD喂养使B2mf/f小鼠脂肪细胞中的MHC-I的mRNA和蛋白表达上调,并增强了MHC-I在细胞膜上的定位,B2mcKO小鼠则完全阻断了这一上调,说明B2M调控MHC-I的表达及膜定位。为了确定脂肪细胞是否以B2M依赖的方式激活CD8+ T细胞,作者从B2mf/f和B2mcKO小鼠EpiWAT分离脂肪细胞并使之分化成熟,用棕榈酸(Palmitic Acid, PA)处理诱导脂肪细胞肥大,然后将其与CD8⁺T细胞共培养,检测CD8⁺T细胞的增殖与活化。结果发现,CD8+T细胞仅在与PA预处理的B2mf/f小鼠的脂肪细胞直接接触时表现出显著的增殖和激活,而未用PA预处理、B2M敲除的脂肪细胞或分离在Transwell小室中的脂肪细胞均无法诱导CD8+T细胞的增殖和活化。这些数据表明,在肥胖期间,脂肪细胞以B2M和细胞接触依赖的方式激活CD8+T细胞。
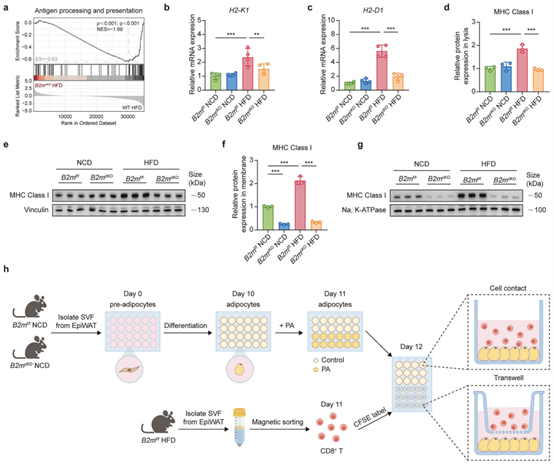
图4. 脂肪细胞激活CD8+T细胞依赖于B2M和直接细胞接触
敲除B2M可防止HFD诱导的脂肪细胞铁过载
B2M通过与遗传性血色病蛋白(Hemochromatosis protein, HFE)和转铁蛋白受体(Transferrin receptor, TFR)的相互作用参与铁摄取和转运通路,并且该通路在HFD刺激下的脂肪细胞中显著上调。值得注意的是,HFD喂养的B2mf/f和B2mcKO小鼠的脂肪细胞中的差异表达基因也富集在与铁离子稳态相关的通路中。为了阐明B2M在肥胖脂肪细胞铁稳态中的作用,作者检测了NCD和HFD饮食状态下B2mf/f和B2mcKO小鼠脂肪细胞中的铁储存相关分子以及细胞内总铁含量。结果发现HFD喂养后,B2mf/f小鼠脂肪细胞中铁储存相关分子的表达以及总铁含量显著升高,而HFD喂养的B2mcKO小鼠没有这种现象,而且脂肪细胞的总铁含量与EpiWAT占比呈正相关。这些结果表明,B2M敲除能抑制HFD诱导的脂肪细胞的铁积累。鉴于HFE需要与B2M二聚化以实现稳定的膜定位,然后通过与TFR1或TFR2切换相互作用来调节铁摄取或通过铁调素-铁转运蛋白(Ferroportin, FPN)调节铁流出,从而有助于肝脏和全身铁稳态。作者推测HFE/B2M-TFR1/2-铁调素-FPN轴可能参与脂肪细胞铁稳态的调节。免疫共沉淀实验证明,NCD组的B2mf/f小鼠的脂肪细胞膜上HFE主要与TFR1 结合,介导铁摄取平衡,而HFD组的B2mf/f小鼠的脂肪细胞HFE更倾向于与TFR2结合(HFE从与TFR1结合转移到与TFR2结合会诱导铁调素表达,而铁调素通过负向调节FPN来阻碍铁流出)。但两种饮食条件下,敲除B2M使得HFE与TFR1和TFR2的结合均被破坏,说明B2M是HFE与TFR家族结合的必需分子。另外,HFD喂养使B2mf/f小鼠脂肪细胞中HFE、TFR2、铁调素的mRNA 和蛋白表达升高,TFR1膜定位和FPN的表达及膜定位均减少,而敲除B2M则阻断了这些变化。总之,这些数据表明,B2M缺失可防止高脂饮食诱导的脂肪细胞铁过载,是脂肪细胞铁稳态的关键调控因子。
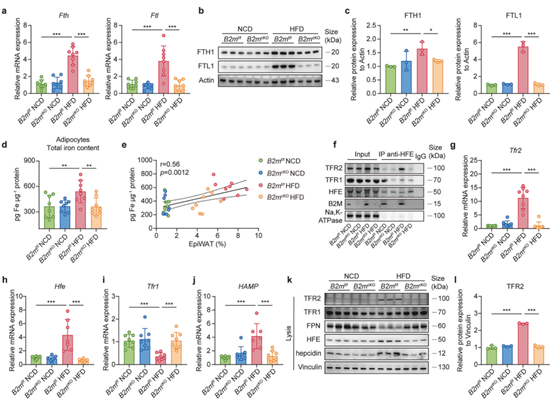
图5. 敲除B2M可防止HFD诱导的脂肪细胞铁过载
B2M缺乏可减轻HFD诱导的脂肪细胞铁死亡和M1极化
由于细胞内的铁过载可能最终会诱导铁死亡,接下来作者做了一系列体外和体内实验来探究铁死亡是否发生在肥大脂肪细胞中以及敲除B2M是否能抑制铁死亡。体外实验中,作者用PA处理B2mf/f和B2mcKO小鼠来源的脂肪细胞,发现PA处理显著上调了B2mf/f小鼠脂肪细胞的铁死亡标志物的表达并诱导了细胞死亡,而B2M敲除则显著减弱了这些效应。体内实验中,HFD喂养的B2mf/f小鼠脂肪细胞的游离亚铁离子含量、ROS水平、脂质过氧化物产物显著升高,GSH水平降低,而B2mcKO小鼠完全逆转了这些变化。透射电镜结果显示,HFD组B2mf/f小鼠脂肪细胞中线粒体萎缩、膜密度增加(铁死亡典型形态),而B2mcKO小鼠脂肪细胞中线粒体形态则是正常的。随后,作者为了证实铁死亡的脂肪细胞会促进脂肪巨噬细胞(Adipose tissue macrophages, ATMs)向M1极化,将PA处理的B2mf/f小鼠脂肪细胞和ATMs共培养,发现ATMs的M1标志物表达显著升高,加入Fer-1(抑制铁死亡)或使用B2mcKO小鼠脂肪细胞,均能完全阻断ATMs的M1极化。综上结果表明,B2M缺乏可减轻HFD诱导的脂肪细胞铁死亡和向M1极化。
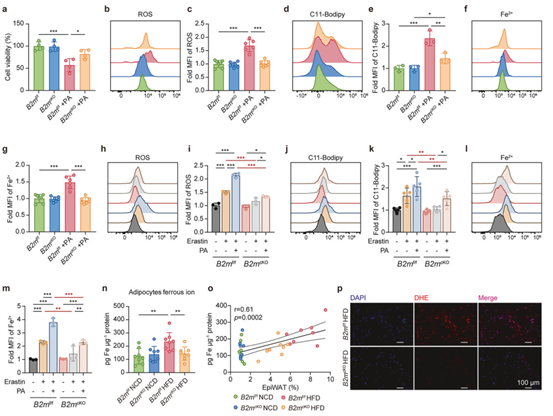
图6. B2M缺乏可减轻HFD诱导的脂肪细胞铁死亡和M1极化
EpiWAT中特异性敲低B2M可缓解肥胖及代谢紊乱
为了进一步研究在肥胖期间特异性干预脂肪组织中B2M表达的治疗潜力,作者使用AAV9-Fabp4-ZsGreen-miR30-shB2m(AAV9-B2m)特异性敲低小鼠EpiWAT中B2M的表达水平。结果显示,AAV9-B2m有效预防了HFD诱导的体重增加、脂肪堆积和脂肪细胞肥大,改善了肝脏的异位脂质沉积,并逆转了HFD诱导的葡萄糖不耐受和胰岛素抵抗,改善了血脂异常和脂肪因子异常,同时降低了EpiWAT中炎症因子的转录水平。总之,这些结果表明,在肥胖过程中干扰EpiWAT中B2M的表达能有效缓解肥胖以及相关代谢紊乱。
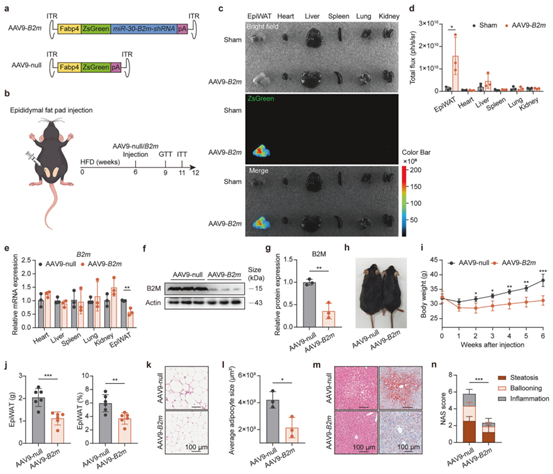
图7. AAV介导的EpiWAT中B2M敲低可改善肥胖和代谢紊乱
脂肪组织中B2M的表达与人类肥胖有关
为了确定B2M与人类肥胖的相关性,作者分析了代谢健康型肥胖人群、代谢不健康型肥胖人群和精瘦人群脂肪组织的RNA-seq数据库,KEGG和GO富集分析显示,与抗原加工和呈递以及铁离子转运相关的基因显著富集。肥胖人群皮下脂肪中的B2M、MHC-I分子、铁储存相关基因的表达显著高于精瘦人群,且代谢不健康型肥胖组高于代谢健康型肥胖组。另外,作者通过相关性分析显示,B2M表达与身体质量指数、脂肪细胞大小、甘油三酯水平、促炎因子水平、铁储存相关基因表达水平呈正相关,与脂联素、抗铁死亡基因的表达呈负相关。肥胖患者内脏脂肪组织中的B2M、MHC-I以及铁转运和储存相关蛋白的表达显著上调,FPN表达降低,与小鼠实验中B2M调控的铁代谢通路变化一致。总之,这些发现表明,人类脂肪组织中B2M的异常增加与肥胖相关的代谢紊乱有关。
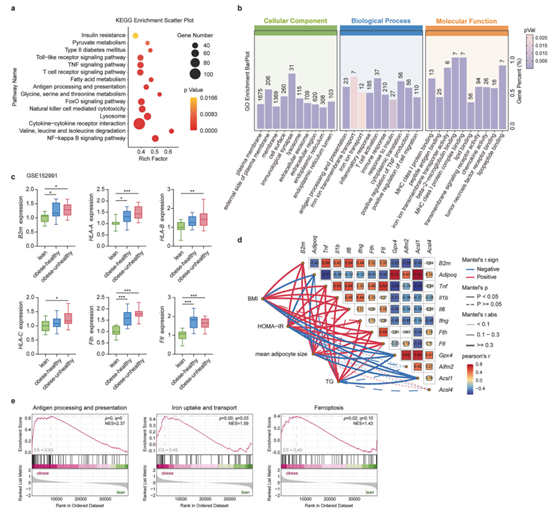
图8. 脂肪组织中B2M的表达与人类肥胖有关
总结
综上所述,该研究团队发现肥胖期间肥大脂肪细胞中B2M表达上调,并揭示了脂肪细胞通过B2M调控肥胖相关慢性炎症的双重机制:B2M既能通过MHC-I抗原呈递途径激活CD8+T细胞,又能通过调控铁稳态诱导脂肪细胞铁死亡,进而促进脂肪组织巨噬细胞向M1极化,这些发现不仅显著推进了对由脂肪细胞失调驱动的慢性脂肪炎症的理解,也为控制肥胖及其代谢并发症提供了潜在的新治疗靶点。
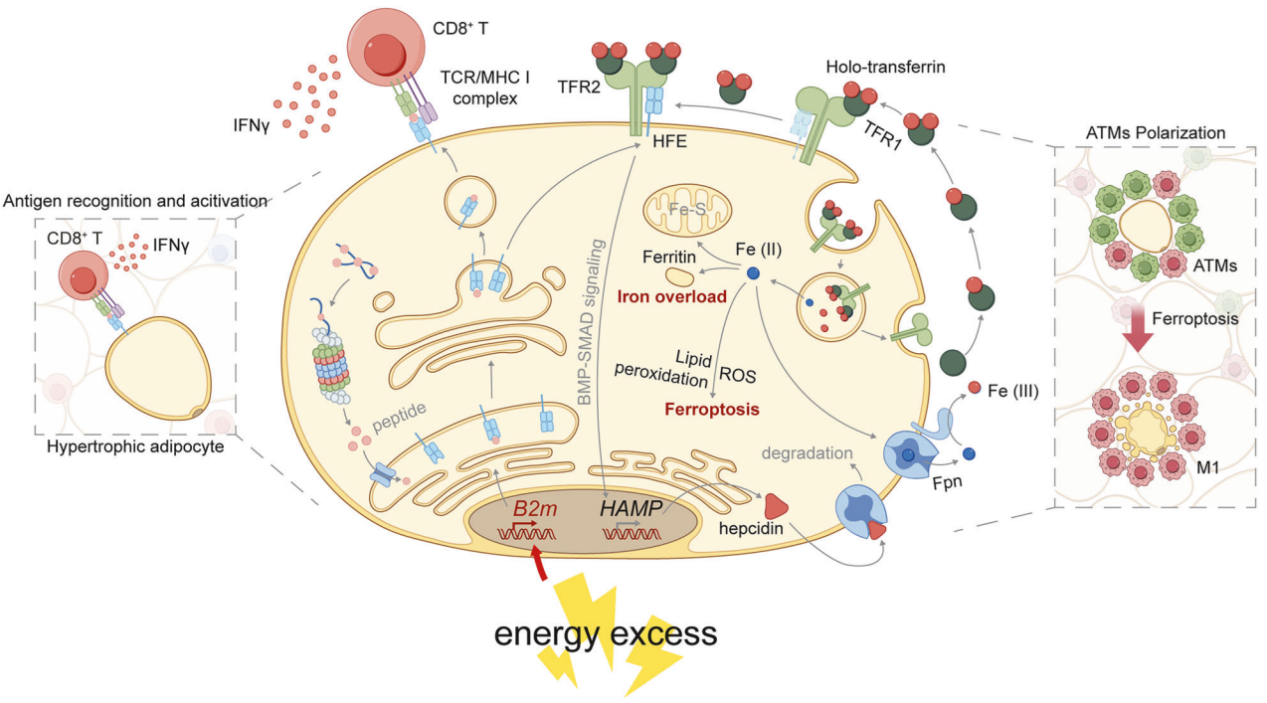
图9. 机制示意图

查看更多

查看更多

查看更多

联系我们

返回顶部