查看更多

 明星产品
明星产品
 关注我们
关注我们

扫码关注我们
了解更多信息
周围神经损伤(PNI)和糖尿病周围神经病变(DPN)是临床上常见且具有破坏性的疾病,常导致肢体感觉与运动功能障碍,严重影响患者的生活质量。目前,尽管已有临床技术与组织工程方法尝试修复神经损伤,但仍缺乏能够精准调控神经微环境、促进功能恢复的有效策略。近年来,手性对映体在多种疾病中表现出截然不同的生物学效应,为神经修复提供了新的研究方向。本研究基于手性选择性调控的概念,合成了右旋Fe3O4纳米颗粒(D-Fe3O4),并系统探讨了其加速周围神经结构与功能恢复的潜力,拓展了手性材料在神经修复领域的应用前景,为开发具有转化潜力的神经组织工程提供了新思路。

2025年10月,上海交通大学医学院附属第六人民医院范存义、周超、徐佳作为共同通讯作者在《ACS Nano》期刊发表了题为“An Autophagy-Sensitive Nanoplatform via Chirality-Selective Modulation for Functional Peripheral Nerve Repair and Target Organ Homeostasis”的研究论文。研究成功合成了Fe3O4纳米粒子对映体,其中D-Fe3O4被雪旺细胞(SCs)内吞后通过自噬驱动的p-JNK/EPHA5通路促进其增殖、迁移及再髓鞘化分化。在PNI和DPN动物模型中,负载D-Fe3O4的植入物显著加速神经结构与感觉—运动功能恢复,并维持靶器官形态与肢体稳态。本研究不仅深化了对手性材料在神经修复中作用机制的理解,也为功能性神经组织修复及靶器官稳态维持提供了一条具有重要转化潜力的新途径。
在本研究中,汉恒生物有幸为作者提供了我司金牌产品:自噬双标腺病毒mCherry-GFP-LC3,成功在小鼠原代雪旺细胞(mSCs)中实现了自噬过程的可视化。结果显示D-Fe3O4显著加速了mSCs的自噬流,这一关键发现为后续阐明其通过“自噬-p-JNK/EPHA5”轴促进神经修复的机制提供了直接的细胞生物学证据。
下面,我们一起来了解具体的研究内容:
1.手性Fe3O4对映体的制备与性能研究
研究采用天冬氨酸诱导的自组装策略,在聚己内酯(PCL)支架上成功合成了具有明确手性结构的Fe3O4纳米颗粒对映体(L型、D型、R型)。所得纳米颗粒呈棕色片层状,尺寸在纳米级范围,元素组成为Fe和O。结构表征证实其为高纯度立方相Fe3O4,其中L型和D型样品在原子晶格排列上呈现明显的手性旋转差异。圆二色光谱分析显示,L型与D型Fe3O4@PCL在220-550 nm范围内呈现镜像对称信号,证实了手性结构的成功构建。磁学测试表明D-Fe3O4具有独特的磁性,为未来磁导向递送提供了可能。此外,透射电子显微镜图像和荧光标记纳米颗粒摄取测定表明,Fe3O4对映体均可被SCs有效内吞,且各组内吞数量相当。以上结果为后续研究D-Fe3O4在手性选择性神经修复中的作用奠定了材料基础。
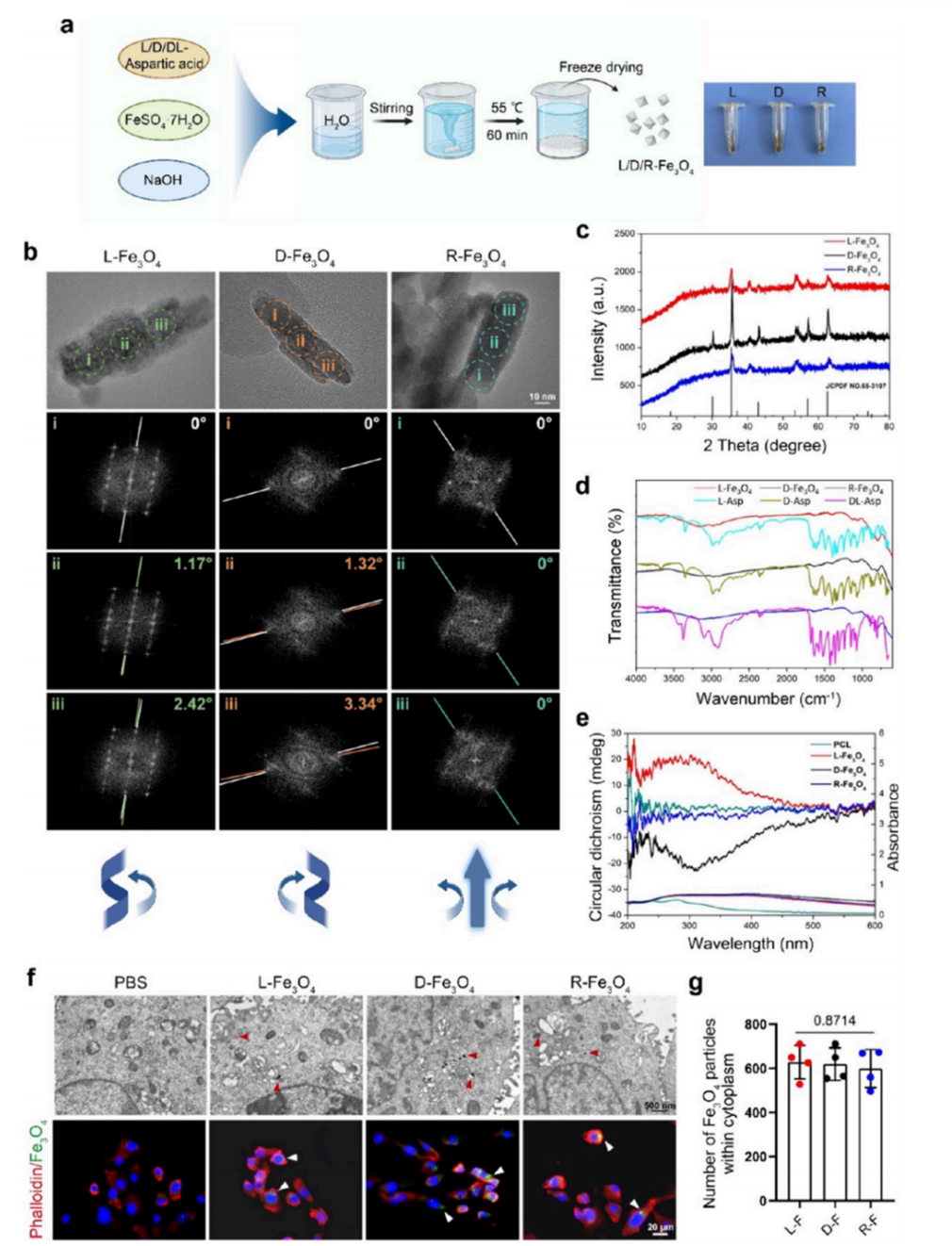
图1. 手性Fe3O4对映体的制备与表征
2.手性Fe3O4对映体对SCs的影响
获得手性Fe3O4对映体材料后,作者系统评估了不同手性Fe3O4对映体对SCs的生物学效应。实验表明,在10 μg/mL浓度作用下,三种对映体均未表现出细胞毒性,且对细胞活力无显著影响。功能学检测发现,D-Fe3O4能特异性促进SCs的增殖、迁移及分化,显著增强其分支形成能力,且效果显著优于L型和R型对映体。与无光学活性的常规Fe3O4及R型对映体相比,D-Fe3O4展现出更优的生物学功能。由此可见,D-Fe3O4对SCs具有手性选择性的功能增强作用,这为其在神经修复中的应用提供了重要依据。
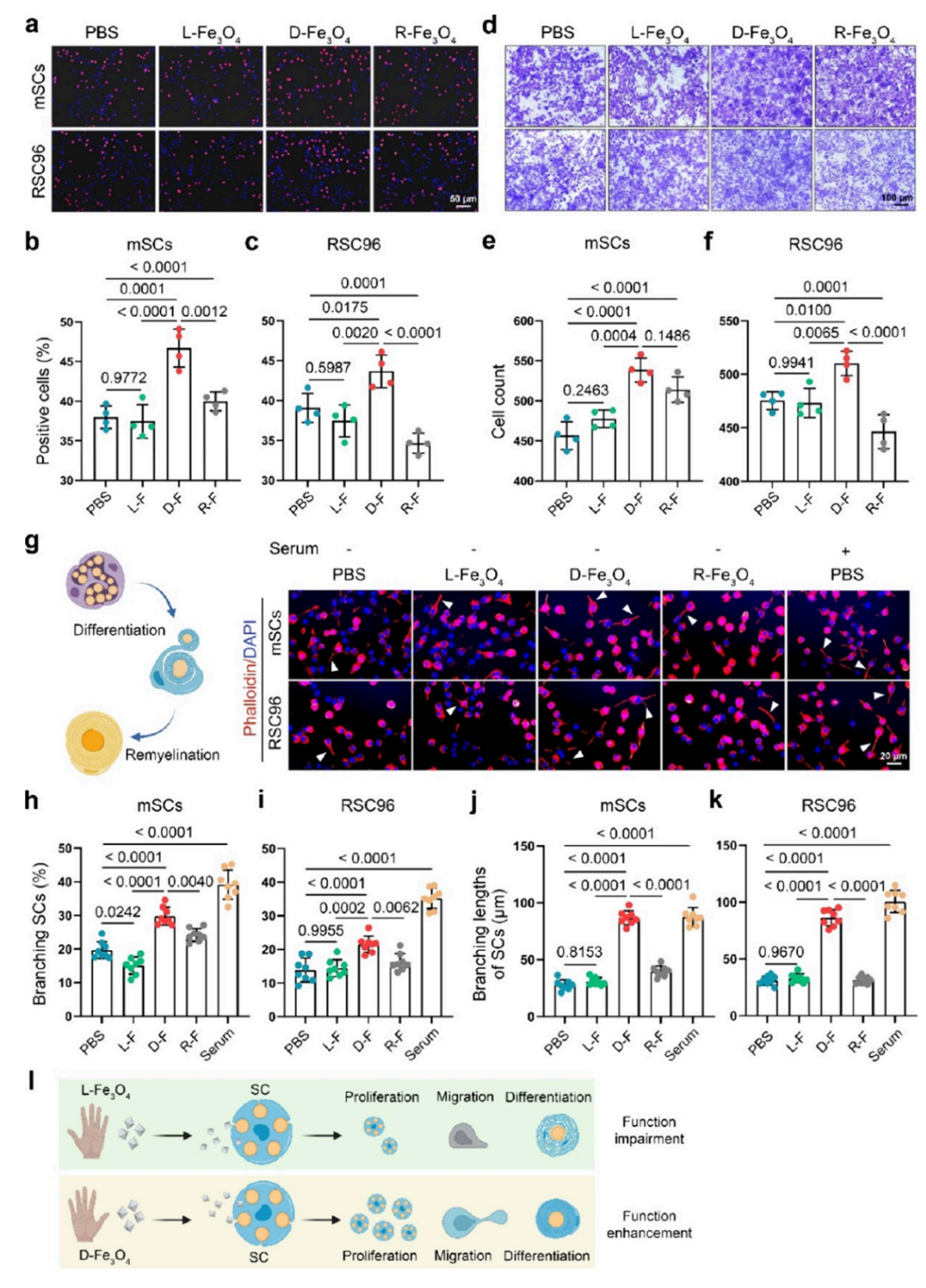
图2. Fe3O4对映体对髓鞘形成的影响
3.手性选择性自噬调控对SCs及轴突导向的作用
为探究D-Fe3O4的功能机制,作者对经L-Fe3O4和D-Fe3O4处理的SCs进行RNA测序和差异表达基因筛选及通路富集分析。结果显示,D-Fe3O4能特异性激活SCs的自噬流,显著上调自噬相关蛋白ATG16L1磷酸化及LC3的表达水平。机制研究表明,该过程依赖于D-Fe3O4与ATG16L1蛋白的特异性相互作用,敲低ATG16L1后其促修复作用完全消失。转录组分析显示,D-Fe3O4处理可特异性激活轴突导向关键因子EPHA5的表达,并通过增强自噬-JNK信号轴实现该调控。功能学验证证实,经D-Fe3O4预处理的SCs能显著促进背根神经节神经元的轴突延伸。这些结果表明,D-Fe3O4通过激活“自噬-JNK/EPHA5”信号轴,以手性选择性方式促进SCs介导的神经修复。
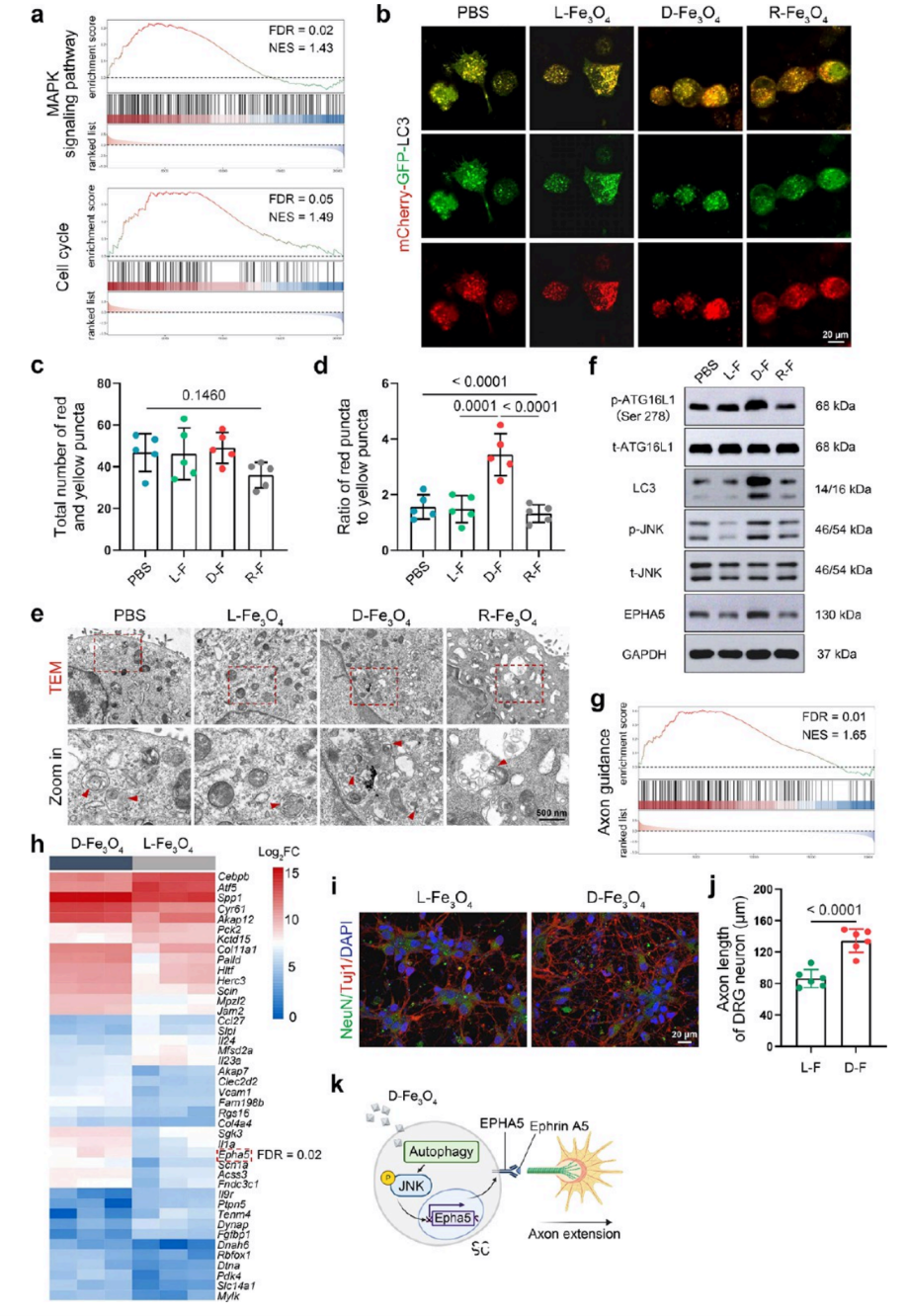
图3. 自噬通过EPHA5介导的轴突导向参与手性选择性神经修复
4.Fe3O4对映体对大鼠神经功能与形态恢复的差异性作用
在体外确定D-Fe3O4的功能后,作者通过大鼠坐骨神经15 mm缺损模型(PNI)系统评估了D-Fe3O4对映体的体内生物安全性与修复效能。实验结果显示:1)生物安全性方面,植入后血清学(AST、ALT、BUN、肌酐)及组织形态学分析均未发现明显器官损伤;2)感觉功能恢复上,D-Fe3O4组在热板实验中的痛觉恢复速度与自体移植组相当,且在12周时对机械性痛觉过敏的改善效果显著优于其他对照组;3)运动功能方面,步态分析显示D-Fe3O4组在术后12周足趾展开与步态协调性明显改善,坐骨神经功能指数恢复程度与自体移植组无统计学差异;4)电生理检测进一步证实,D-Fe3O4组神经传导速度与复合肌肉动作电位恢复指数均表现出与自体移植相似的优异恢复效果。综上,D-Fe3O4在PNI模型中展现出与自体移植相当的生物安全性和多维度神经功能的修复能力。
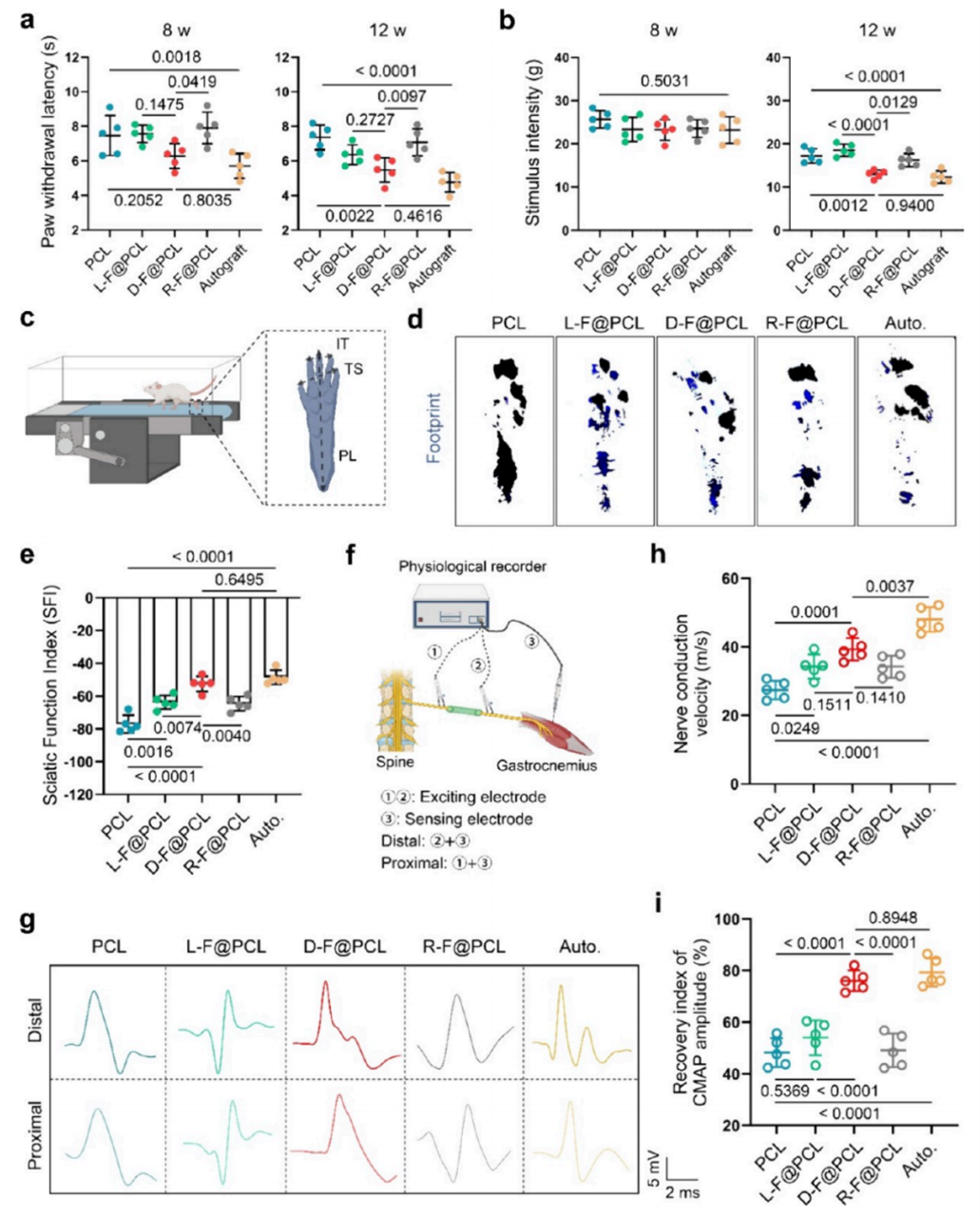
图4. 大鼠坐骨神经损伤后功能恢复的评估
通过透射电子显微镜(TEM)、组织学染色及免疫荧光染色等组织学评估发现,术后12周时,D-Fe3O4组再生神经的髓鞘厚度、轴突直径及g-比率(反映髓鞘的厚度和神经传导效率)等指标优于L-Fe3O4组,接近自体移植水平,神经纤维数量更多且结构更完整。免疫荧光染色进一步证实,D-Fe3O4组髓鞘化神经纤维密度更高(标记物MBP和S100β表达上调),轴突延伸标志物(Tuj1和NF200)表达更强。表明D-Fe3O4能有效促进髓鞘修复和轴突再生,优于L-Fe3O4和R-Fe3O4。
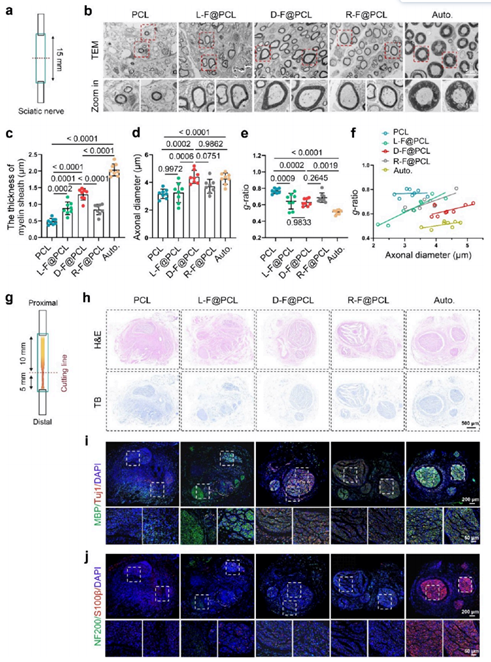
图5. 再生神经纤维形态学重建的评估
PNI会因去神经化引起的微环境紊乱而影响所支配肌肉的结构和功能,而D-Fe3O4在PNI修复中展现出显著优势。实验发现,D-Fe3O4组在术后12周时,L5水平脊髓的Nissl+细胞数量增多,且Nestin表达升高、GFAP表达降低,提示其能加速脊髓功能恢复并减少胶质瘢痕形成。在肌肉层面,D-Fe3O4有效维持了比目鱼肌的形态和湿重,与自体移植组效果相当,并通过H&E及Masson染色证实其能减少肌肉纤维萎缩和胶原沉积。进一步分析显示,D-Fe3O4组快慢肌球蛋白的分布更接近正常生理状态,表明其能促进肌肉功能特异性恢复。综上,D-Fe3O4可以作为PNI修复的一种高效且生物相容性良好的治疗途径。
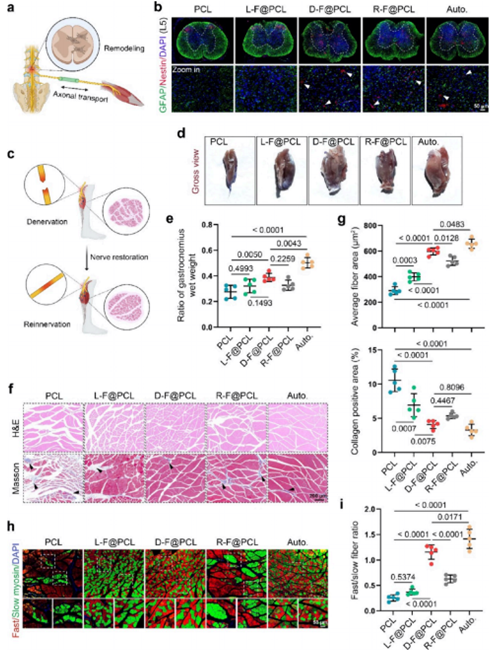
图6. 受损伤神经支配的靶器官检测
7.Fe3O4对映体在DPN大鼠模型中的手性选择性效应
DPN动物模型的研究结果表明,D-Fe3O4在缓解神经病变进展中表现出显著优势。在功能层面,D-Fe3O4 能有效改善DPN早期典型的肢体远端感觉功能障碍,显著减轻热板实验和Von Frey试验中的痛觉过敏症状。D-Fe3O4在改善神经传导速度(NCV)和复合肌肉动作电位(CMAP)方面优于L-Fe3O4和R-Fe3O4组,尤其在术后24周效果突出。透射电镜(TEM)分析表明,D-Fe3O4显著延缓DPN导致的脱髓鞘病变,受损神经纤维数量明显少于对照组。免疫荧光染色(S100β/Tuj1)证实其具有更强的轴突保护作用。这些结果共同说明D-Fe3O4在改善DPN病理进程中的综合效能显著优于其他对映体形式。
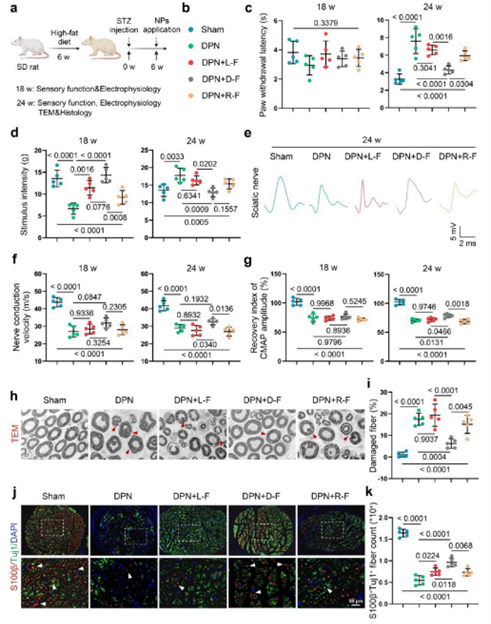
图7. DPN大鼠神经功能与结构的评估
研究显示,DPN模型大鼠的坐骨神经会出现明显的轴突密度下降、脱髓鞘及轴突退化现象,而负载D-Fe3O4的神经支架能显著保护轴突结构,其效果明显优于其他手性对映体(L-Fe3O4与R-Fe3O4)。机制研究表明,D-Fe3O4能有效恢复神经组织的自噬水平,使其接近生理状态。在靶器官层面,Masson染色显示D-Fe3O4治疗组肌纤维面积增大、胶原沉积减少;快慢肌球蛋白检测证实该组肌肉功能得到显著改善。综上结果表明,D-Fe3O4不仅能够通过调控自噬促进神经结构修复,还能有效延缓肌肉萎缩,为DPN的临床干预提供了新的实验依据。

图8. 受损神经及其靶器官的组织学评估
总结
综上所述,本研究不仅证明了D-Fe3O4在手性选择性调控中的优越性,还阐明了其通过自噬-JNK/EPHA5轴促进神经修复和靶器官保护的机制,为PNI和DPN的治疗提供了全新的纳米治疗平台和理论依据,具有重要的科学价值和临床转化前景。
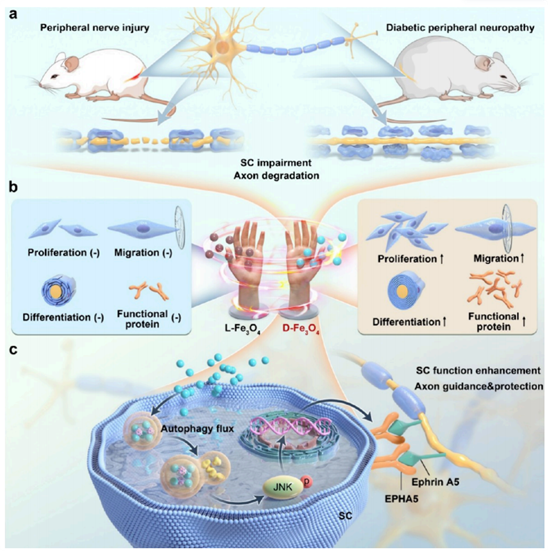
图形摘要. 手性选择性调控的D-Fe3O4对映体用于神经组织修复的示意图

查看更多

查看更多

查看更多

联系我们

返回顶部