查看更多

 明星产品
明星产品
 关注我们
关注我们

扫码关注我们
了解更多信息
骨关节炎(OA)是一种以软骨破坏、骨赘形成和滑膜炎为主要病理特征的退行性关节疾病,严重影响老年人的生活质量。目前,临床治疗主要依赖非甾体抗炎药、皮质类固醇注射和关节置换术,这些治疗方式虽能缓解症状,但无法逆转OA进展,并且目前尚无可用于治疗OA的靶向药物。近年来,随着对OA发生发展机制的深入研究,发现软骨细胞衰老及其慢性炎症在其中起核心作用。而蛋白质棕榈酰化作为一种动态、可逆的翻译后修饰,可调控蛋白质的功能进而参与多种病理过程,但其在OA中的作用和机制尚不清楚。因此,本研究旨在探索棕榈酰化修饰在OA进程中的调控作用。

2025年9月30日,浙江大学医学院附属邵逸夫医院沈舒滢、赵兴与东南大学附属中大医院季明亮在《Nature Aging》(IF=19.5)上联合发表题为“ZDHHC11-mediated palmitoylation alleviates chondrocyte senescence and serves as a therapeutic target for osteoarthritis”的研究论文。本研究揭示了棕榈酰转移酶ZDHHC11作为OA治疗潜在新靶点的作用与机制。研究发现,ZDHHC11在衰老及OA软骨中表达下调,而在软骨细胞与小鼠模型(包括自然衰老及Zdhhc11条件性敲除小鼠)中过表达ZDHHC11均能有效抑制软骨细胞衰老、促进细胞外基质(ECM)合成并缓解OA病理表型。在机制上,阐明了ZDHHC11可催化载脂蛋白D(APOD)发生棕榈酰化修饰,这与E3泛素连接酶GNB2介导的APOD泛素化过程相竞争,从而稳定APOD蛋白水平。进一步研究发现,APOD通过抑制衰老相关信号GATA4-P65,减轻炎症与ECM分解代谢,最终延缓软骨衰退。基于此,作者创新性地开发了装载Zdhhc11 mRNA的软骨靶向脂质纳米颗粒递送系统(mRNA-LNP-CAP),该体系能在动物模型中实现特异性递送并显著改善OA进展。该研究不仅首次明确ZDHHC11通过介导棕榈酰化修饰调控软骨衰老和炎症进程,为理解OA发病机制提供新视角,同时也为开发针对OA的靶向核酸疗法奠定了重要理论基础。
汉恒生物有幸为作者提供了ZDHHC11和APOD的过表达AAV载体,通过关节腔注射成功在小鼠关节软骨中过表达ZDHHC11和APOD,辅助阐明了其在OA中的作用机制。
下面我们一起来看看作者的研究过程和结果:
1.ZDHHC11在衰老软骨细胞及退行性OA组织中表达下调
作者首先分离了原代人软骨细胞(HCs),并用IL-1β处理细胞以诱导炎症环境,处理后棕榈酰化水平显著下降(补充图1 a)。同时,在未处理的HCs和小鼠软骨细胞(MCs)中鉴定出5种高表达的棕榈酰化转移酶,当用siRNA分别敲低基因后,仅ZDHHC11敲低后对软骨细胞分解代谢和衰老有显著影响(补充图1 b-d,图1 a)。进一步研究发现,IL-1β处理后Zdhhc11 mRNA的表达水平下降(图1 b)。在OA患者中,通过番红O-固绿染色和免疫荧光染色发现,ZDHHC11的表达随软骨降解及衰老标志物升高而降低,且与Kellgren–Lawrence(评估OA严重程度的影像学标准)分级呈负相关(图1 c, g)。在连续传代或H2O2诱导衰老的HCs中,ZDHHC11的蛋白水平也显著下降,SA-β-Gal(细胞衰老标志物)阳性区域增加(图1 d-f)。综上提示ZDHHC11可作为评估OA严重程度的指标。
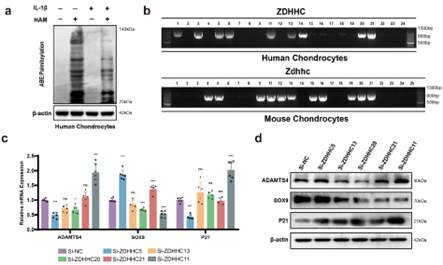
补充图1. HCs中ZDHHC11的鉴定与表征
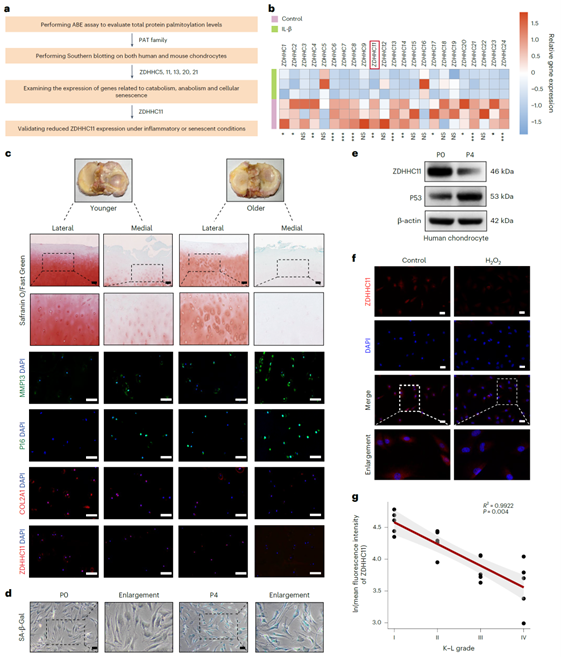
图1. ZDHHC11在老年OA患者及衰老软骨细胞中的表达下调
2.ZDHHC11减轻衰老相关的OA病理表型
上述结果表明ZDHHC11可能具有保护软骨的作用。为验证其在体内的作用,作者对年轻(3月龄)和老年(24月龄)小鼠实施内侧半月板失稳(DMM)手术构建OA模型,并于术后14天在关节腔内注射AAV- Zdhhc11进行基因治疗。结果显示,ZDHHC11过表达后能显著减轻OA的严重程度,具体表现为骨赘数量减少、滑膜损伤和滑膜炎得到缓解、OARSI评分(OA软骨损伤分级)降低(图2 a-g)。在分子层面,治疗组的COL2A1蛋白水平升高,而MMP3、IL-6、P21和P16的表达下降(图2 f)。此外,ZDHHC11过表达还改善了小鼠的机械性痛觉超敏反应(图2 h)。动物实验结果支持了ZDHHC11作为治疗衰老相关性OA的潜在靶点。
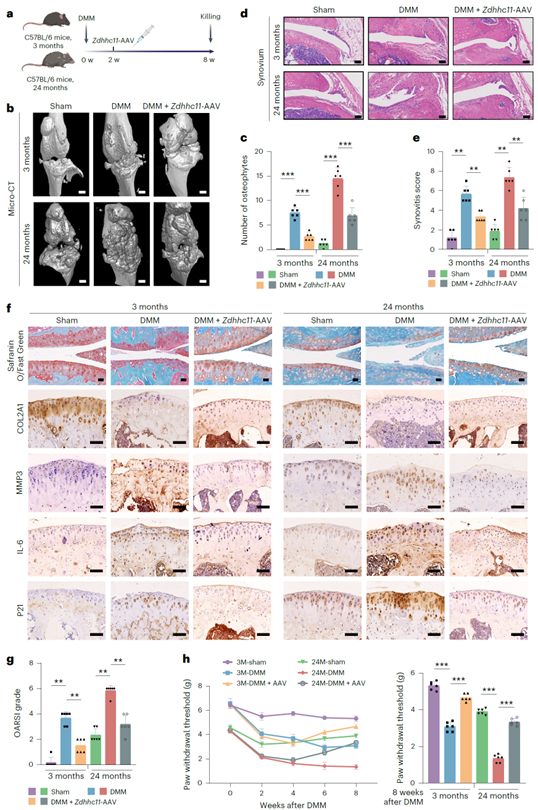
图2. ZDHHC11在体内可缓解与年龄相关的OA病理表型
3.ZDHHC11在Zdhhc11 cKO-DMM小鼠模型中显著缓解侵袭性OA表型
接着,作者通过挽救实验探究了ZDHHC11在OA及细胞衰老表型中的作用。在Zdhhc11条件性敲除(cKO)小鼠模型中实施DMM手术,术后14天在关节腔注射AAV-Zdhhc11病毒。结果发现,在cKO-DMM小鼠中恢复ZDHHC11的表达有效逆转了OA严重程度,并缓解OA症状,具体表现为减轻了骨赘形成、滑膜炎和关节软骨退化,关节疼痛得到缓解,同时降低了衰老标志物的表达(图3)。这些结果提示ZDHHC11在OA进展过程中具有关节保护作用。
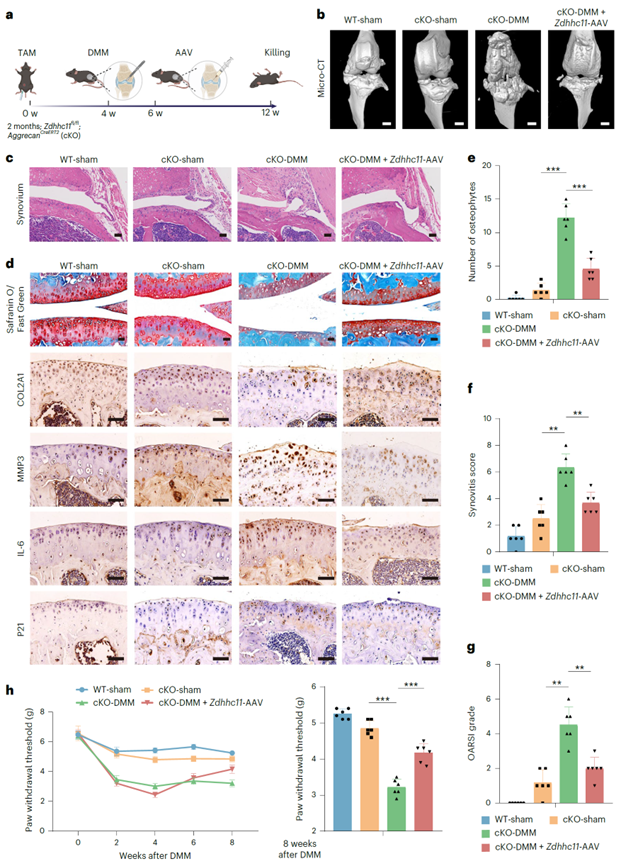
图3. ZDHHC11可减轻Zdhhc11 cKO-DMM小鼠的侵袭性OA表型
4.ZDHHC11作为棕榈酰化酶可介导APOD的棕榈酰化修饰
基于上述实验证明ZDHHC11在OA中的关节保护及抗衰老作用,作者继续探讨了其中的分子机制,特别是其作为棕榈酰转移酶的下游靶点的相关功能。在ZDHHC11过表达的软骨细胞中通过IP-MS和生信分析显示,APOD可能是ZDHHC11的关键互作蛋白(图4 a-c)。经Co-IP、分子对接及ABE实验证实,ZDHHC11与APOD的C185位点直接结合,并介导其棕榈酰化修饰(图4 d-f)。采用单细胞RNA测序进一步分析发现,不同软骨细胞亚群中APOD的表达水平与衰老基因评分(SenMayo)呈负相关(图4 g-i)。这表明APOD在衰老相关OA中具有抗衰老作用,且受ZDHHC11调控。
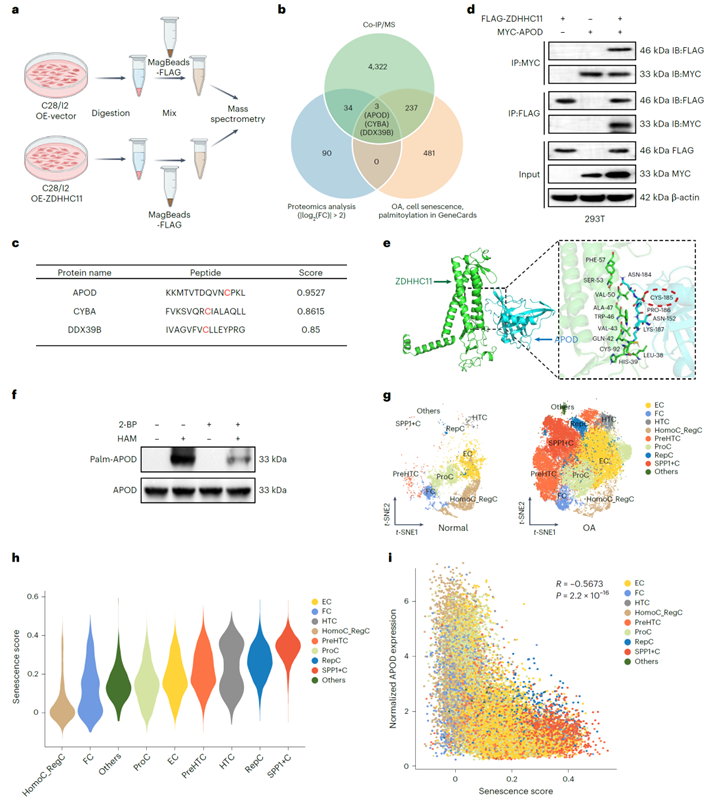
图4. ZDHHC11作为棕榈酰转移酶介导APOD棕榈酰化修饰
5.APOD的C185位点棕榈酰化可抑制ECM分解代谢及软骨细胞衰老
为探究APOD棕榈酰化水平在OA和软骨细胞衰老中的作用,作者发现其C185位点在物种间具有高度保守性,并对其进行C185A突变模拟去棕榈酰化修饰(图5 a,b)。当敲除ZDHHC11时,显著降低了野生型APOD的棕榈酰化水平,而过表达后能逆转该效应,但对于APOD(C185A)突变体则未检测到棕榈酰化修饰水平(图5 c-e)。在软骨细胞中过表达APOD能促进软骨细胞标志物的表达,同时降低ECM合成代谢因子、细胞衰老标志物的表达,进而改善OA和衰老表型;而过表达APOD(C185A)突变体的效果则相反(图5 f-i)。这些结果表明,ZDHHC11介导的APOD C185位点棕榈酰化是抑制ECM降解和软骨细胞衰老、进而延缓OA进展的关键分子机制。
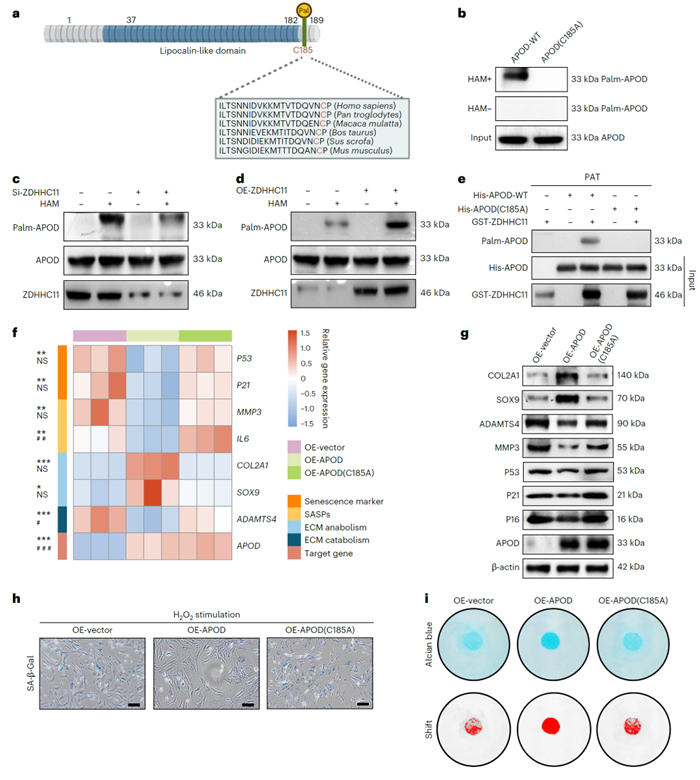
图5. APOD蛋白在C185位点的棕榈酰化修饰可抑制ECM降解代谢及软骨细胞衰老
6.APOD去棕榈酰化通过E3泛素连接酶GNB2触发蛋白酶体降解途径
接着,作者研究了APOD蛋白稳定性受棕榈酰化和泛素化调控的分子机制。结果表明,使用2-BP(棕榈酰化抑制剂)处理软骨细胞会显著降低APOD的稳定性,并加速其通过泛素-蛋白酶体途径降解(图6 a-c)。进一步研究发现,E3泛素连接酶GNB2与APOD存在相互作用,且介导APOD的泛素化(图6 d-f)。从机制上看,ZDHHC11催化的APOD棕榈酰化与GNB2介导的泛素化之间存在竞争关系,即棕榈酰化修饰能阻碍GNB2与APOD的结合,从而抑制其泛素化降解,而去棕榈酰化则促进APOD与GNB2的结合及泛素化(图6 g-k)。综上所述,抑制APOD的棕榈酰化会阻断其对软骨细胞的保护作用,敲低GNB2则能增强该保护作用(图6 l)。
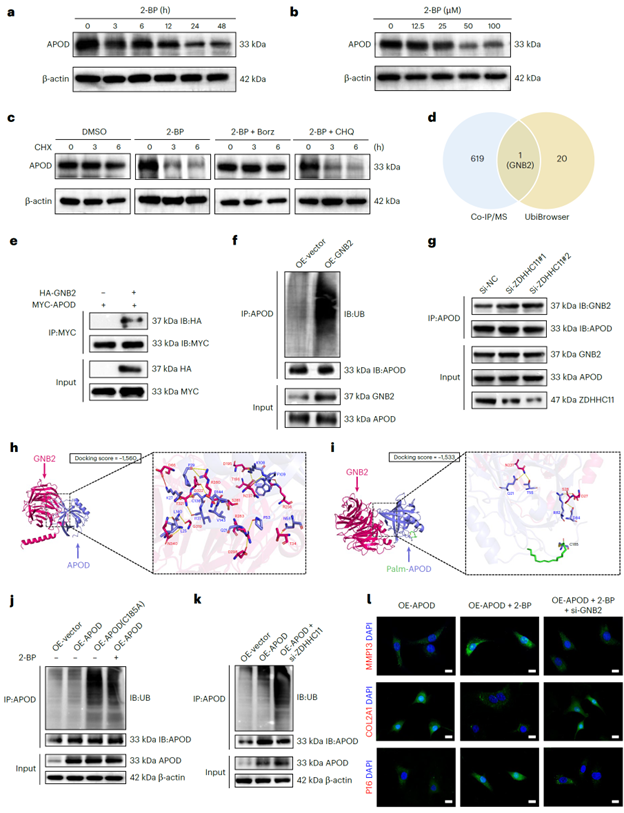
图6. APOD去棕榈酰化通过E3泛素连接酶GNB2介导蛋白酶体途径降解
7.ZDHHC11介导的棕榈酰化通过抑制GATA4-P65信号通路缓解OA进展
随后,作者探究了ZDHHC11介导的APOD棕榈酰化调控ECM代谢与细胞衰老的分子机制。在HCs中敲低ZDHHC11或APOD,一致地发现GATA4表达显著上调,并激活下游的NF-κB信号通路促进P65的磷酸化与核转位;反之,过表达ZDHHC11或APOD可逆转这些效应,同时敲低GATA4又能阻止这种逆转效应(图7 a-i)。其中P65磷酸化与GATA4表达上调与APOD的去棕榈酰化与泛素化水平呈正相关关系(图7 j)。此外,在ZDHHC11敲低的HCs中过表达APOD,可显著抑制HC衰老和ECM代谢异常(图7 k)。这些结果证实ZDHHC11介导的APOD棕榈酰化通过竞争性抑制GNB2介导的泛素化,下调衰老相关GATA4-P65信号通路,从而缓解OA进展。
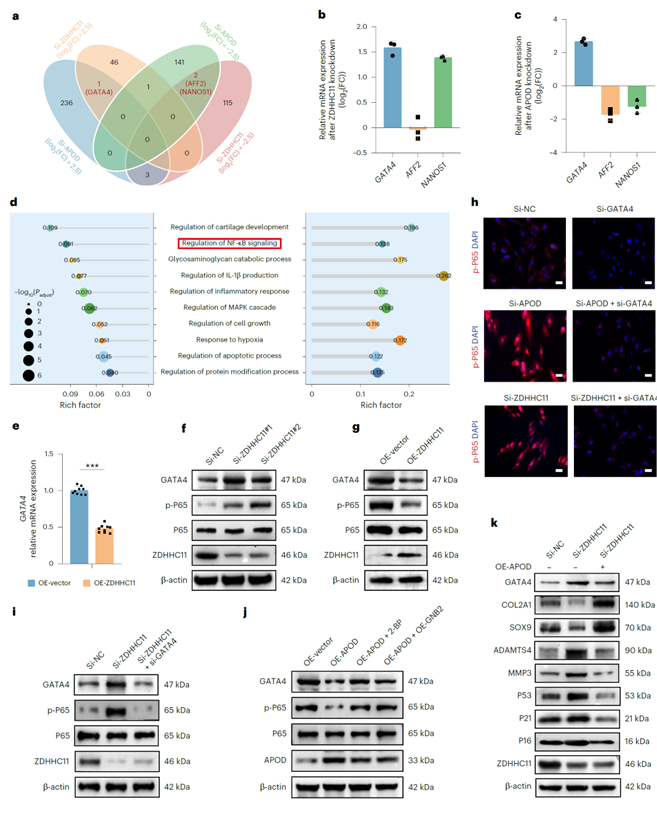
图7. ZDHHC11介导的棕榈酰化通过抑制GATA4-P65信号通路缓解OA进展
8.Zdhhc11 mRNA-LNP可恢复OA大鼠的软骨完整性,并显著减轻其关节衰老程度
针对ZDHHC11对OA的治疗潜力,作者开发了一种靶向软骨细胞的脂质纳米颗粒递送系统,用于递送Zdhhc11 mRNA,并在大鼠OA模型中验证了其治疗效果。结果显示,经软骨靶向肽(CAP)修饰的mRNA-LNP(mRNA-LNP-CAP)能特异性被软骨细胞摄取并高效表达目的蛋白(图8 a-e)。在体内实验中,大鼠进行DMM手术后,6周内每周通过关节腔注射Zdhhc11 mRNA-LNP-CAP,与无靶向效果的Zdhhc11 mRNA-LNP对照相比,Zdhhc11 mRNA-LNP-CAP能更有效地缓解关节病变,具体表现为骨赘形成显著减少、滑膜炎减轻、软骨降解被抑制、OARSI评分降低,且衰老相关信号GATA4-P65被抑制(图8 f-k)。综上结果,Zdhhc11 mRNA-LNP-CAP能促进软骨修复和抑制细胞衰老,有效缓解OA的进展。
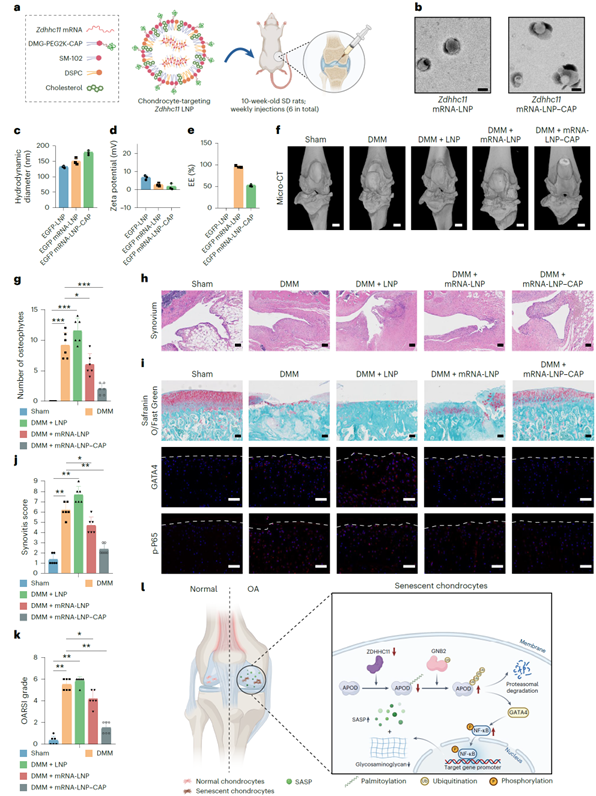
图8. Zdhhc11 mRNA-LNP-CAP可挽救OA软骨衰退并有效缓解大鼠关节衰老
总结
综上,本研究明确了ZDHHC11在OA发生发展中对软骨起关键保护作用,它可抑制HC相关ECM分解代谢和衰老表型。从机制上看,ZDHHC11介导APOD发生棕榈酰化修饰,以竞争性抑制GNB2介导的APOD泛素化降解,进而抑制GATA4-P65信号通路,减少炎症反应与分解代谢,最终延缓软骨退变与细胞衰老进程。研究进一步开发了靶向软骨递送Zdhhc11 mRNA的脂质纳米颗粒系统,为OA治疗提供了新的靶向策略。该项工作不仅阐明了蛋白质棕榈酰化修饰在OA中的新机制,也为开发药物靶向递送系统奠定重要基础。

查看更多

查看更多

查看更多

联系我们

返回顶部