查看更多

 明星产品
明星产品
 关注我们
关注我们

扫码关注我们
了解更多信息
荧光素酶作为一种理想的报告基因,被广泛应用于转录因子结合位点与启动子活性分析、信号转导、药物筛选、动物活体成像等领域。本期小编为大家介绍双荧光素酶报告系统在基因转录调控验证方面的应用,主要从以下五个方面展开介绍:基因转录调控机制、调控元件的生物信息学分析、双荧光素酶验证系统相应质粒体系及反应原理、双荧光素酶系统的应用、双荧光素酶系统应用的案例分享。

一、基因转录调控机制
真核生物基因表达是一个十分复杂而有序的过程,依赖于众多反式作用因子(如转录因子)和顺式作用元件(如启动子、增强子和抑制子等)之间的精确互作。基因表达在多个层次受到调控,包括染色体结构、转录、转录后加工、翻译和翻译后修饰等。其中,转录水平的调控发生在基因表达的初期阶段,是基因表达调控的关键环节,主要通过转录因子特异识别并结合靶基因调控区的顺式元件,从而调节基因表达的强度、控制基因表达的时空特异性、或应答外界刺激和环境胁迫,最终影响生物表型及生理功能,对生命的正常发育和进化至关重要。

图1. 基因转录机制示意图[1]
在顺式调控元件中,启动子是位于基因上游的一段DNA序列,作为转录起始的关键调控区域,负责招募RNA聚合酶及相关转录因子,启动基因转录,其核心元件通常包括TATA框、CAAT框和GC框等,这些元件的组合和序列特征决定了启动子的基础活性和调控特征;增强子则通常位于基因上游、下游甚至内含子中,增强子通过形成染色质环与启动子区域物理接近,招募转录因子和辅激活因子,显著提升转录效率;相反,抑制子(或沉默子)则具有抑制转录的功能,可远距离或近距离降低启动子活性,参与基因表达的负调控。
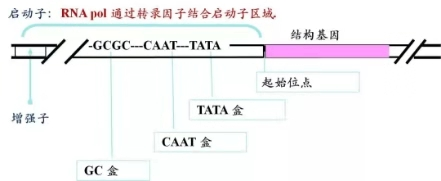
图2. 启动子关键元件示意图
了解启动子、增强子、抑制子及转录因子之间的互作关系,对于解析基因功能、信号通路调控网络及相关分子机制具有重要的研究意义。双荧光素酶报告系统通过将待研究的调控元件克隆至荧光素酶报告基因上游或下游,构建报告载体,转入细胞后通过检测荧光素酶活性变化,直观反映调控元件的功能及转录因子与元件的互作效应,已成为该研究领域的经典验证实验。下面小编为大家详解一下利用双荧光素酶报告系统进行转录调控元件活性及结合位点预测等实验设计的思路与方案。
二、调控元件的生物信息学分析与预测
在线网站UCSC(https://www.genome.ucsc.edu/)与NCBI(https://www.ncbi.nlm.nih.gov/)是获取目标基因启动子序列的常用数据平台。一般可提取转录起始位点(TSS)上游约2000 bp区域作为待研究的启动子序列;
在线网站JASPAR(https://jaspar.genereg.net/)是常用的转录因子结合基序数据库,可输入启动子序列预测潜在的转录因子结合位点;
EnhancerAtlas(http://www.enhanceratlas.org/)、dbSUPER(https://asntech.org/dbsuper/)等数据库则收录了多种细胞与组织中的增强子注释信息。
关于转录因子与启动子结合位点预测的详细方法可关注“小恒学术”视频号,观看往期相关视频,了解更多、更详细的查找序列和预测结合的操作步骤等。
三、双荧光素酶验证系统相应质粒体系及反应原理
用于启动子活性及与转录因子结合验证的双荧光素酶报告系统包括:pGL3-Basic质粒,将待分析的启动子元件序列构建到F-Luciferase上游的多克隆位点处;pcDNA3.1系列质粒,用于过表达待测转录因子。而用于增强子/抑制子研究的双荧光素酶报告系统包括:pGL3-Promoter质粒,将待分析增强子/抑制子序列构建到启动子上游。以上两个系统均需要共转pRL-TK质粒,用于表达R-Luciferase的内参质粒。
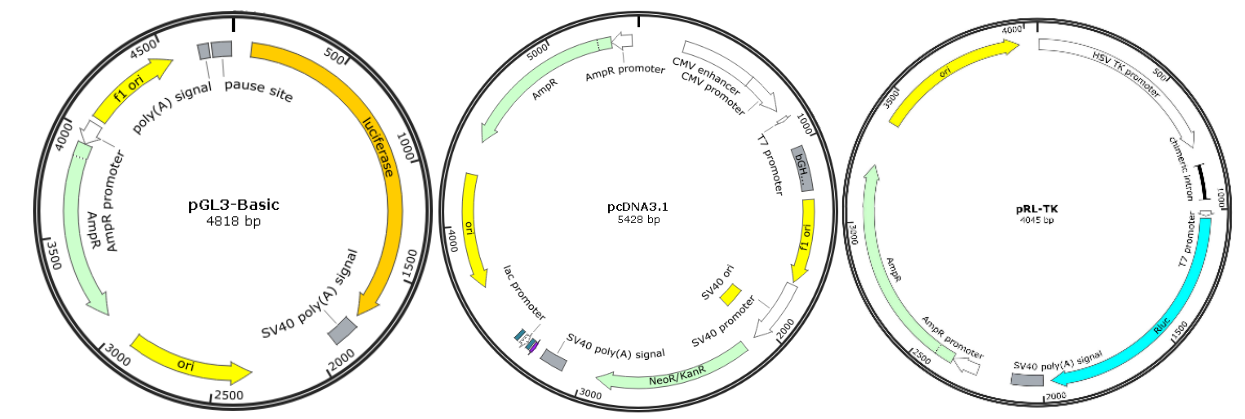
图3. 启动子和转录因子互作验证双荧光素酶质粒系统
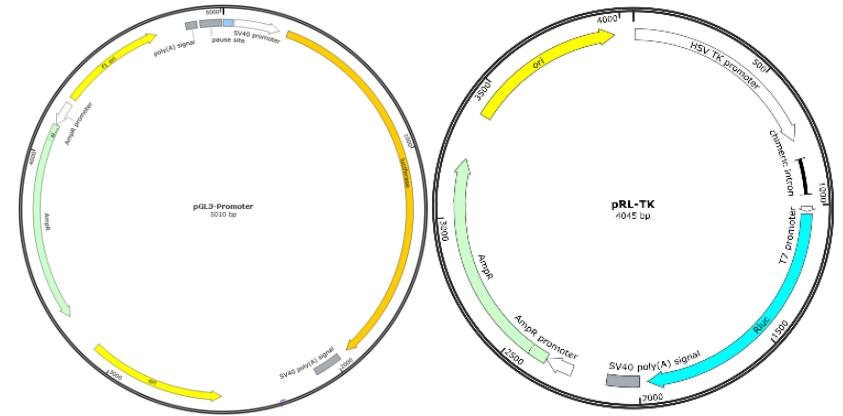
图4. 增强子/抑制子活性验证双荧光素酶质粒系统
利用荧光素酶与底物结合发生化学发光反应的特性,将上述构建好的启动子活性验证质粒或增强子/抑制子活性验证质粒或转录因子表达质粒等实验所需待测质粒转染细胞,同时转染内参质粒pRL-TK以校正不同样品之间的转染效率。随后,经适当刺激或处理后裂解细胞,测定荧光素酶活性,通过荧光素酶活性高低判断刺激因素/转录因子等对待测顺式作用元件调控的影响。

图5. 转录因子与启动子互作验证反应过程
四、双荧光素酶系统的应用
1.潜在启动子/启动子核心区活性检测
实验思路:截断式检测,即逐步缺失远端序列(因为核心启动子位置靠近TSS端,缺失近端处会丧失基本转录活性),适用于确定启动子核心区域或转录因子与启动子预测结合位点较多且评分相近,需要进一步缩小范围的情况。一般选取目的基因上游总长为2000 bp碱基(也可选取基因上游2000 + 下游200 bp)作为目标基因的启动子序列进行验证。通过Fluc/Rluc荧光素酶活性比值表示启动子转录活性的强弱。
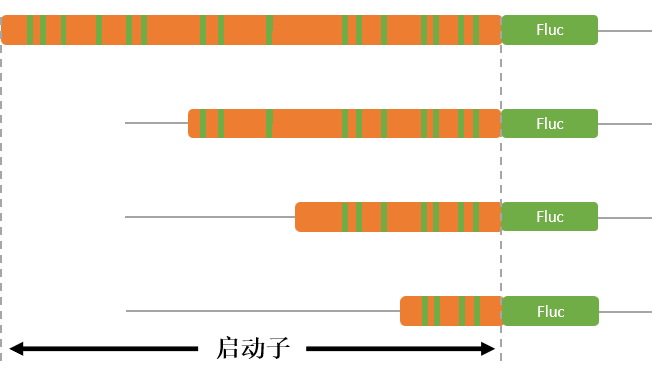
图6. 启动子截断序列示意图
表1. 截断式启动子活性验证的双荧光素酶实验分组

1/2组去背景值后通过荧光素酶活性对比可验证待测启动子活性;2/3/4/5去背景值后可通过荧光素酶活性验证待测启动子的核心区域。
2.潜在增强子/抑制子等调控子活性检测
1)将增强子/抑制子的调控元件构建至pGL3-Promoter报告载体的多克隆位点区域(SV40启动子前),并检测双荧光素酶活性。以增强子Enhancer为例说明,通过Fluc/Rluc荧光素酶活性比值表示增强子对下游基因启动转录增强的效果。
表2. 增强子活性验证的双荧光素酶实验分组

2)将增强子/抑制子的调控元件和待测启动子序列构建至pGL3-Basic报告载体的多克隆位点区域(报告基因Fluc前),并检测双荧光素酶活性。本实验分组可参考表3,其中四组实验可以同时进行,也可以先验证启动子活性(实验组1+实验组2)后,再验证增强子活性。以增强子Enhancer为例进行展示。
表3. 增强子和目的启动子活性验证的双荧光素酶实验分组
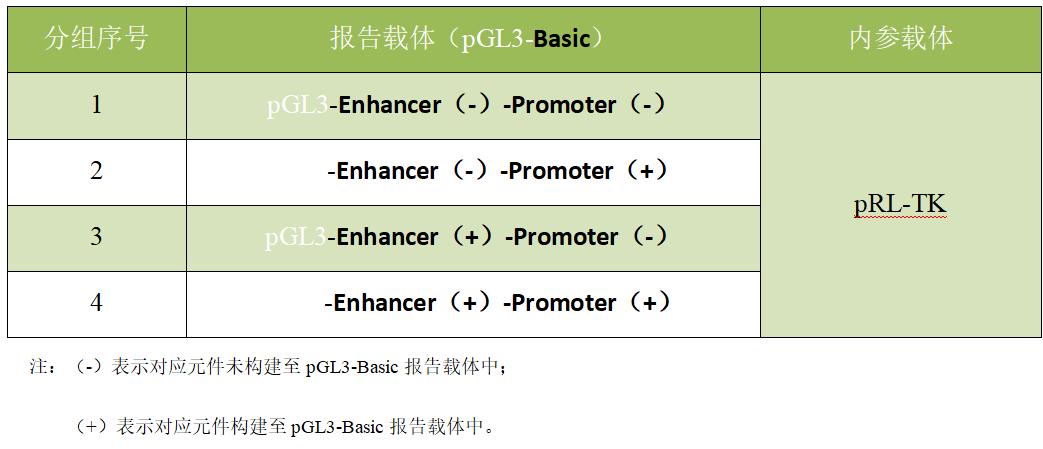
1/2组荧光素酶活性对比表示目的启动子的启动活性(若有多个待验证的启动子区域则增加分组);1/3组荧光素酶活性对比表示增强子/抑制子是否具备启动转录活性;2/4组荧光素酶活性对比表示增强子/抑制子对下游基因启动转录增强/抑制的效果。
3.启动子和转录因子互作验证
转录因子可以结合至启动子区域,改变启动子启动转录功能的强弱,进而引起下游报告基因Fluc转录水平的变化,通过酶标仪检测底物与荧光素酶反应发光强弱的改变,最终验证启动子和转录因子的互作关系。
1)验证转录因子与启动子的互作
表4. 启动子和转录因子结合验证的双荧光素酶实验分组
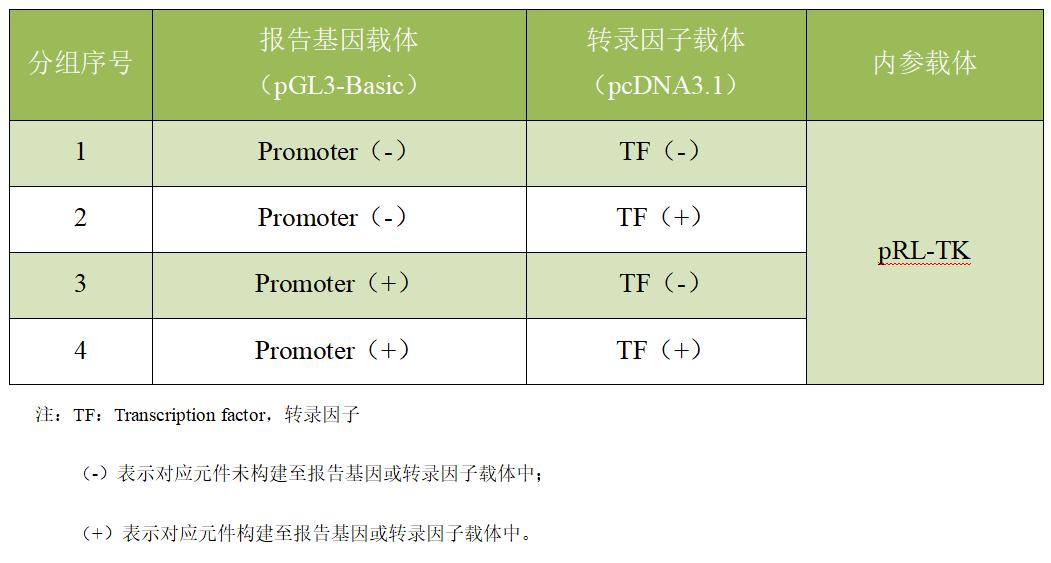
1/3组荧光素酶活性对比表示目的启动子的启动活性(若有多个待验证的启动子区域则增加分组);1/2组荧光素酶活性对比表示转录因子是否具备启动转录活性;3/4组荧光素酶活性对比表示转录因子对下游基因启动转录增强/抑制的效果。
2)验证转录因子与启动子的互作位点
在四组的基础上加上各个待验证结合位点突变型启动子载体,以验证转录因子与启动子的具体结合位点(预测结合位点1突变型启动子:Promoter-Mut1、预测结合位点2突变型启动子:Promoter-Mut2、预测结合位点3突变型启动子:Promoter-Mut3)。每多一个待验证启动子结合位点,则建议增加2组:启动子突变型报告基因载体+TF转录因子载体组和启动子突变型报告基因载体+TF转录因子空载体组。
表5. 启动子和转录因子结合位点验证的双荧光素酶实验分组

若3/4组荧光素酶活性对比表示转录因子对下游基因启动转录具有增强/抑制的调控作用,则6/8/10通过突变不同预测结合位点,可以观察荧光素酶活性是否改变,说明是否在对应突变位置上进行结合。5/7/9作为严格对照,表示突变体启动子仍具有启动转录活性。
五、双荧光素酶系统应用的案例分享
经典案例1
文章标题:Nucleosome assembly protein-like 1 degradation-dependent novel cardioprotection mechanism of Wnt2 against ischemia-reperfusion injury
发表期刊:Signal Transduction and Targeted Therapy;
影响因子:52.7;
第一单位:上海心血管疾病研究所;
实验结果:双荧光素酶实验结果显示在缺氧/复氧(H/N)条件下,含氧化反应元件(ARE)启动子活性显著降低,而Wnt2处理显著增强ARE启动子的荧光素酶活性,表明Wnt2能够转录激活ARE依赖的抗氧化基因(如SOD1、SOD2、GPX1、UCP3),从而降低ROS水平、抑制细胞凋亡与铁死亡。这一机制揭示了Wnt2-Lrp6/Trim11-Nap1L1轴在调节氧化还原稳态中的关键作用,为缺血再灌注损伤的靶向治疗提供了新策略。
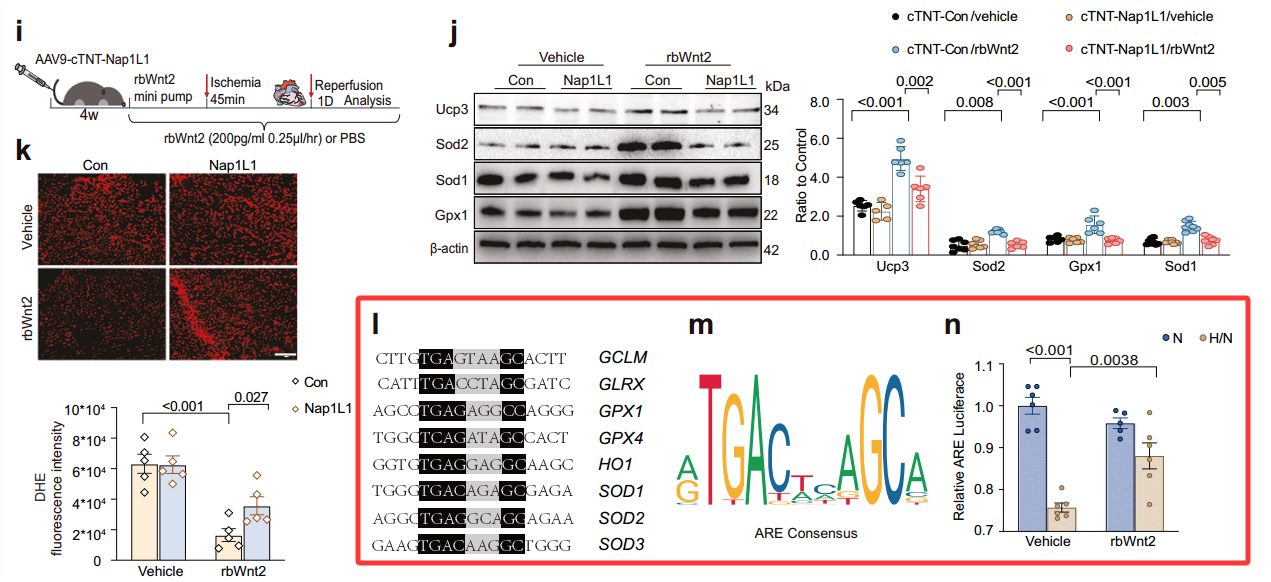
图7. pHBLuc-ARE双荧光素酶报告系统在文献中的应用(原文图5)[2]
经典案例2
文章标题:FGF4-FGFR1 signaling promotes podocyte survival and glomerular function to ameliorate diabetic kidney disease in male mice
发表期刊:Nature Communications;
影响因子:15.7;
第一单位:温州医科大学;
实验结果:双荧光素酶实验结果显示Tfcp2l1通过转录激活FGF4,进而调控FGF4/FGFR1/AMPK/FOXO1信号轴,抑制足细胞氧化应激与凋亡,保护肾小球功能。该机制阐明了FGF4在糖尿病肾病中的保护作用,并为开发基于FGF4信号通路的肾脏保护疗法提供了新的分子靶点与实验依据。

图8. Tfcp2l1调控FGF4表达研究中的双荧光素酶应用(原文补充图2)[3]
经典案例3
文章标题:Inhibition of CAV1 attenuates diabetic cardiomyopathy through reducing ferroptosis via activating NRF2/GCLC signaling pathway
发表期刊:Theranostics;
影响因子:13.3;
第一单位:南开大学;
实验结果:双荧光素酶实验证实NRF2通过转录激活 GCLC(谷氨酸半胱氨酸连接酶催化亚基),促进了抗氧化分子谷胱甘肽的合成,从而增强细胞的抗氧化防御能力,抑制心肌细胞的铁死亡。这阐明了在糖尿病心肌病(DCM)中,CAV1通过抑制NRF2的核转位及其下游GCLC的转录,导致抗氧化能力下降和铁死亡增加的核心分子机制,为靶向CAV1/NRF2/GCLC轴治疗DCM提供了关键的实验依据。
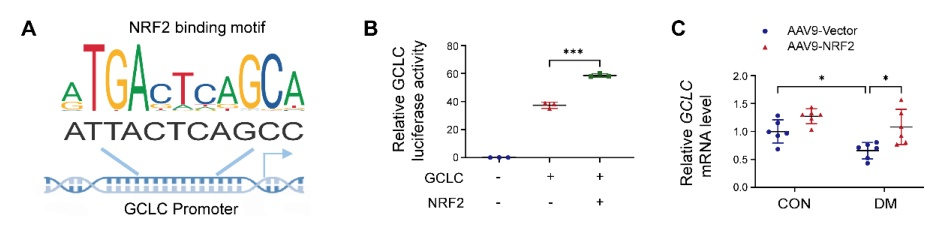
图9. NRF2调控GCLC表达研究中的双荧光素酶应用(原文图7)[4]
经典案例4
文章标题:CRSP8-driven fatty acid metabolism reprogramming enhances hepatocellular carcinoma progression by inhibiting RAN-mediated PPARα nucleus-cytoplasm shuttling
发表期刊:Journal of Experimental & Clinical Cancer Research;
影响因子:11.4;
第一单位:中山大学附属第三医院;
实验结果:双荧光素酶实验证实CRSP8通过转录激活RAN,进而促进RAN/CRM1/PPARα核质穿梭复合体的形成,最终抑制PPARα的核定位及其介导的脂噬和脂肪酸氧化功能。这一机制阐明了CRSP8如何通过调控脂肪酸代谢重编程促进肝细胞癌进展,并为针对CRSP8高表达肝癌的代谢靶向治疗提供了理论依据。
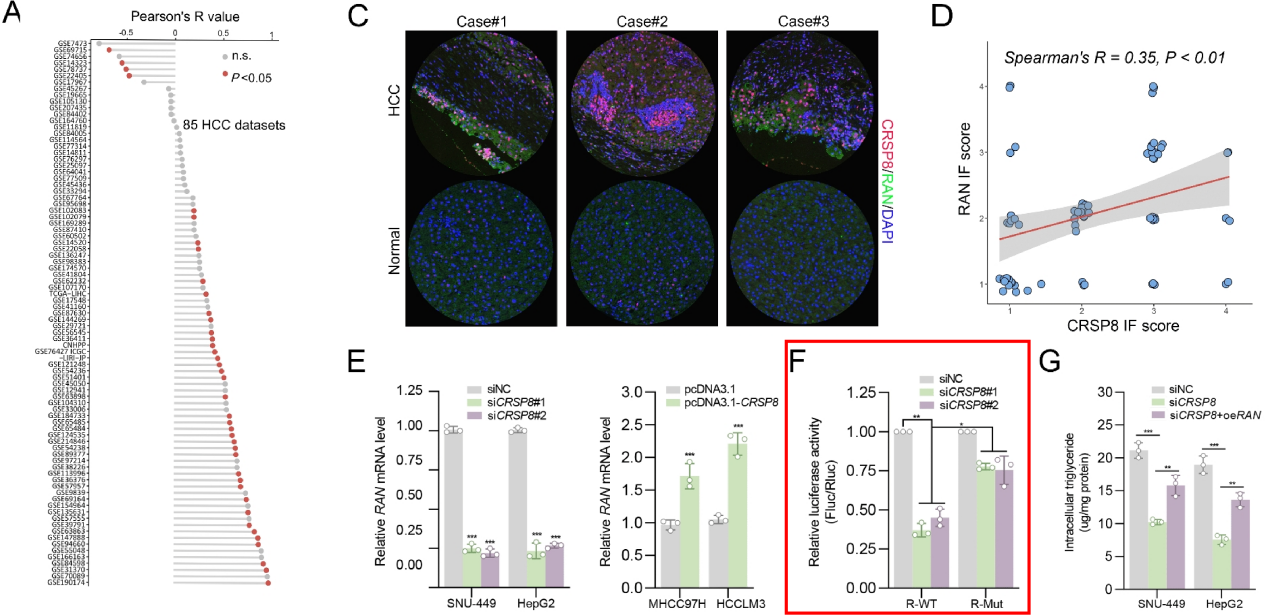
图10. CRSP8调控RAN表达研究中的双荧光素酶应用(原文图7)[5]
经典案例5
文章标题:Histidine triad nucleotide-binding protein 2 attenuates doxorubicin-induced cardiotoxicity through restoring lysosomal function and promoting autophagy in mice
发表期刊:MedComm;
影响因子:10.7;
第一单位:复旦大学附属中山医院;
实验结果:双荧光素酶实验直接证实了“HINT2→SREBF2→TFAM”这一转录调控轴的存在,阐明了HINT2通过调控SREBF2的转录功能影响下游线粒体基因的表达,进而维持NAD+/NADH平衡、溶酶体功能与自噬流,最终减轻阿霉素心脏毒性的分子机制。

图11. SREBF2调控TFAM表达研究中的双荧光素酶应用(原文图7)[6]
本期干货内容主要为大家介绍了双荧光素酶报告系统在转录因子与启动子互作验证、启动子活性验证和增强子/抑制子活性验证中的应用,包括实验原理及实验设计思路,并附上了经典的应用案例文献,希望对正在做这方面实验的小伙伴有所帮助,感兴趣的小伙伴可以持续关注留意一下哦~~~
参考文献:
[1] Carlberg C ,Molnár, Ferdinand.The Basal Transcriptional Machinery[M].Springer Netherlands,2014.
[2] Wang Y, Chen L, Lin J, Liu X, Jin K, Huang C, Wang H, Jia J, Wu J, Ding Z, Gao P, Ge J, Gong H, Zou Y. Nucleosome assembly protein-like 1 degradation-dependent novel cardioprotection mechanism of Wnt2 against ischemia‒reperfusion injury. Signal Transduct Target Ther. 2025 Dec 16;10(1):403.
[3] Zhou J, Wang S, Lou J, Pan B, Zhao M, Li Q, Zhou J, Du Y, Ding S, Yu M, Zhou J, Chen X, Jin L, Wang X, Hu Y, Wang Z, Li X, Zheng C, Sun J, Huang Z. FGF4-FGFR1 signaling promotes podocyte survival and glomerular function to ameliorate diabetic kidney disease in male mice. Nat Commun. 2025 Nov 25;16(1):10430.
[4] Li G, Liu R, Peng Z, Zhang S, Sun R, Wang Z, Li J, Gao Y, Xu Y, Cui J, Liu J, Yan J, Cao L, Ren S, Chu Y, Feng L, Yang L, Shen Y, Qi Z. Inhibition of CAV1 attenuates diabetic cardiomyopathy through reducing ferroptosis via activating NRF2/GCLC signaling pathway. Theranostics. 2025 Mar 31;15(11):4989-5006.
[5] Lin Y, Liang Z, Weng Z, Liu X, Zhang F, Chong Y. CRSP8-driven fatty acid metabolism reprogramming enhances hepatocellular carcinoma progression by inhibiting RAN-mediated PPARα nucleus-cytoplasm shuttling. J Exp Clin Cancer Res. 2025 Mar 11;44(1):93.
[6] Jiang H, Zhang J, Jia D, Liu L, Gao J, Zhang B, Dong Z, Sun X, Yang W, Ou T, Ding S, He L, Shi Y, Hu K, Sun A, Ge J. Histidine triad nucleotide-binding protein 2 attenuates doxorubicin-induced cardiotoxicity through restoring lysosomal function and promoting autophagy in mice. MedComm (2020). 2025 Feb 17;6(3):e70075.

查看更多

查看更多

查看更多

联系我们

返回顶部