查看更多

 明星产品
明星产品
 关注我们
关注我们

扫码关注我们
了解更多信息
在饥饿、压力或损伤的危机时刻,自噬可以精准地识别并回收自身受损的蛋白质、衰老的细胞器,将其降解为可循环利用的“原料”。这不仅是细胞应对压力因素的“生存策略”,更是维持细胞内部平衡的“清道夫”。本期我们就将从自噬的来源和发展、自噬的分类、自噬发生的过程及相关的基因家族、自噬的诱导方式和自噬的检测方式等五大方向认识自噬的研究方向和过程。

一、自噬的来源和发展
1963年,克里斯汀·德·迪夫首次提出了自噬(Autophagy)的概念,源自希腊语,“auto”意为自我,“phagy”意为进食,合并意为“自食”。它描述的是真核生物细胞内的一种现象:双层膜囊泡将细胞内的成分进行包裹,随后运输至溶酶体进行降解。1990年,日本学者大隅良典在酿酒酵母中展现了细胞自噬的过程,不仅发现了多个自噬的关键基因,还阐明了酵母中的自噬机制,并在人的细胞中也发现了类似的复杂机制。在2016年,大隅良典也因发现自噬机制的杰出贡献荣获了诺贝尔生理学或医学奖。自此,自噬研究已然成为生物学、医学、植物学和微生物学等领域的热门研究方向。
由于生物体在不断进行自我更新,细胞及其内部成分会不断地被重塑和循环利用。真核细胞有两种主要的降解系统,即溶酶体和蛋白酶体,而自噬的过程就是借助溶酶体系统[1]。
自噬包括生理条件下的基础型自噬和应激条件下的诱导型自噬。前者是细胞的自我保护,能够防止有毒蛋白质聚集物的积累、清除受损的细胞器,并为细胞和生物体提供生存所需的生物能量底物[2]。但自噬过度可能导致代谢应激、降解细胞成分,甚至引起细胞死亡等。而自噬作用的双面性也体现在疾病的发生发展过程中。例如,在肿瘤发生的早期阶段,自噬通过涉及质量控制系统和氧化应激反应的过程,帮助维持基因组完整性并抑制组织损伤和炎症,从而发挥肿瘤抑制作用。然而,在肿瘤发展的晚期,自噬为癌细胞提供营养并促进其免疫逃逸[3],因此,自噬也被称为细胞生存的“双刃剑”。
二、自噬的分类[1, 4]
每小时约有1 % ~ 1.5 %的蛋白质通过自噬过程被分解代谢,即便是在肝脏这种营养丰富的环境中亦是如此[1]。自噬是将细胞质物质送入溶酶体或液泡途径的统称。根据底物进入溶酶体途径的不同,自噬大致可分为三类:巨自噬、微自噬和伴侣介导的自噬,而将其分类细化又可分为16类自噬,我们来具体了解下自噬的分类。
1、巨自噬的分类
巨自噬(简称为“自噬”),需要借助中间细胞器“自噬体”。隔离膜将一小部分细胞质(包括可溶性物质和细胞器)隔离出来,形成自噬体。自噬体与溶酶体融合形成自噬溶酶体,并分解其中所包含的物质。巨自噬被认为是自噬的最主要类型,其研究最为深入广泛。
(1)批量自噬,是一种非选择性过程,靶向大量的大分子或亚细胞器。自噬体的形成依赖于LC3(微管相关蛋白1轻链3)的酯化修饰,LC3-I转化为LC3-II并锚定在自噬体膜上,细胞质物质被隔离到自噬体中,并输送到溶酶体进行降解。
大分子自噬:
(2)聚集体自噬,其中聚集的蛋白质被泛素化,并由泛素结合自噬受体(如 p62 或 NBR1)靶向,p62通过其LC3相互作用区域LIR与自噬体膜上的LC3结合,从而将蛋白聚集体包裹进自噬体进行降解;
(3)糖自噬,其中STBD1作为糖原自噬的受体,能够识别糖原并通过LIR与GABARAP结合,促进溶酶体内糖原通过GAA(酸性α-葡萄糖苷酶)等酶分解为非磷酸化葡萄糖;
(4)脂自噬,脂酶A等分子参与脂滴的分解,自噬体包裹脂滴后与溶酶体融合,溶酶体中的酶将脂滴分解为脂肪酸等小分子,转化为 ATP供细胞利用;
(5)颗粒自噬,其中应激颗粒(RNA和蛋白质)的隔离由Cdc48/VCP介导,使应激颗粒能够被输送至溶酶体进行降解。
细胞器自噬:
(6)线粒体自噬,受损线粒体的膜电位改变会触发自噬信号,通过被可溶性或膜结合的线粒体自噬受体结合,这些受体也能结LC3,导致线粒体被包裹进自噬体,并随后被输送至溶酶体进行降解;线粒体自噬的一种特殊形式一碎片状线粒体自噬,其机制是,线粒体部分通过外线粒体膜蛋白Metaxin-1(MTX1)结合LC3C,导致p62的募集和自噬体的形成;
(7)内质网自噬,位于内质网的不同部位特定的受体FAM134B、RTN3L、ATL3、SEC62、CCPG1和TEX264,通过结合LC3导致内质网被隔离进自噬体,并发生溶酶体降解;
(8)核自噬,核 LC3结合到lamin B1,形成小凸起,被切离到细胞质中进行自噬降解;
(9)溶酶体自噬,在溶酶体膜通透性增加时发生,可伴随或不伴随泛素化:galectin-3被募集到受损的溶酶体上,招募TRIM16和自噬蛋白(如ULK1和ATG16L1),溶酶体上的泛素化导致p62的募集,p62结合LC3以促进自噬过程;在泛素非依赖过程中,galectin-8(Gal-8)被募集到受损的溶酶体上,能够直接结合与LC3相互作用的NDP52受体,以继续自噬过程。
异体自噬
(10)细菌的DNA被cGAS(环鸟甘酸-腺苷酸合成酶)等检测到,cGAS 是一种通过Smurf1触发泛素化过程的传感器;随后NBR1受体附着在泛素链上,LC3 继续自噬过程以降解细菌;
(11)细菌损伤了自噬体的膜,暴露内部糖基,招募Gal-8,然后被NDP52识别以招募TBK1、LC3C、Nap和Sintbad;视神经蛋白、p62和NDP52受体与病原体上的泛素相互作用,招募自噬吞噬系统,吞噬的病原体随后被降解。
2、微自噬的分类
在微自噬过程中,溶酶体自身会通过溶酶体膜的向内折叠包裹细胞质中的小成分。微自噬过程中的膜动态变化可能与内吞作用所需转运复合物(ESCRT)依赖的多囊泡体(MVB)形成的内体分选过程的膜动态变化类似。在MVB形成过程中,大量或有选择性的细胞质蛋白质会被整合到内体腔中[5]。
(12)通过内体溶酶体膜的直接内陷来捕获细胞质成分;
(13)微-内质网自噬,使用SEC62受体,通过溶酶体的内陷来捕获和降解内质网;
(14)具有KFERQ五肽基序的蛋白质的内体微自噬,该过程需要HSC70分子伴侣。
3、伴侣介导的自噬的分类
第三种自噬类型是伴侣介导的自噬。这类自噬不涉及膜重组,在伴侣介导的自噬过程中,底物蛋白质可以直接穿过溶酶体膜。伴侣蛋白HSC70(热休克同源蛋白70)和伴随伴侣蛋白协同作用特异性地识别含有类似KFERQ五肽的蛋白[6]。而跨膜蛋白Lamp-2A是Lamp-2 的一种亚型,在溶酶体上起着受体的作用,未折叠的蛋白质则通过LAMP2A多聚体转运复合物被送入溶酶体内降解[1]。
(15)涉及 HSC70 和其他如 HSP40 的共分子伴侣通过靶向含有KFERQ五肽相关基序的蛋白质,并使底物通过LAMP2A受体进入溶酶体进行降解;
(16)以类似 CMA 的方式,DNA自噬/ RNA自噬的发生:核酸与 LAMP2C受体结合,允许核酸被溶酶体摄取。
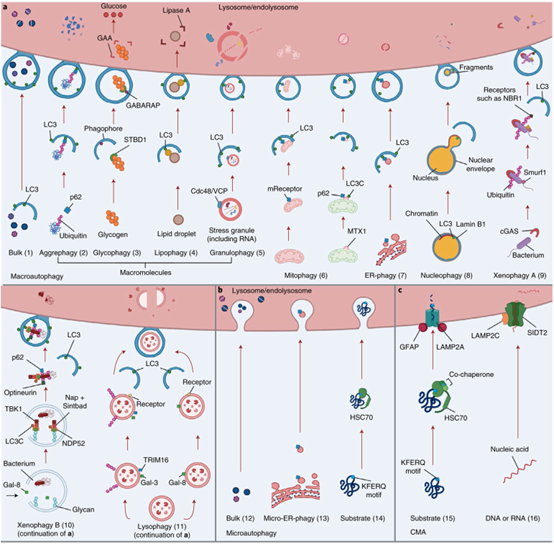
图1. 不同的自噬机制[4]
根据降解底物的选择性不同,自噬也可分为非选择性自噬和选择性自噬。非选择性自噬是不加选择地将细胞质成分或细胞器运送到溶酶体;选择性自噬是降解特定的靶点,如受损的细胞器、聚集蛋白或入侵细菌等。选择性自噬研究最为广泛的是细胞器自噬中的线粒体自噬和内质网自噬[1]。
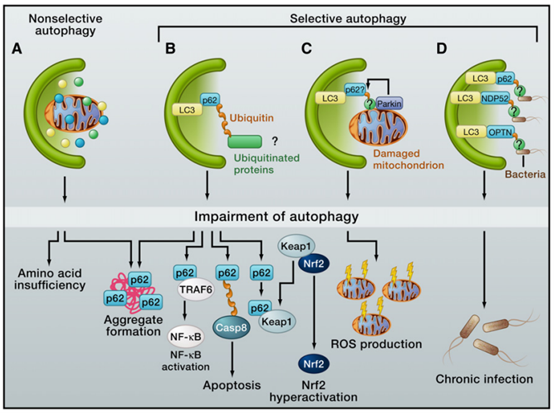
图2. 非选择性与选择性自噬[1]
三、自噬发生的过程及相关的基因家族
20世纪90年代大隅良典在酿酒酵母中发现自噬相关基因。2003年,丹尼尔·克利昂斯基等人将在自噬过程中起关键作用的基因统称为AuTophaGy(ATG)基因,并深入研究了这些基因所编码的蛋白质与自噬功能之间的相互关联。学者们也陆续通过基因筛选在酵母中鉴定出了40多个ATGs,其中约有一半的基因与哺乳动物的ATGs明显同源[3]。核心的ATG蛋白在其他真核生物(包括哺乳动物)中高度保守,并且在酵母和哺乳动物中以类似的层级方式发挥作用[7]。那我们就一起了解下自噬发生的过程及相关的基因家族和信号网络机制吧。
自噬是一个受复杂信号精细调控的生物学过程,自噬过程一般分为以下三个阶段:
自噬起始阶段:细胞接收到自噬诱导信号后,在胞浆内形成一个小的类似脂质体双分子层的扁平状膜结构。该结构可在电镜下观察到,被称为吞噬泡。吞噬泡随着自噬的发展过程不断扩张,是自噬发生的第一个铁证。
相关基因调控网络:在自噬诱导过程中,ULK1(Atg1 同源物)复合体(包括ULK1、Atg13、FIP200和Atg101)会被激活并转移到内质网的某一区域。一旦进入内质网,ULK1 复合体会调节III类磷脂酰肌醇(PtdIns)3-激酶(PtdIns3K)复合体(包括Beclin 1、Atg14(L) / barkor、Vps15、Vps34和Ambra1),这种调节受到RalB和含Exo84的外排体囊复合体的促进。Beclin 1被招募到PtdIns3K复合体中的过程也对饥饿条件敏感;在营养丰富的条件下,Beclin 1与内质网相关的Bcl-2形成复合物,并通过JNK1磷酸化Bcl-2后释放出来。Atg9L,一种多跨膜蛋白,也参与自噬体形成的早期阶段(Atg9L可能被招募到囊泡上)[1,8]。
自噬小体形成阶段:吞噬泡不断延伸,LC3B逐渐募集。随后,p62带着需要降解的细胞内容物结合上来,磷脂双层膜将胞浆中的细胞成分,包括细胞器,全部揽入膜结构中,然后“收口”,成为密闭的球状的autophagosome,即“自噬体”。电镜下观察到自噬体是自噬发生的第二个铁证。自噬体必须要有两个特征:一是双层膜,二是含有胞浆成分,如线粒体、内质网碎片等。
相关基因调控网络:PI3P复合体的形成会招募双FYVE含有蛋白1(DFCP1)并促进ω体(Omegaosome,是一种PI3P富集的动态膜结构,通常出现在自噬起始位点,被认为是自噬体形成的“摇篮”)的形成。其他与PI3P结合的WIPI蛋白(与Atg18同源)对于ω体/隔离膜的成熟也至关重要。Atg12–Atg5–Atg16L1 复合物以及LC3(与Atg8同源)–磷脂酰乙醇胺(PE)结合物在隔离膜的延伸和闭合过程中发挥着重要作用[1,8]。
自噬溶酶体阶段:自噬体与溶酶体融合形成自噬溶酶体。形成自噬溶酶体后,自噬体的内膜被溶酶体中的蛋白水解酶降解,两者的内容物合二为一。自噬小体中的细胞组分被降解之后,对机体有用的产物(如氨基酸、脂肪酸等)被输送到胞浆中,供细胞重新利用,而残渣或被排出细胞外或滞留在胞浆中。
相关基因调控网络:SNARE蛋白家族基因: STX17、SNAP29等介导自噬体与溶酶体的膜融合过程,是融合阶段的直接执行者。LAMP2A是CMA的受体,也参与溶酶体膜稳定性的维持。自噬体与溶酶体融合调控基因:如ATG7,可以影响后续与溶酶体的融合效率,ATG5和ATG12也参与自噬体膜延伸,间接影响融合。溶酶体酸化与水解酶基因:如VATPase亚基基因编码质子泵,维持溶酶体酸性环境。
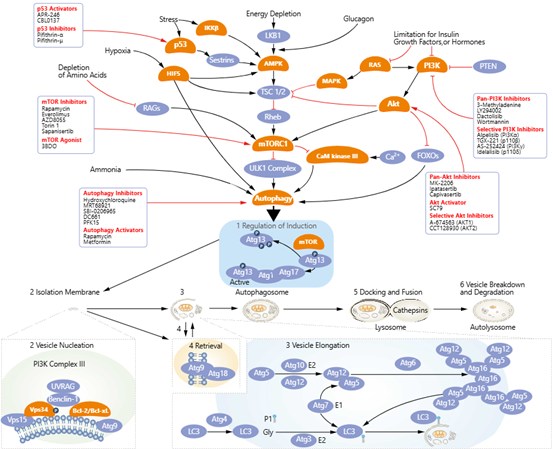
图3. 自噬信号通路图(来源于https://www.selleck.cn/pharmacological_autophagy.html)
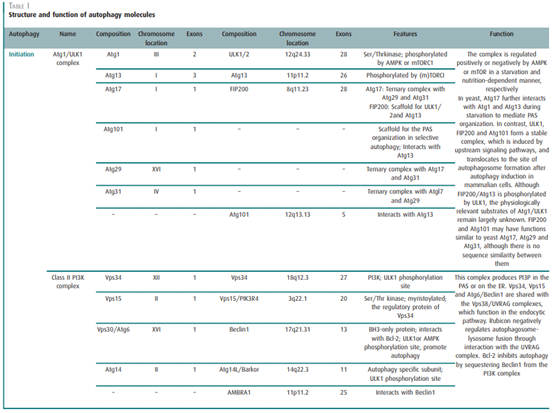
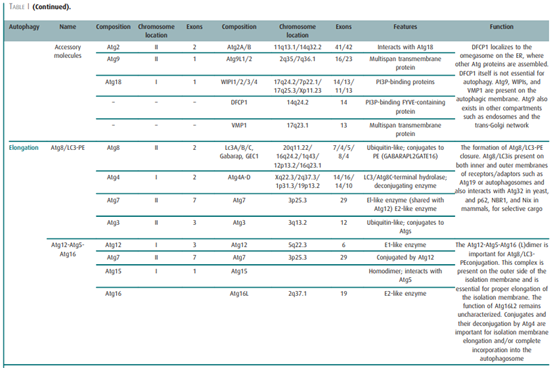
图4. 自噬分子的结构与功能[8]
四、自噬的诱导方式
怎么判断自噬是否参与了在研的某个表型?首先我们可以通过改变自噬的强弱来观测自噬与表型之间的正向或者反向关系,以此初步判断自噬与表型的相关性。在此我们介绍两种操控自噬的方法及常用药物,其他药物及压力因素见图5。
诱导自噬:利用饥饿培养(如EBSS饥饿培养基,不含有血清和氨基酸)来激活自噬流。EBSS处理细胞超过16 h可以有效激活自噬。类似的还有用mTOR抑制剂雷帕霉素(Rapamycin)及其类似物处理细胞,在1-20μM的浓度下处理2h可以有效诱导自噬。
抑制自噬:最常用的抑制剂是溶酶体抑制剂—氯喹(chloroquine diphosphate),通常使用浓度在30-100μM,处理时间为12-16 h。氯喹处理过的细胞由于溶酶体功能被抑制而无法正常降解溶酶体内容物,这会致使自噬流由于自噬溶酶体降解阻断而变相增强。类似的抑制晚期自噬进程的药物还有Bafilomycin A1、NH4Cl等,均可以抑制溶酶体对底物的降解,显著增加自噬囊泡的数量。需要说明的是,3-MA也属于常用自噬抑制药物,但其抑制的是自噬发生的较早期,会显著抑制自噬小体的形成。
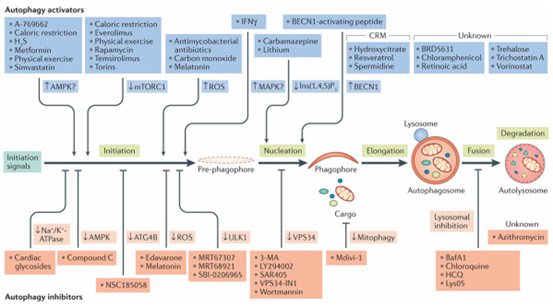
图5. 药物和干预措施调控自噬通路[9]
五、自噬的检测方式
在明白如何切入自噬研究方向之后,我们还需要知晓有哪些“标准”能够证明自噬的发生。即如何衡量研究细胞内(比如药物或基因干预细胞系/原代细胞,甚至动物个体组织/脏器)是否发生了自噬、以及自噬流的强弱变化。在此,我们称之为自噬研究的“黄金标准”。这些“黄金标准”指标具体如下:
大自噬——利用Western Blot检测LC3剪切的变化;LC3存在LC3-I和LC3-II两种形式。LC3-I存在于胞浆里,而LC3-II会和自噬体膜相结合。当自噬被激活时,LC3-I会经过加工变成LC3-II,LC3-II量和自噬体数量呈正相关。所以,检测LC3-II/LC3-I的比值,可以评估自噬水平的高低。
大自噬——电镜直接观察自噬囊泡;自噬体属于亚细胞结构,直接借助透射电镜观察自噬不同阶段的形态变化是最直接的方法。不同时期的自噬体形态有明显的区别,自噬初期的隔离膜:新月状或杯状,双层或多层膜,有包绕胞浆成分的趋势;自噬中期的自噬小体:双层或多层膜的液泡状结构,内含胞浆成分等;自噬后期的自噬溶酶体:单层膜,胞浆成分已降解。
大自噬——荧光蛋白标记的LC3监测自噬流;mCherry-EGFP-LC3,mCherry用于标记与追踪LC3,EGFP的减弱可指示溶酶体与自噬小体的融合形成自噬溶酶体(即由于EGFP对酸性敏感),当自噬体与溶酶体融合后EGFP荧光发生淬灭,此时只能检测到红色荧光。这种串联的荧光蛋白表达载体系统直观清晰的指示了细胞自噬流的水平。
细胞器自噬——细胞器定位肽融合荧光,通过观察荧光的变化监测自噬流。
分子伴侣介导的自噬——借助分子伴侣所识别的底物基序KFERQ与mCherry或eRFP红光直接融合,开发出了KFERQ-mCherry / KFERQ-eRFP 探针,使其转化为CMA底物,在自噬初期CMA底物靶向溶酶体时,便可通过观察红色荧光斑点数量来检测活细胞中的CMA活性。
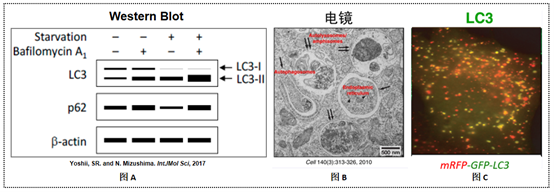
图6.衡量大自噬的三个“黄金标准”[10-11]
LC3剪切修饰(图A)、电镜观察自噬体(图B)、荧光蛋白标记的LC3监测自噬流(图C)。
汉恒生物专营病毒包装十余载,建立了庞大的基因研究现货工具库,现可提供自噬家族基因研究相关产品,包括慢病毒(Lentivirus, LV)、腺病毒(Adenovirus, AD)、腺相关病毒(Adeno-associated-virus, AAV)等,自噬现货详情见表1-5。如有技术或产品需求,欢迎随时咨询汉恒生物微信公众号或拨打官网技术服务热线:400-092-0065。本期内容到这里就结束了,下期我们将会继续分享细胞自噬相关的基因家族,敬请关注。
表1. LC3病毒现货
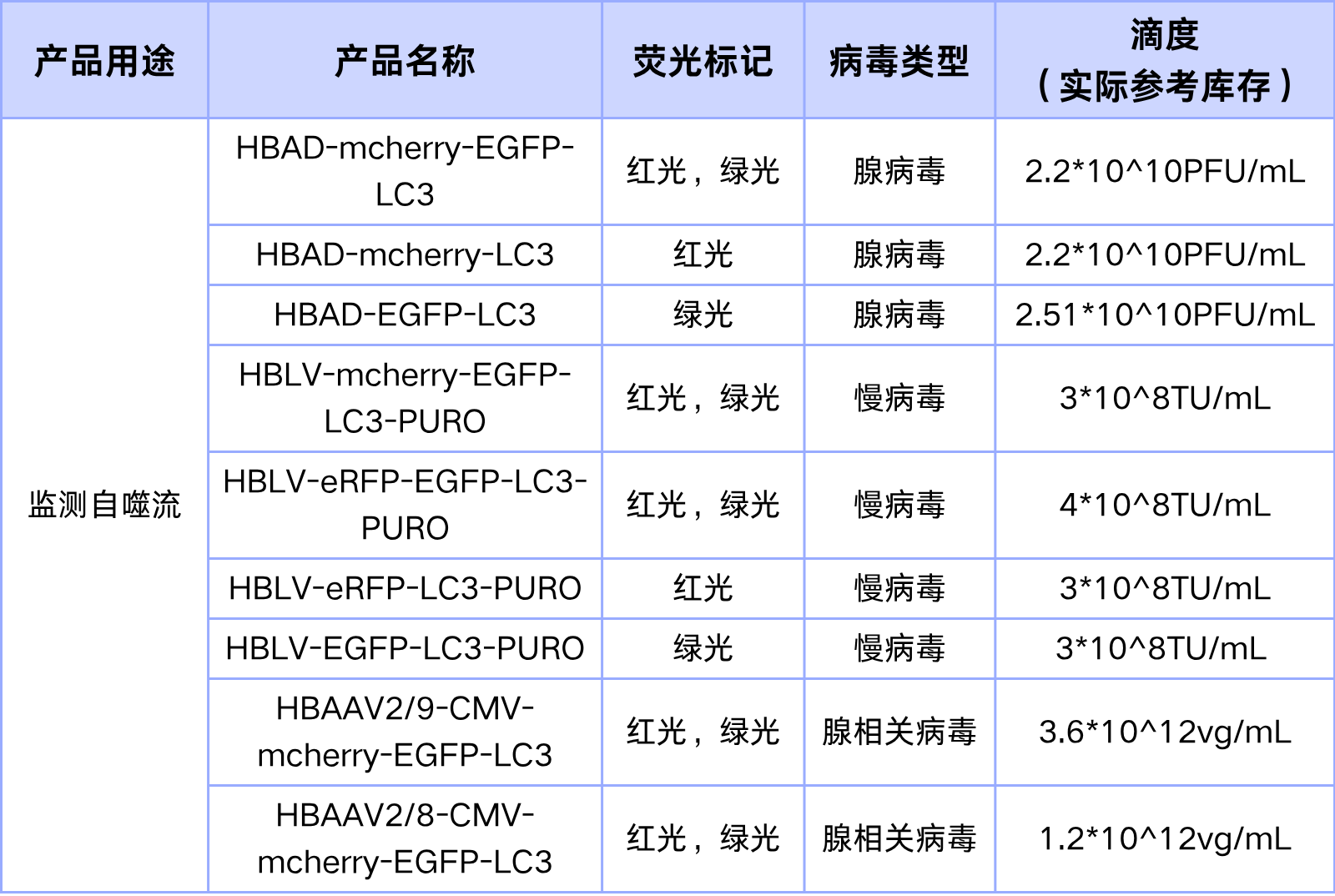
表2. 线粒体自噬病毒现货
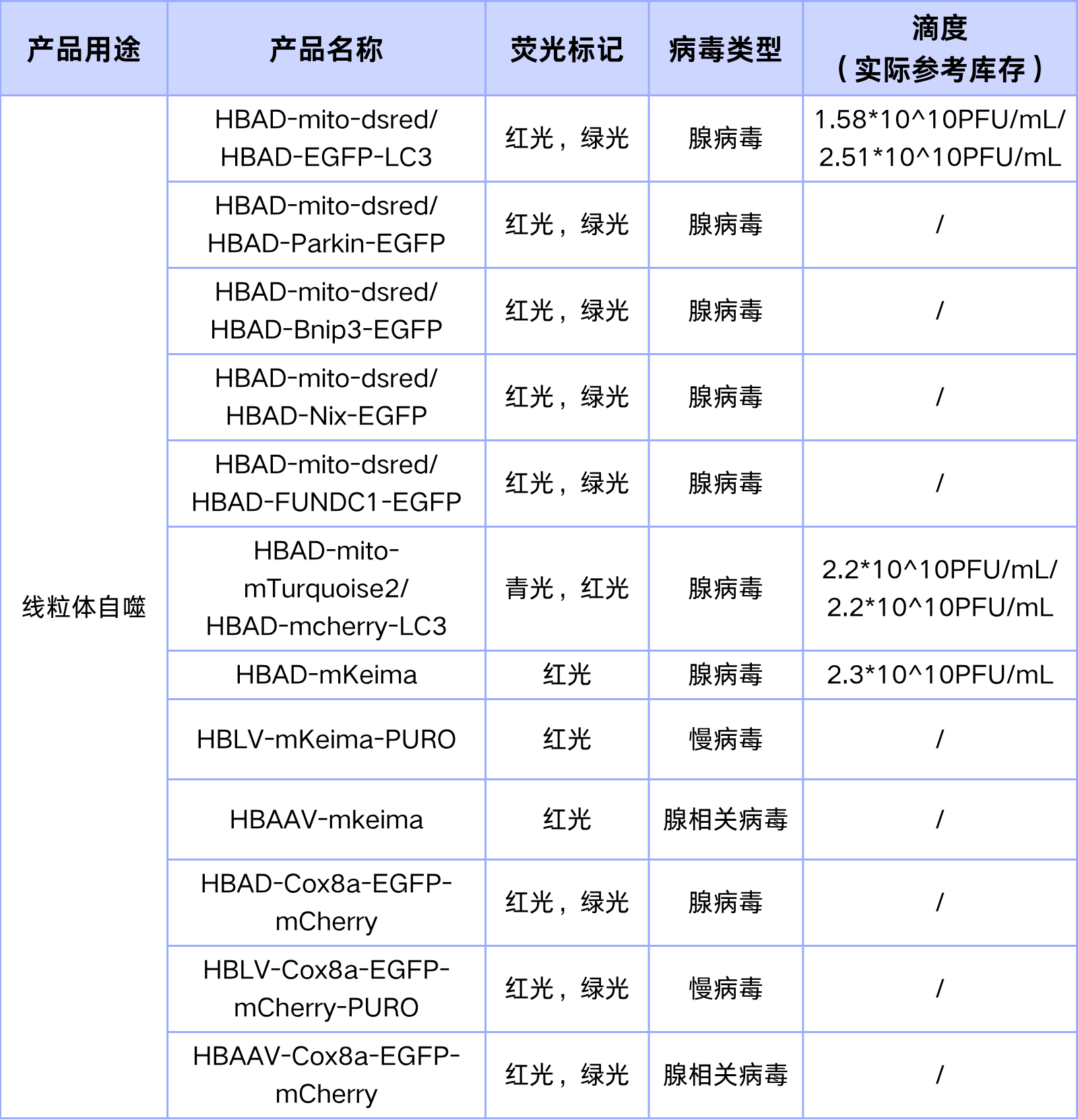
表3. 内质网自噬病毒现货
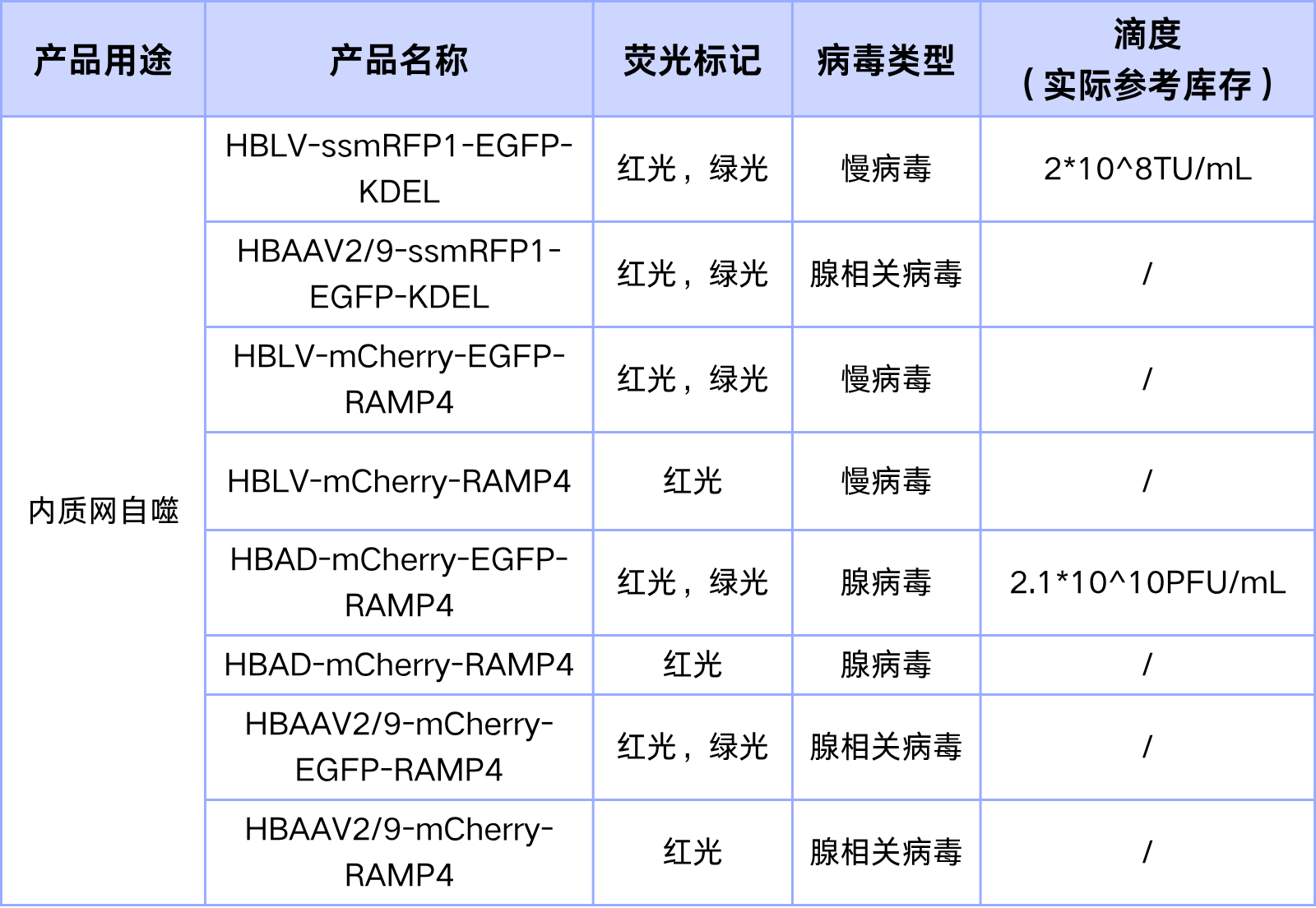
表4. 分子伴侣介导自噬病毒现货
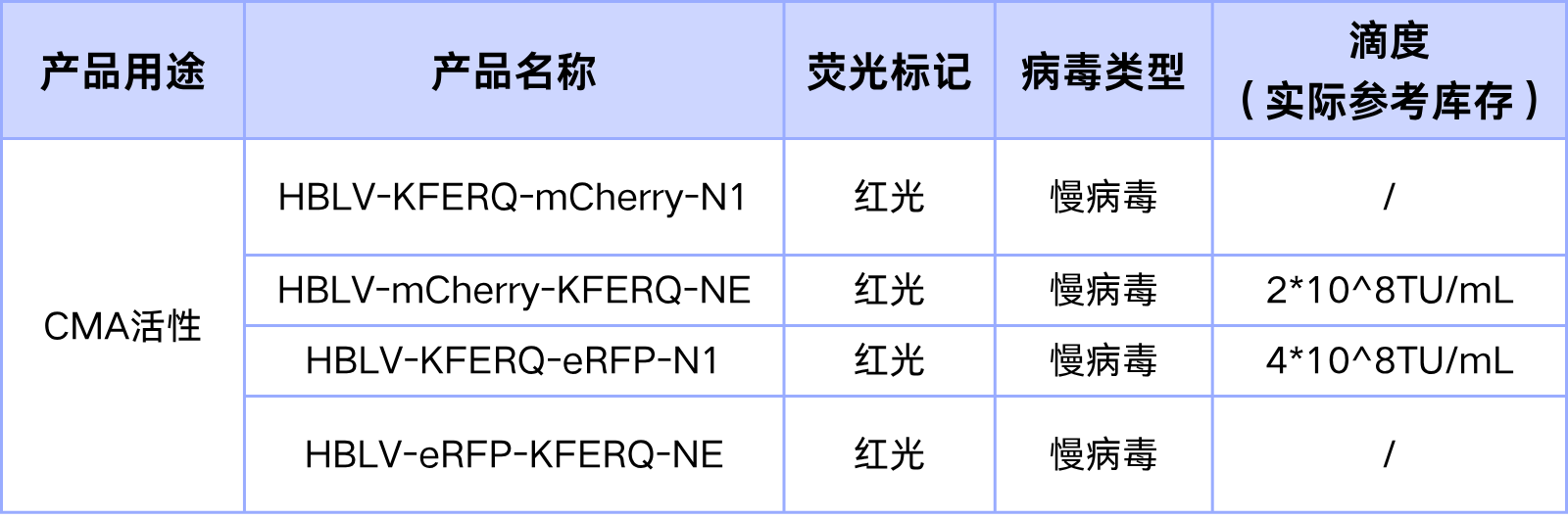
表5. 自噬相关基因病毒现货列表
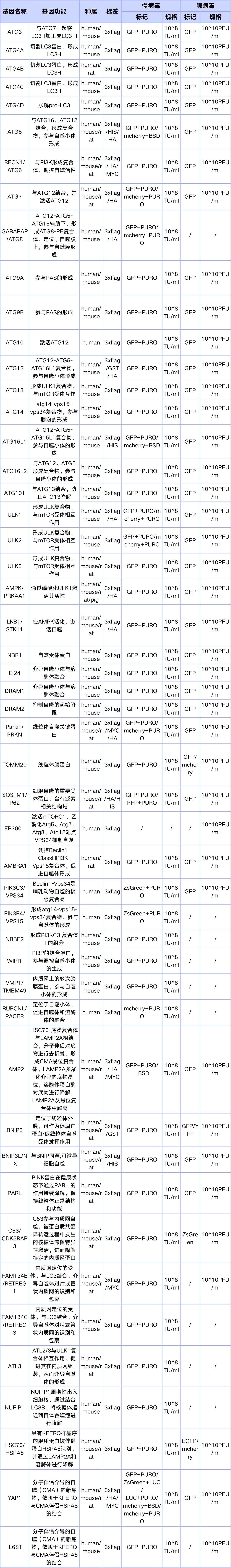
参考文献:
[1] Mizushima N, Komatsu M. Autophagy: renovation of cells and tissues. Cell. 2011 Nov 11;147(4):728-41. doi: 10.1016/j.cell.2011.10.026. PMID: 22078875.
[2] Doherty J, Baehrecke EH. Life, death and autophagy. Nat Cell Biol. 2018 Oct;20(10):1110-1117. doi: 10.1038/s41556-018-0201-5. Epub 2018 Sep 17. PMID: 30224761; PMCID: PMC9721133.
[3] Liu S, Yao S, Yang H, Liu S, Wang Y. Autophagy: Regulator of cell death. Cell Death Dis. 2023 Oct 4;14(10):648. doi: 10.1038/s41419-023-06154-8. PMID: 37794028; PMCID: PMC10551038.
[4] Aman Y, Schmauck-Medina T, Hansen M, Morimoto RI, Simon AK, Bjedov I, Palikaras K, Simonsen A, Johansen T, Tavernarakis N, Rubinsztein DC, Partridge L, Kroemer G, Labbadia J, Fang EF. Autophagy in healthy aging and disease. Nat Aging. 2021 Aug;1(8):634-650. doi: 10.1038/s43587-021-00098-4. Epub 2021 Aug 12. PMID: 34901876; PMCID: PMC8659158.
[5] Sahu R, Kaushik S, Clement CC, Cannizzo ES, Scharf B, Follenzi A, Potolicchio I, Nieves E, Cuervo AM, Santambrogio L. Microautophagy of cytosolic proteins by late endosomes. Dev Cell. 2011 Jan 18;20(1):131-9. doi: 10.1016/j.devcel.2010.12.003. Erratum in: Dev Cell. 2011 Mar 15;20(3):405-6. PMID: 21238931; PMCID: PMC3025279.
[6] Orenstein SJ, Cuervo AM. Chaperone-mediated autophagy: molecular mechanisms and physiological relevance. Semin Cell Dev Biol. 2010 Sep;21(7):719-26. doi: 10.1016/j.semcdb.2010.02.005. Epub 2010 Feb 20. PMID: 20176123; PMCID: PMC2914824.
[7] Itakura E, Mizushima N. Characterization of autophagosome formation site by a hierarchical analysis of mammalian Atg proteins. Autophagy. 2010 Aug;6(6):764-76. doi: 10.4161/auto.6.6.12709. PMID: 20639694; PMCID: PMC3321844.
[8] Cao W, Li J, Yang K, Cao D. An overview of autophagy: Mechanism, regulation and research progress. Bull Cancer. 2021 Mar;108(3):304-322. doi: 10.1016/j.bulcan.2020.11.004. Epub 2021 Jan 8. PMID: 33423775.
[9] Galluzzi L, Bravo-San Pedro JM, Levine B, Green DR, Kroemer G. Pharmacological modulation of autophagy: therapeutic potential and persisting obstacles. Nat Rev Drug Discov. 2017 Jul;16(7):487-511. doi: 10.1038/nrd.2017.22. Epub 2017 May 19. PMID: 28529316; PMCID: PMC5713640.
[10] Yoshii SR, Mizushima N. Monitoring and Measuring Autophagy. Int J Mol Sci. 2017 Aug 28;18(9):1865. doi: 10.3390/ijms18091865. PMID: 28846632; PMCID: PMC5618514.
[11] Mizushima N, Yoshimori T, Levine B. Methods in mammalian autophagy research. Cell. 2010 Feb 5;140(3):313-26. doi: 10.1016/j.cell.2010.01.028. PMID: 20144757; PMCID: PMC2852113.

查看更多

查看更多

查看更多

联系我们

返回顶部