查看更多

 明星产品
明星产品
 关注我们
关注我们

扫码关注我们
了解更多信息
自噬是真核细胞中高度保守的稳态调控机制,通过降解胞内受损组分(如细胞器、错误折叠蛋白及代谢废物等),实现营养物质的循环利用与细胞存活调控。在上一期内容中,我们从自噬的起源、分类、相关基因、诱导方式及检测手段等方面,系统介绍了自噬的核心概念与研究方法。在自噬过程中,吞噬泡的形成、延伸、成熟及其与溶酶体的融合,需要一系列自噬相关蛋白(ATG)的协同作用。其中,WD重复域磷脂相互作用蛋白(WD-repeat protein Interacting with PhosphoInositides,WIPI)家族作为关键效应分子,凭借其磷脂结合能力介导蛋白复合物的组装与膜转运,成为连接自噬信号通路与膜动力学的重要枢纽。本期将重点介绍WIPI家族基因的功能与调控机制。

WIPI家族基因的核心特征与分类[1,2,3]
WIPI家族蛋白属于PROPPIN(β-螺旋桨结合多磷酸肌醇)家族成员,该家族蛋白在自噬与膜转运过程中发挥核心调控作用,能够特异性识别并结合磷脂酰肌醇磷酸(PtdInsP),从而锚定于细胞内膜系统,并招募下游效应分子。在哺乳动物中,WIPI家族包含4个旁系同源基因(WIPI1/ATG18A、WIPI2、WIPI3/WDR45B、WIPI4/WDR45),各成员均具有由WD40重复序列构成的7叶β-螺旋桨结构,该结构为其执行蛋白-蛋白和蛋白-脂质相互作用提供了稳定的结构平台。
在结构上,WIPI蛋白的β-螺旋桨第5至第6叶之间含有一个保守的FRRG/LRRG基序,是该家族特异性结合PtdInsP的关键结构域,决定了其在细胞内膜系统中的定位特性,并参与自噬、内体再循环及高尔基体相关膜转运等多种生理过程。此外,部分WIPI成员因可变剪接产生多种亚型,其结构差异影响功能特异性和组织表达模式。
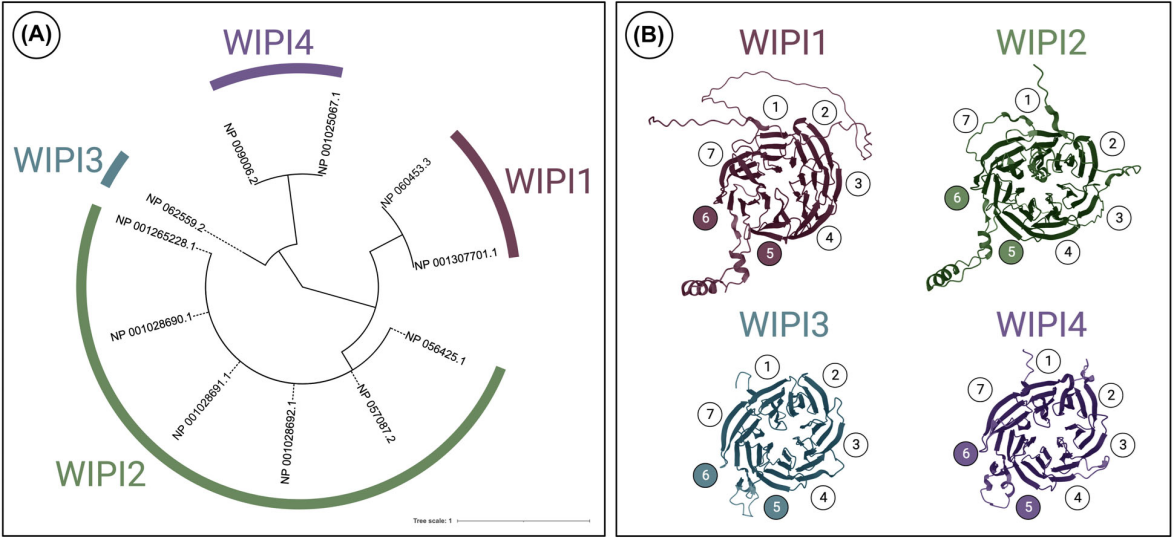
图1. 人源WIPI基因的β-螺旋桨结构[2]
>WIPI家族基因在真核生物中高度保守,进化上可分为两个旁系同源亚组,其进化差异决定了功能的分化。亚组1包含WIPI1与WIPI2,同源于酵母中的Atg18与Atg21,核心功能是参与经典自噬过程,介导吞噬泡的延伸与成熟;亚组2包含WIPI3(WDR45B)与WIPI4(WDR45),同源于酵母中的Hsv2,更侧重于调控非经典自噬、高尔基体相关膜降解及神经元特异性膜转运过程。这种进化上的分化的使得WIPI家族能够协同调控细胞内多种膜相关生理过程,维持细胞稳态。
WIPI家族各成员的功能及作用机制[3]
WIPI1(ATG18A)
WIPI1是WIPI家族中最早被鉴定的成员,其核心功能依赖于与PtdIns(3)P、PtdIns(3,5)P2的特异性结合,进而定位于细胞内的吞噬泡和内体膜上。与WIPI2不同,WIPI1并非基础自噬过程所必需,但可通过调控自噬通量参与自噬过程的精细调控,尤其在营养充足或自噬被轻度激活的状态下,其作用更为显著。
在非自噬膜转运过程中,WIPI1参与内体再循环通路,尤其在转铁蛋白受体的回收过程中发挥重要作用,通过介导内体膜的裂变与融合,维持细胞内铁离子的稳态平衡。此外,WIPI1还可与Retromer复合物相互作用,参与溶酶体相关膜蛋白的回收与转运,维持溶酶体的正常功能。从调控机制来看,WIPI1的活性受PI3K-III复合物的调控,其磷酸化修饰可影响其与磷脂的结合能力及细胞内定位,进而调控其功能的发挥。
WIPI2(ATG18B)
WIPI2是WIPI家族中唯一被证实为自噬必需的分子,其功能贯穿于经典自噬过程的多个关键环节,尤其在吞噬泡的延伸、自噬体的形成过程中发挥核心作用。WIPI2通过其β-螺旋桨结构中的FRRG基序结合PtdIns(3)P,定位于吞噬泡膜上,随后与ATG2蛋白形成稳定的复合物,该复合物是吞噬泡膜延伸与脂质转运的关键载体。
近年来的研究进一步揭示了WIPI2的作用机制,WIPI2的主要亚型WIPI2b可通过双结合位点模式招募并激活ATG12-ATG5-ATG16L1复合物,其中ATG16L1的卷曲螺旋结构域上存在两个WIPI2b结合位点(WBS1、WBS2),二者竞争结合WIPI2b的同一口袋,但可形成2:4的化学剂量比复合物,其中WBS2位点在酵母和哺乳动物中高度保守,是自噬正常进行所不可或缺的,而WBS1位点仅存在于哺乳动物中,可进一步促进自噬通量的提升。
在非自噬功能方面,WIPI2参与内体-质膜的回收过程,尤其在整合素β1的循环转运中发挥重要作用,通过调控整合素β1在细胞膜上的表达水平,影响细胞的黏附与迁移能力。
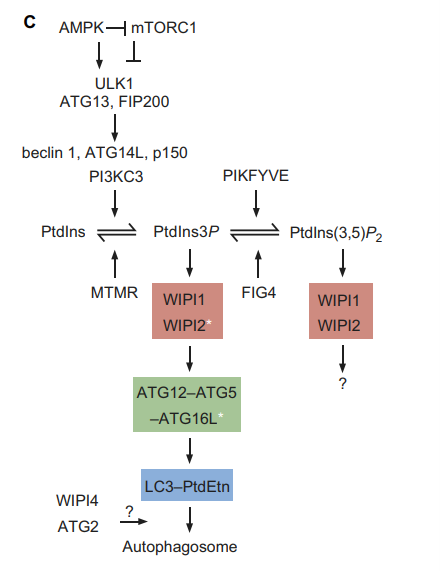
图2. WIPI基因在自噬溶酶体形成中的功能[3]
WIPI3(WDR45B)
WIPI3属于WIPI家族亚组2,同源于酵母中的Hsv2,其核心功能侧重于非经典自噬及高尔基体相关膜过程的调控。WIPI3在正常人体组织中广泛表达,初始的表达分析发现,其在卵巢癌、子宫癌和肾癌中存在异常表达,提示其可能和肿瘤的发生发展密切相关。
WIPI3的核心功能之一是参与高尔基体膜相关降解通路,该通路是一种非经典自噬相关的膜降解途径,通过从高尔基体生成自噬相关结构,介导高尔基体来源的异常蛋白或膜结构的降解。此外,WIPI3还可调控神经元轴突的生长与延伸,通过与细胞骨架相关蛋白的相互作用,介导轴突膜的转运与重塑,维持神经元的正常形态与功能。从调控机制来看,WIPI3可与WIPI4协同作用,共同参与神经元特异性的膜转运过程,其活性可能受磷酸化修饰的调控,但具体调控机制尚未完全阐明。
WIPI4(WDR45)[3,6,7]
WIPI4与WIPI3同属亚组2,是X连锁编码蛋白,其核心功能与自噬过程的成熟阶段及神经元稳态调控密切相关。WIPI4可通过结合PtdIns(3)P定位于吞噬泡膜上,参与吞噬泡的成熟与溶酶体的融合过程。近年来的研究发现,WIPI4可与ATG2A相互作用,通过稳定ATG2A在自噬体膜上的定位,协助ATG2A介导内体与自噬体之间的脂质转运,促进自噬体的膜延伸与闭合,这一过程需ANKFY1的协助,ANKFY1可通过其FYVE结构域结合富含PtdIns(3)P的脂质体,帮助ATG2A锚定在膜表面,进而增强WIPI4与ATG2A的协同作用。
由于WIPI4在神经元中特异性高表达,其功能异常对神经系统的影响尤为显著。WIPI4可调控神经元的突触功能与轴突稳态,通过参与突触囊泡的转运与回收,维持突触传递的正常进行,其表达异常可导致突触功能障碍,进而引发神经元损伤。此外,WIPI4还参与线粒体自噬过程,通过介导受损线粒体的识别与降解,维持神经元内线粒体的稳态,减少活性氧的积累,避免神经元凋亡。
WIPI4是目前WIPI家族中与疾病关联最为明确的成员,其X连锁显性突变可导致BPAN(β-螺旋桨蛋白相关神经退行性变),该疾病是一种进行性神经退行性疾病,儿童期主要表现为发育迟缓、运动障碍、癫痫,成年后逐渐进展为帕金森样症状,其发病机制主要与WIPI4突变导致的自噬障碍、神经元凋亡有关。此外,WIPI4的表达异常还与阿尔茨海默病、帕金森病等其他神经退行性疾病相关,推测其可能通过调控自噬通量,影响异常蛋白的聚集与降解,进而参与疾病的发病过程。
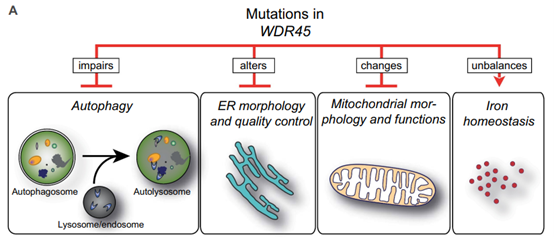
图3. WIPI4基因突变对细胞功能的影响[7]
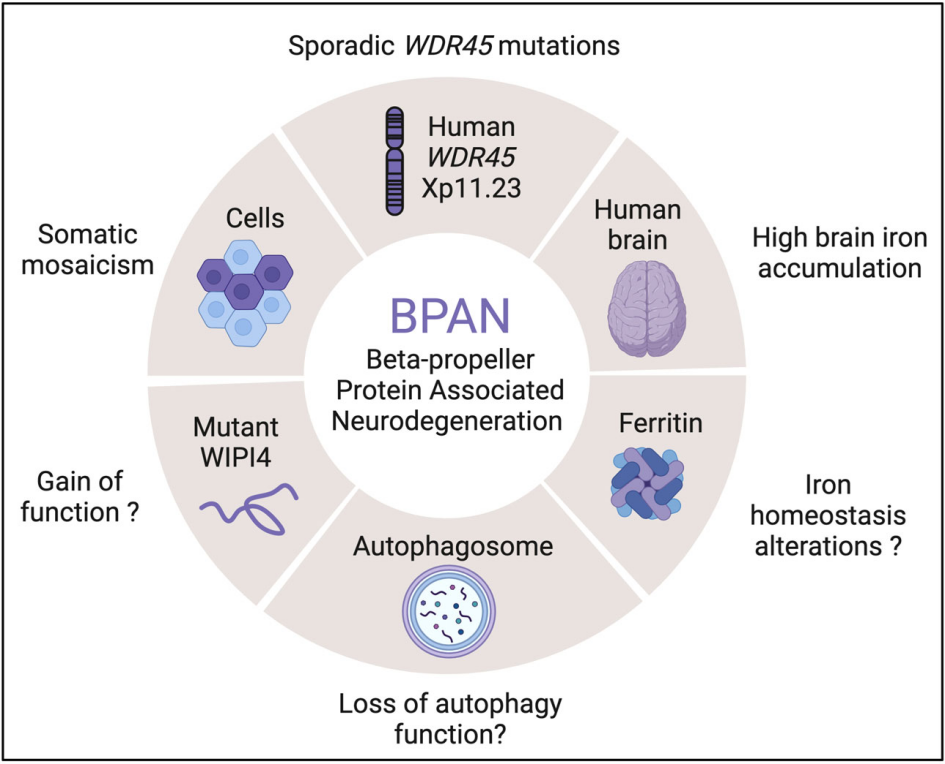
图4. WIPI4基因突变与BPAN的关系[2]
WIPI家族基因的共同作用机制与调控网络
自噬核心通路中的协同作用[4,5]
WIPI家族4个成员虽功能存在分化,但在自噬过程中形成协同调控网络,其核心共性是通过与磷脂酰肌醇磷酸的特异性结合,实现细胞内的膜定位,进而介导自噬相关蛋白复合物的组装与功能发挥。在经典自噬过程中,PI3K-III复合物激活后产生PtdIns(3)P,WIPI2首先结合PtdIns(3)P定位于吞噬泡膜上,与ATG2形成复合物,介导吞噬泡膜的延伸与脂质转运;随后WIPI2招募ATG16L1复合物,促进ATG8-PE偶联,推动自噬体的形成与成熟。
WIPI1虽非自噬必需,但可通过调控自噬通量,协同WIPI2维持自噬过程的稳定;WIPI4则主要参与吞噬泡的成熟与溶酶体的融合,通过与ATG2A、ANKFY1的协同作用,促进自噬体膜的延伸与闭合,确保自噬底物的有效降解;WIPI3则通过高尔基体膜相关降解通路,从高尔基体生成自噬相关结构,为自噬过程提供膜来源,尤其在经典自噬受抑制时,其非经典自噬调控作用更为显著。
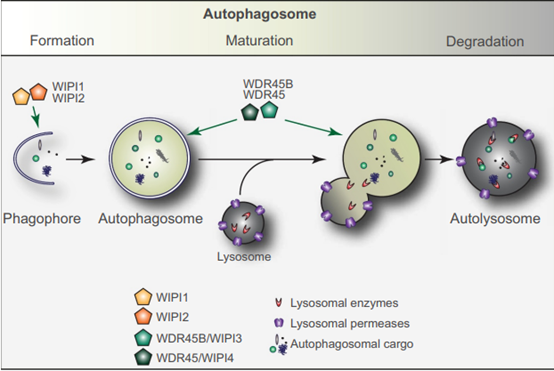
图5. WIPI蛋白在自噬中的作用[7]
非自噬膜转运过程中的协同作用[4,5]
除自噬通路外,WIPI家族成员还广泛参与细胞内的非自噬膜转运过程,形成协同调控网络,维持细胞内的膜稳态与信号传导。WIPI1主要参与内体再循环与Retromer介导的膜转运,WIPI2参与内体-质膜的回收过程,二者协同维持内体系统的正常功能;WIPI3与WIPI4则主要参与高尔基体相关膜转运与神经元特异性膜过程,二者协同调控神经元轴突生长与突触功能,维持神经系统的正常发育与稳态。
整体调控网络
WIPI家族基因的功能发挥受多种信号通路与修饰方式的调控,形成复杂的调控网络。从上游调控来看,PI3K-III复合物是核心调控因子,其激活后产生的PtdIns(3)P可介导所有WIPI家族成员的膜定位,进而激活其功能;此外,P38-ULK1-PI4KB轴可通过调控PtdIns(4)P的产生,影响WIPI2在非经典自噬中的功能发挥,尤其在RAS突变肿瘤中,这一调控轴的异常激活是导致非经典自噬紊乱的关键原因。在蛋白修饰层面,磷酸化、泛素化是调控WIPI家族成员活性的主要方式,例如,WIPI1的Ser395位点磷酸化可增强其与PtdIns(3)P的结合能力,促进其在吞噬泡上的定位;而WIPI4的泛素化修饰可介导其自身降解,进而调控自噬通量的动态平衡。
此外,WIPI家族成员还可与多种调控因子形成相互作用网络,例如,WIPI2可与Beclin1、Vps34等PI3K-III复合物成员相互作用,促进PI3K-III复合物的激活与膜定位;WIPI4可与转录因子EB(TFEB)相互作用,TFEB作为自噬与溶酶体生物发生的核心调控因子,可通过调控WIPI4的转录表达,形成负反馈调控回路,维持自噬过程的稳态。同时,miRNA也参与WIPI家族基因的转录后调控,如miR-18a-5p可靶向抑制WIPI2的表达,减少自噬体的形成,进而促进肿瘤细胞的增殖与转移;miR-34a可调控WIPI4的表达,参与神经元凋亡的调控,其表达异常与神经退行性疾病密切相关。
近年来,随着基因编辑与蛋白结构解析等技术的发展,WIPI家族基因的功能研究持续深入。现有研究表明,WIPI不仅是自噬通路中的必需调控因子,还广泛参与内体再循环、受体回收、神经元发育等非自噬性生理过程,该家族基因的变异与多种遗传性疾病及肿瘤预后密切相关。未来,仍需深入解析WIPI家族的分子机制与调控网络,明确各成员及其亚型的功能特异性,揭示其在疾病中的致病机制,推动相关生物标志物与治疗药物的研发。
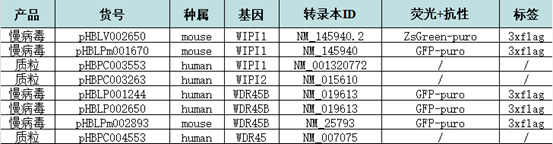
汉恒生物专营病毒包装十余载,建立了庞大的基因研究现货工具库,现可提供WIPI相关基因的表达调控工具(见表1),也可定制靶向特异性组织或细胞的基因调控工具,包括慢病毒(Lentivirus, LV)、腺病毒(Adenovirus, AD)、腺相关病毒(Adeno-associated-virus, AAV)以及质粒等,如有技术或产品需求,欢迎随时咨询汉恒生物微信公众号或拨打官网技术服务热线:400-092-0065。本期内容到这里就结束了,下期我们将会继续分享自噬相关的基因家族,敬请关注。
表1. 汉恒生物WIPI家族基因现货
参考文献:
[1] Almannai M, Marafi D, El-Hattab A W. WIPI proteins: Biological functions and related syndromes[J]. Frontiers in Molecular Neuroscience, 2022,15:1011918.
[2] Proikas-Cezanne T, Haas M L, Pastor-Maldonado C J, et al. Human WIPI β-propeller function in autophagy and neurodegeneration[J]. FEBS Letters, 2024, 598:127-139.
[3] Proikas-Cezanne T, Takacs Z, Do¨nnes P, et al. WIPI proteins: essential PtdIns3P effectors at the nascent autophagosome[J]. Journal of Cell Science, 2015, 128(1):1-11.
[4] Müller A J, Proikas-Cezanne T. Function of human WIPI proteins in autophagosomal rejuvenation of endomembranes[J]. FEBS Letters, 2015, 589:1546-1551.
[5] Shimizu T, Tamura N, Nishimura T, et al. Comprehensive analysis of autophagic functions of WIPI family proteins and their implications for the pathogenesis of β-propeller associated neurodegeneration[J]. Human Molecular Genetics,2023,32(16):2623-2637.
[6] Nakashima M, Takano K, Tsuyusaki Y, et al. WDR45 mutations in three male patients with West syndrome [J]. Journal of Human Genetics, 2016:1-9.
[7] Cong, Y., So, V., Tijssen, M. A. J., Verbeek, D. S., Reggiori, F., & Mauthe, M. (2021). WDR45, one gene associated with multiple neurodevelopmental disorders. Autophagy, 17(12), 3908–3923.

查看更多

查看更多

查看更多

联系我们

返回顶部