查看更多

 明星产品
明星产品
 关注我们
关注我们

扫码关注我们
了解更多信息
在前几期的干货中,小恒主要为大家介绍了自噬通路中及WIPI家族基因,这个家族基因隶属于大名鼎鼎的ATG家族。而ATG家族的其他成员们在自噬通路中又扮演了什么角色呢?在接下来的两期,我们将为大家介绍这一庞大家族在细胞自噬中的功能与机制。

一、ATG的发现与功能
自噬过程由一系列进化保守的基因介导,这些基因被统称为自噬相关基因(Autophagy-related gene, ATG)。上世纪90年代,大隅良典实验室利用酵母作为模式生物,通过在营养饥饿条件下进行系统的遗传筛选,首次鉴定出十余个控制自噬过程的关键基因,并将其命名为ATG。随后的十几年间,研究人员逐渐鉴定出40余个ATG成员,这些基因协同调节细胞稳态,在细胞自噬和其他生理过程中发挥重要作用。根据Beth Levine与Guido Kroemer合作在Cell发表的论文,已知ATG家族蛋白的基本功能远不止于经典的自噬过程,其广泛参与包括:自噬溶酶体降解途径;LC3相关的细胞吞噬;非常规分泌性蛋白质、炎症介质等分泌;颗粒/溶酶体分泌的胞吐作用;外泌体分泌;以及依赖于逆运复合体的囊泡运输等膜动态过程。此外ATG蛋白还参与了病原体复制过程、细胞死亡途径、细胞周期调控和先天免疫信号传导等其他关键细胞事件1,2。
其中,参与自噬溶酶体降解途径是ATG最为重要的功能。已知约有16-20个核心ATG蛋白直接参与该通路的执行,根据不同功能,ATG蛋白家族可被分为多个功能复合体,主要包括:ATG1蛋白激酶复合体、ATG9复合体、磷脂酰肌醇3-激酶PI3K复合体和ATG5/12/16复合体等3,4。接下来,小恒将以自噬溶酶体降解过程中各核心复合体的参与顺序,为大家逐一解析在自噬通路不同阶段发挥关键作用的ATG基因家族成员。
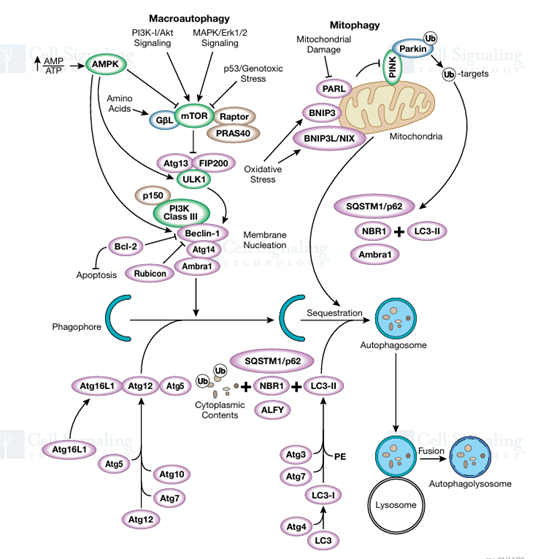
图1. 自噬信号转导通路(2025 © Cell Signaling Technology)
二、基因详解
1.ULK1/Atg1复合物——自噬起始调控
自噬的启动依赖于ULK1/2激酶复合物的激活,这一复合物在哺乳动物中则一般由ULK1(或ULK2)和ATG13、FIP200(又称RB1CC1,ATG17)、ATG101组成;在酵母中对应为Atg1、Atg13及Atg17-Atg29-Atg31复合物组成。该复合体作为自噬通路中的关键信号换能器,负责整合上游能量感应通路(如mTOR与AMPK)的信号,并启动下游自噬体形成过程。在自噬启动阶段,ATG13与FIP200-ATG101复合体预组装形成一个平台,进而招募ULK1形成完整复合物,该复合物被上游信号激活后从胞浆中易位并富集到自噬体形成位点(Phagophore Assembly Site,PAS),由此启动下游事件。其中,ULK1作为催化核心分子,已在多项研究中被用于鉴定上游调节激酶,识别调控自噬通路的下游底物,并被视为潜在的自噬调节药物靶点。
ATG13(autophagy related 13)作为一个关键的支架蛋白,将ULK1与FIP200连接起来以维持复合物的结构稳定性和激酶活性,是ULK1的直接作用底物和调控因子5。在结构上,ATG13可分为两个区域:N端为球状结构域,包含HORMA(Hop1、Rev7和Mad2)折叠,负责与ATG101相互作用并用于招募ATG14;C端为一个较长的内在无序区域(IDR),包含两个FIP200结合区和一个与ULK1 C端EAT/tMIT结构域结合的基序。此外,ATG13的中间区域包含多个磷酸化位点,这些位点在营养状态变化时被磷酸化或去磷酸化,动态调节其与ULK1和FIP200的结合能力6。在营养充足条件下,ATG13被TORC1高度磷酸化,抑制其与ULK1和FIP200的互作,负向调节ULK1激酶活性,从而抑制自噬;而在饥饿条件下,ATG13发生去磷酸化,并通过其中间区域与ULK1和ATG17相互作用,促进复合物组装,诱导ULK1向PAS的募集及ULK1的二聚化和激活。
FIP200(focal adhesion kinase family interacting protein of 200 kDa,RB1CC1)即200 kDa黏着斑激酶家族相互作用蛋白,早期研究发现其与FAK激酶结合并抑制其激酶活性,后续进一步研究中将其鉴定为酵母Atg17的哺乳动物同源物7,8。人FIP200基因编码一种200kDa的蛋白质,结构包含一个二聚化的N端结构域、一个IDR、一个线圈(CC)区域和一个包含亮氨酸拉链基序的C端“爪”结构域。N端结构域二聚体支撑ULK1复合物的组装,C端爪结构域可与NDP52、p62、TAX1BP1等运货受体(cargo receptor)相互作用,从而将ULK1复合物招募至特定细胞位置,此外也可通过与ATG16L1直接相互作用调节自噬体形成9–11。在III类磷脂酰肌醇-3激酶复合物PI3KC3-C1存在下,ULK复合物与PI3KC3-C1形成超复合物,使得ULK1在FIP200支架上完成二聚化,形成自噬的结构机制。在酵母中,一个Atg13与不同的Atg17二聚体中的两个Atg17结合,这种结合模式可形成高阶组装,诱导Atg1复合物的液-液相分离,促进Atg蛋白聚集并组织自噬体形成位点;而哺乳动物中,一个ATG13与同一FIP200二聚体内的两个FIP200结合,无法诱导ULK复合物的高阶组装,这代表可能存在其他潜在机制实现相分离12。近年研究表明,内质网表面的钙瞬变可诱导FIP200的液-液相分离,形成易于融合的小滴状结构,触发自噬体形成位点13。
此外,在线粒体自噬中,FIP200介导了ULK1激酶复合物向线粒体的特异性募集,并在后续自噬阶段中通过自身磷酸化修饰调节下游过程8。
ATG101(autophagy-related protein 101)是一个高度保守的的自噬调节蛋白,在除酿酒酵母外的大多数真核生物中,其作为ULK/Atg1复合物的必需亚基代替了酵母系统中的Atg29和Atg31。人ATG101基因编码一个218个氨基酸的蛋白,该蛋白整体为一个典型的HORMA结构域,通过这一结构域与ATG13形成异二聚体,保护ATG13免受蛋白酶体降解,维持ULK1复合物稳定性14,15。此外,ATG101可通过C端区域与PI3KC3复合物相互作用,以及通过Trp-Phe(WF)指区与其他下游因子相互作用来确保准确的自噬诱导信号传导16。
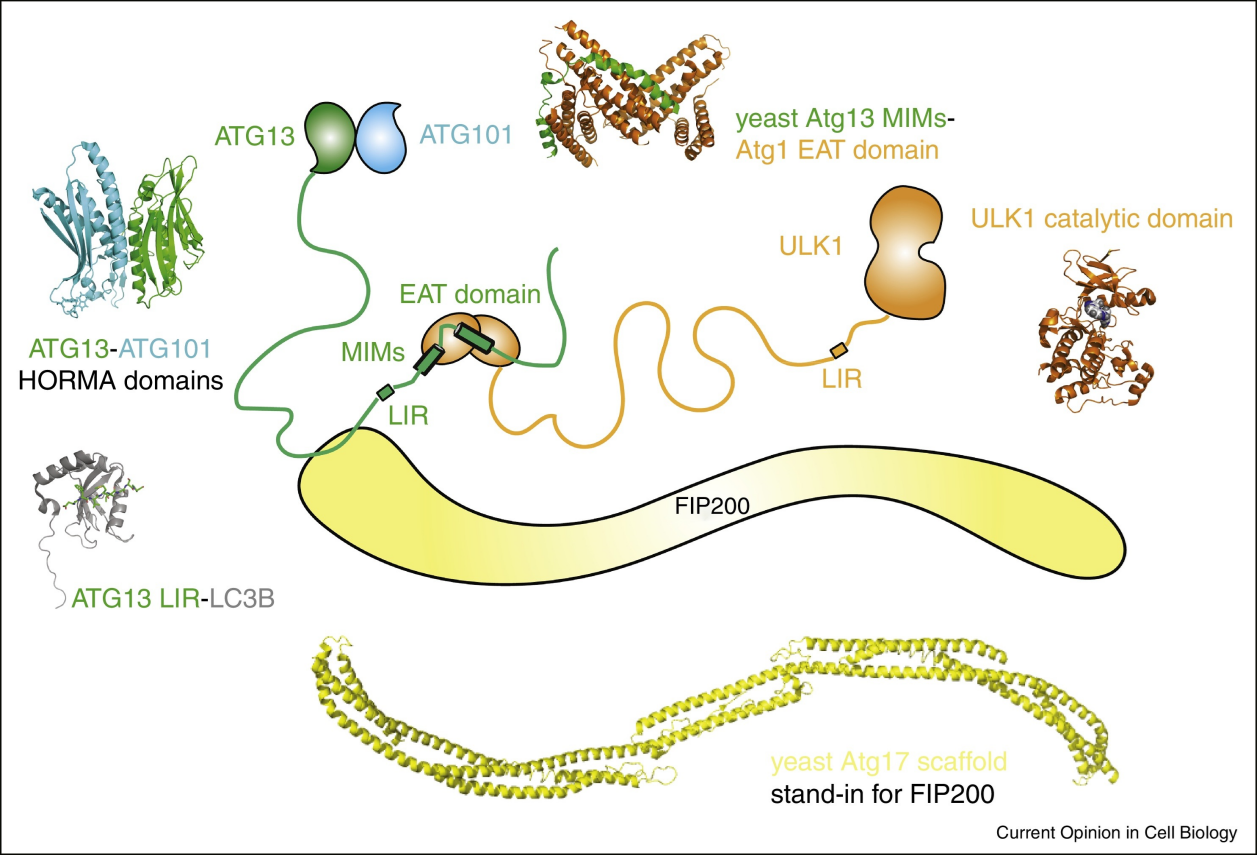
图2. ULK1复合体模型17
2.III型PI3K复合物——膜成核
III型磷脂酰肌醇3-激酶(PtdIns3k)通过磷酸化磷脂酰肌醇产生磷脂酰肌醇3磷酸(PI3P)是自噬起始过程中的早期事件,PI3P可招募下游效应蛋白,介导自噬特异性膜运输与成核(nucleation)过程,为自噬泡的形成奠定基础18,19。PtdIns3k至少形成两种不同的复合物,称为I型复合物和II型复合物(PI3KC3-C1和C2),这两种复合物都包含催化亚基PIK3C3(酵母Vsp34的哺乳动物同源体)、识别蛋白激酶PIK3R4(酵母Vps15的哺乳动物同源体)和Beclin1(酵母Atg6的哺乳动物同源体),此外PI3KC3-C1还包含Atg14L,PI3KC3-C2还包含抗紫外辐射相关基因UVRAG。PI3KC3-C2与UVRAG共同促进内体和自噬体的成熟;而PI3KC3-C1复合物负责在隔离膜上产生PI3P,募集WIPI蛋白,驱动膜延伸20。在此复合物中我们将介绍ATG14和Beclin1这两种重要的ATG蛋白家族成员。
Beclin1是哺乳动物中首个被鉴定的自噬相关基因,作为酵母Atg6的哺乳动物同源基因,在PI3KC3复合物中的发挥核心支架作用。自噬启动时,Beclin1受活化的ULK1磷酸化修饰,增强了与VPS34、VPS15和ATG14L的结合作用,促进PI3K III复合体的组装和激活,通过与其他几种蛋白质相互作用来执行其自噬和膜运输功能。人BECN1基因编码一种450个氨基酸的蛋白质,包含三个重要功能区域:N端为具有多个磷酸化位点的无序区域,以及与BCL-2蛋白相互作用所需的BCL-2同源-3(BH3)结构域,而BCL-2通过与该结构域结合限制Beclin1参与形成C1和C2的水平,从而抑制自噬;中段为可与UVRAG或ATG14的CC结构域相互作用的卷曲(CC)结构域,通过这一结构域可实现与UVRAG或ATG14竞争性结合导致形成相对更稳定的二聚体,通过变构调节相关的脂质激酶活性;C端为与膜结合的β-α自噬特异性(BARA)结构域,CC结构域的C端和BARA结构域之间的部分重叠区域被称为ECD,ECD/BARA区域构成与VPS34结合及膜定位的关键界面21–24。除了BCL-2家族(如BCL-2、BCL-XL等)的互作调节外,其他众多因子可通过Beclin1的磷酸化来影响自噬:Unc-51样激酶1(ULK1)、AMP活化蛋白激酶(AMPK)可磷酸化Beclin1无序区相应位点诱导自噬体的成核;致癌激酶BCR-ABL激酶通过磷酸化ECD/CC结构域的Y233和Y352位点来抑制自噬;泛素化过程中,如E3连接酶TRAF6、TRIM50可通过Beclin1的泛素化增强自噬水平;在蛋白水解裂解过程中,凋亡半胱天冬酶对Beclin1的裂解也可导致其功能失活,诱导自噬水平下降25。
ATG14(autophagy related 14)也称beclin-1相关自噬相关关键调节因子(Barkor)或ATG14L,是PI3KC3-C1的特异性自噬亚基,通过调节PI3KC3-C1复合物的细胞亚定位来引导其发挥作用。在结构上,ATG14在N端区域含有富含半胱氨酸的结构域和三个卷曲螺旋结构域,这些结构域负责ATG14的核心功能,即桥接PIK3C3和Beclin1,以及将PI3KC3-C1复合物靶向至PAS;C端具有一个Barkor/Atg14(L)自噬体靶向序列(BATS)结构域,可感知膜曲率,并通过两亲性α螺旋的疏水侧与膜结合,从而将复合物锚定到膜特定位置上游激酶对PI3KC3-C1复合物的磷酸化也反应在ATG14上,ATG14在饥饿或缺氧期间可促进ULK1复合物对Beclin1 S15或S30的磷酸化促进自噬;ATG14L中的多个丝氨酸/苏氨酸残基可被mTOR磷酸化,残基突变为丙氨酸则增加PI3K和自噬活性25–27。此外,ATG14在自噬的早期成核阶段之外也具有非PI3KC3-C1功能,它与t-SNARE复合物(STX17和SNAP29)和SNARE效应蛋白Snapin相互作用,促进自噬体-溶酶体融合过程和内吞运输活性28。
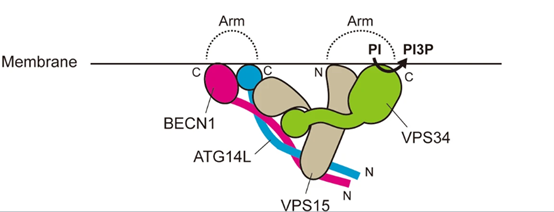
图3. 哺乳动物PI3KC3-C1复合物的结构19
3.ATG9/ATG9A转运系统——膜供给
哺乳动物细胞中的自噬体直径可达500-1500 nm,体积显著大于与经典的单膜转运囊泡(直径30-80 nm)29。而自噬体膜富含脂质,其生物合成需要大量的脂质供应,供应来源包括内质网、高尔基体、线粒体等多种细胞器的脂质递送。在将这些膜源运输至生长中的自噬体的过程中,ATG9系统承担了关键的转运功能。ATG9是ATG核心蛋白中唯一的跨膜蛋白,在脊椎动物中进化出ATG9A(autophagy related 9A)和ATG9B(autophagy related 9B)两个旁系同源基因,它们都可形成同源三聚体,并作为脂质扰乱酶参与膜脂在脂双层中的重新分布,或是通过囊泡递送脂质修饰酶以改变隔离膜的脂质组成,促进自噬体膜的形成与扩展。ATG9A是功能明确且分布广泛的核心自噬蛋白,是研究基础自噬机制的首选对象;ATG9B则具有表达组织特异性,在胎盘和垂体中表达较高,在特定组织或应激条件下可补偿ATG9A的功能缺失30。
ATG9A是自噬体形成所需的唯一跨膜蛋白,定位于小囊泡,作为脂质扰乱酶充当自噬和囊泡运输的调节剂,促进自噬体或囊泡膜的扩张。其结构可划分为三个主要区域:N端包含短的无义序列和分选基序,用于识别外壳衔接蛋白和磷酸化位点;C末端整体是无序肽段,其末端有一个HDIR(HORMA结构域相互作用区),其对于ATG9A与HORMA结构域蛋白ATG13和ATG101的相互作用至关重要;ATG9A中央区包括大约500个氨基酸,ATG9A形成的同源三聚体,每个原聚体都包含22个α螺旋和4个β链,通过跨膜螺旋的结构域交换组装而成,具有内部孔和空腔分支网络,包括一个亲水性中心孔、三个侧孔和三个垂直孔,这种复杂的空腔结构在膜中形成漏斗状溶剂池,使得磷脂在双膜脂质小叶之间的运动,从而实现其脂质扰乱功能31–33。
在大自噬起始阶段,ATG9A囊泡与组装完成的ULK复合物相互作用,ATG9A先于ATG13异位至内质网,并在omega体上产生磷脂酰肌醇4-磷酸(PI4P)以募集ATG13,两者在内质网延伸、omega体上的相互作用催化隔离膜的形成。有研究表明,在p62依赖性自噬或NDP52依赖性线粒体自噬过程中,ATG13-ATG101可以不依赖ULK结合ATG9A,这代表ATG9A可介导非经典起始调控路径。在衍生阶段,ATG9A囊泡作为隔离膜的“种子膜”,ATG9A可接受脂质实现自噬体的延伸,或恢复隔离膜上的脂质失衡。脂桥转运蛋白可与ATG9A相互作用,将脂质从供体膜直接转移至受体膜,例如,ATG9A的中央孔和侧支旁近位点可与脂桥转运蛋白ATG2A的C末端结合,而ATG2A介导的含PI3P膜结构间的脂质转移受到酵母Atg18/21的哺乳动物同源物WIPI4的刺激,这类相互作用共同增强了复合物的膜拴系能力和脂质转移34,35。在膜闭合阶段,ATG9A被证明可与IQGAP1相互作用招募内体分选复合物ESCRT-III,通过类质膜修复的机制促进自噬体的闭合。在PINK1-Parkin介导的线粒体自噬中,ATG9A囊泡和ULK1/FIP200由运货受体独立募集到受损线粒体上,触发隔离膜形成,最终包裹受损细胞器形成自噬体8。除了自噬功能外,ATG9A在质膜修复、囊泡运输、趋化迁移和细胞器稳态中也起着至关重要的作用36。
ATG9B的结构与酵母同源物更为相似,但与ATG9A相比C末端较短且缺乏HDIR,这表明ATG9B可能不与ATG13-ATG101结合,或存在其他互作机制;而ATG9B的N末端比ATG9A更长,并含有富含脯氨酸的重复区,该结构可能参与核糖体停滞等调控过程37。一项研究发现小鼠肝细胞的Atg9b敲低降低了LC3脂化水平和自噬斑点数;在另一项研究中,人HEK293A细胞中ATG9B的表达能够挽救ATG9A基因敲除细胞中SQSTM1的异常积累30。这些研究表明ATG9B与ATG9A之间相似的结构使得这两个基因功能存在重叠,但目前关于ATG9B的研究较少,其在ATG9A功能冗余之外是否具有独特生理角色仍不清楚。
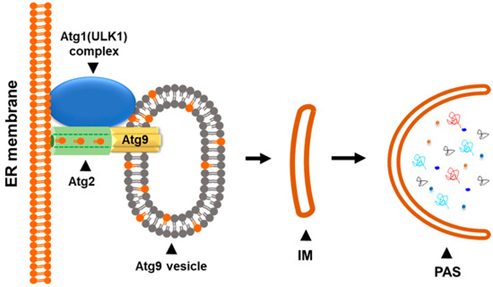
图4. Atg9囊泡参与自噬体生物发生的起始38
4.Atg12-ATG5泛素样结合系统——膜延伸闭合
隔离膜中的PI3P的产生可招募效应子WIPI2,WIPI2通过将E3-连接酶(ATG12-ATG5-ATG16L1)复合物募集到隔离膜中,诱导ATG8蛋白(LC3和GABARAPLs)与PE,组装成蛋白支架以促进自噬中的隔离膜扩展衍生39。在这个过程,ATG12-ATG5-ATG16L1和ATG8/LC3/GABARAP系统构成了泛素样共价偶联系统,在膜的延伸、弯曲以及闭合中起到了关键作用40。虽然ATG12-ATG5-ATG16L1复合物本身并不直接参与膜的弯曲或封闭,但它扮演着类似于E3泛素连接酶的角色,将E2结合酶(LC3-ATG3)和底物(自噬体膜上的PE)在空间上拉近,促进LC3从ATG3向PE的转移,对于LC3/ATG8-PE系统的运行十分重要。
ATG12(autophagy related 12)是一个类泛素蛋白,促进膜的延伸闭合以形成自噬小体。人源ATG12蛋白由140个氨基酸组成,在结构上,ATG12包含N端的一段内源性无序区(IDPR),泛素样结构域(YBL)和一段无序序列。在酵母中,IDPR区域与UBL结构域相邻对于其与Atg7和Atg10的结合至关重要,也可保护Atg12的C端免受蛋白酶降解。ATG12的一级结构与泛素(Ub)蛋白并没有同源性,但是ATG12存在泛素超折叠结构以及形成异肽键C端的甘氨酸。在ATG12系统中,泛素样蛋白ATG12的C端甘氨酸被E1样酶ATG7以ATP依赖的方式激活,依次与ATG7和E2样酶ATG10形成硫酯中间体,最终通过异肽键与ATG5的受体赖氨酸残基结合,此外,Atg12还与Atg5形成疏水和亲水性相互作用,从而固定其在Atg5上的位置41,42。两组ATG12-ATG5偶联物与ATG16(L)二聚体形成复合体,并作为ATG8家族的E3酶促进Atg8与膜脂质磷脂酰乙醇胺(PE)的头基结合43。
ATG7(autophagy related 7)是一种同源二聚体E1样酶,在自噬中可激活两条泛素样修饰通路。在结构上,ATG7包含N端结构域(ETD)和C端结构域(CTD)44。NTD负责结合E2(Atg3、Atg10),从而将ATG8转移至ATG3或将ATG12转移至ATG10;CTD中包含三个重要结构域,具有ATP结合位点的腺苷化结构域(AD)负责结合和催化ATP与ATG12或ATG8的C末端甘氨酸形成高能硫酯键,催化半胱氨酸结构域(CL)负责接收被激活的ATG12或ATG8以形成短暂的中间体,C端结构域(ECTD)负责识别和捕获底物。ATG7可分别驱动ATG8或ATG12腺苷化,消耗ATP与二者形成硫酯中间体(如ATG7-ATG12),随后将它们转移到两个同源的E2酶ATG3或ATG10上。作为自噬机制的一部分,ATG7除了参与降解途径,也参与调控细胞凋亡与坏死的转换45,46。此外,研究还发现了一种缺乏E1样酶活性的ATG7同工型,该变体无法对ATG8同源蛋白进行脂化修饰,这一同工型生物学功能尚不明确,但它可能通过破坏功能性ATG7同源二聚体的形成来负向调控自噬过程47。
ATG10(autophagy related 10)负责承接由ATG7激活的ATG12并将其最终递送至ATG5,是介导ATG12与ATG5连接的E2样结合酶45。在结构上,ATG10呈现典型的E2酶样折叠(UBC折叠),该结构由一个四链反平行的β-折叠片层和围绕在其周围的几个α-螺旋组成,在相对灵活的催化环结构上存在一个保守的半胱氨酸残基,在UBC核心结构域的C端有一个额外的α-螺旋结构域48。在自噬流中,ATG10的半胱氨酸残基亲核攻击ATG7-ATG12的硫酯键,将ATG12被转移到ATG10上,同时释放出ATG7;当ATG10-ATG12复合物与ATG5正确定位后,由ATG5攻击ATG10-ATG12中的硫酯键形成酰胺键,生成稳定的ATG12-ATG5共价复合物并释放ATG10。ATG10的活性半胱氨酸被释放出来,恢复到自由状态,可以重新回到第一步,参与下一轮的催化循环49。
ATG5(autophagy related 5)是一个泛素样蛋白,负责促进LC3-PE酰胺键形成和自噬体的膜延伸。人类ATG5由275个氨基酸组成,主要由N端和C端两个串联的、结构上类似的泛素样结构域(Ubl)和一个富含螺旋结构域的铰链区构成,这三个结构域融入了ATG5独特的整体结构,与其他蛋白进行相互作用。N端Ubl结构域主要负责与ATG16L1的相互作用;C端Ubl结构域负责与ATG3相互作用;位于连接两个Ubl结构域的柔性铰链区域附近的共价修饰位点Lys130可与ATG12发生G-Cter共价结合,形成ATG12–ATG5共轭体50,51。ATG5是ATG12唯一的共价修饰靶标,由此形成的ATG12-ATG5异源二聚体是一个具有下游功能的活性单位,可被ATG16L1特异性地识别并进行非共价结合,组装为ATG12-ATG5-ATG16L1复合物。复合物定位于隔离膜后,ATG5可通过C端Ubl结构域捕获并定位携带LC3的ATG3。此外,在ATG16L1缺失的情况下,位于溶酶体膜上的TECPR1(结合PtdIns(4)P的溶酶体蛋白)可招募ATG5-ATG12复合物中的ATG5,结合组装成ATG12-ATG5-TECPR1类E3复合物,调控非典型LC3脂质化,介导自噬体-溶酶体融合或修复损伤的溶酶体膜52,53。
ATG16L1(autophagy related 16 like 1)是酵母Atg16的功能性哺乳动物同源物,主要负责下游靶隔离膜的识别和锚定54。人源ATG16L1蛋白由607个氨基酸组成,包含三个主要结构域:N端ATG5结合域可与ATG5蛋白特异性结合;中段的卷曲螺旋结构域(CCD)可驱动两个ATG16L1分子寡聚化形成同源二聚体,促使ATG12-ATG5-ATG16L1单元组装成最终的四聚体,此外,这一区域也可结合WIPI2和Rab33调节自噬体膜的延长;C端WD40重复结构域识别早期自噬膜上的PIP3和WIPI2,实现膜识别和靶向结合,并可能参与炎症控制和病原体清除等过程55–57。ATG16L1介导ATG12-ATG5复合物到隔离膜的招募,并将两个共价偶联系统固定至膜上,使LC3在该位点发生脂化,进而促进隔离膜的伸长、闭合,最终形成自噬体和自噬溶酶体。另外,ATG16L1也参与不形成典型双膜自噬体的LC3相关吞噬,例如LAP(LC3相关吞噬作用)时,ATG16L1会被招募至吞噬泡的膜上并驱动LC3的脂化58。另一种哺乳动物同源物ATG16L2与ATG16L1差异集中在中段CCD区,这使得ATG16L2可与ATG12-ATG5形成复合物,但在常规自噬过程中缺乏LC3酯化激活性59,60。近年的研究发现ATG16L2的缺失并不影响自噬流,而它的过表达可能竞争性抑制ATG16L1的作用,但内源性ATG16L2的主要功能依然尚待探究61,62。
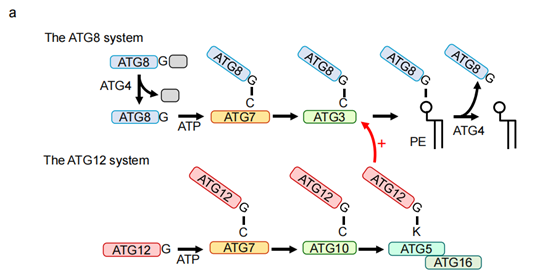
图5. ATG共轭系统43
三、相关的载体现货
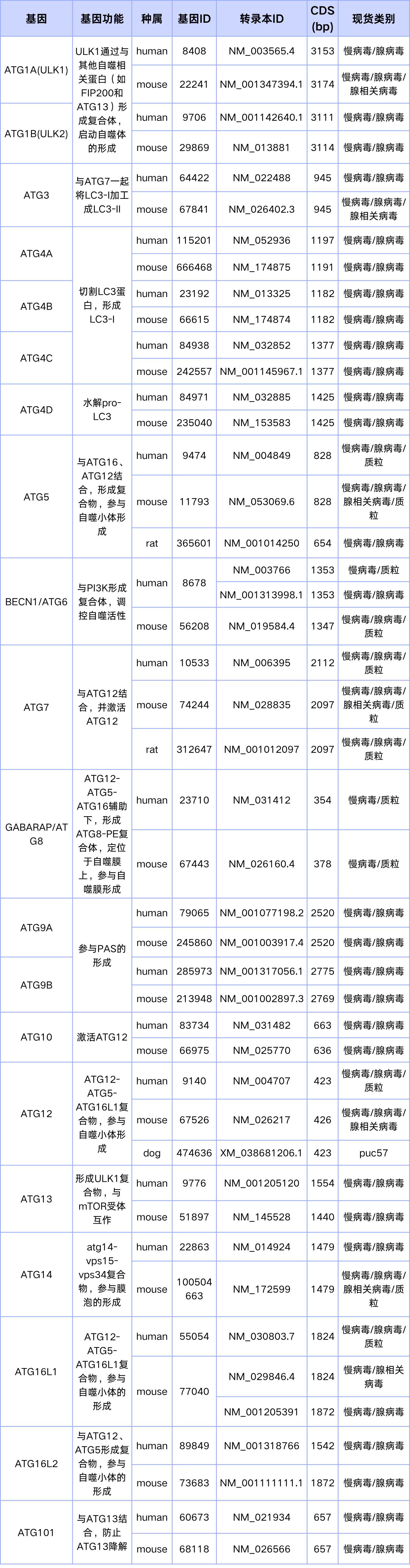
汉恒生物专营病毒包装十余载,建立了庞大的基因研究现货工具库,可为广大研究人员提供多种炎性小体相关基因的病毒现货。若有其他病毒包装需求或疑问,也欢迎随时咨询汉恒生物微信公众号或拨打官网技术服务热线:400-092-0065。
表1. ATG相关基因现货列表
参考文献:
1.Levine B, Kroemer G. Biological Functions of Autophagy Genes: A Disease Perspective. Cell. 2019;176(1-2):11-42. doi:10.1016/j.cell.2018.09.048
2.Yamamoto H, Zhang S, Mizushima N. Autophagy genes in biology and disease. Nat Rev Genet. 2023;24(6):382-400. doi:10.1038/s41576-022-00562-w
3.Tanida I. Autophagosome formation and molecular mechanism of autophagy. Antioxid Redox Signal. 2011;14(11):2201-2214. doi:10.1089/ars.2010.3482
4.Mizushima N, Yoshimori T, Ohsumi Y. The role of Atg proteins in autophagosome formation. Annu Rev Cell Dev Biol. 2011;27:107-132. doi:10.1146/annurev-cellbio-092910-154005
5.Alers S, Wesselborg S, Stork B. ATG13. Autophagy. 2014;10(6):944-956. doi:10.4161/auto.28987
6.Yamamoto H, Fujioka Y, Suzuki SW, et al. The Intrinsically Disordered Protein Atg13 Mediates Supramolecular Assembly of Autophagy Initiation Complexes. Dev Cell. 2016;38(1):86-99. doi:10.1016/j.devcel.2016.06.015
7.Gan B, Guan JL. FIP200, a key signaling node to coordinately regulate various cellular processes. Cell Signal. 2008;20(5):787-794. doi:10.1016/j.cellsig.2007.10.021
8.Eickhorst C, Babic R, Rush-Kittle J, et al. FIP200 Phosphorylation Regulates Late Steps in Mitophagy. Journal of Molecular Biology. 2024;436(15):168631. doi:10.1016/j.jmb.2024.168631
9.Turco E, Witt M, Abert C, et al. FIP200 Claw Domain Binding to p62 Promotes Autophagosome Formation at Ubiquitin Condensates. Mol Cell. 2019;74(2):330-346.e11. doi:10.1016/j.molcel.2019.01.035
10.Gong X, Zhou Y, Wang Y, et al. Molecular bases of the interactions of ATG16L1 with FIP200 and ATG8 family proteins. Nat Commun. 2025;16(1):9035. doi:10.1038/s41467-025-64097-4
11.Ohnstad AE, Delgado JM, North BJ, et al. Receptor‐mediated clustering of FIP200 bypasses the role of LC3 lipidation in autophagy. EMBO J. 2020;39(24):e104948. doi:10.15252/embj.2020104948
12.Hama Y, Fujioka Y, Yamamoto H, Mizushima N, Noda NN. The triad interaction of ULK1, ATG13, and FIP200 is required for ULK complex formation and autophagy. eLife. 13:RP101531. doi:10.7554/eLife.101531
13.Zheng Q, Chen Y, Chen D, et al. Calcium transients on the ER surface trigger liquid-liquid phase separation of FIP200 to specify autophagosome initiation sites. Cell. 2022;185(22):4082-4098.e22. doi:10.1016/j.cell.2022.09.001
14.Qi S, Kim DJ, Stjepanovic G, Hurley JH. Structure of the Human Atg13-Atg101 HORMA Heterodimer: an Interaction Hub within the ULK1 Complex. Structure. 2015;23(10):1848-1857. doi:10.1016/j.str.2015.07.011
15.Noda NN, Mizushima N. Atg101: Not Just an Accessory Subunit in the Autophagy-initiation Complex. Cell Struct Funct. 2016;41(1):13-20. doi:10.1247/csf.15013
16.Kim BW, Jin Y, Kim J, et al. The C-terminal region of ATG101 bridges ULK1 and PtdIns3K complex in autophagy initiation. Autophagy. 2018;14(12):2104-2116. doi:10.1080/15548627.2018.1504716
17.Lin MG, Hurley JH. Structure and Function of the ULK1 Complex in Autophagy. Curr Opin Cell Biol. 2016;39:61-68. doi:10.1016/j.ceb.2016.02.010
18.Yu X, Long YC, Shen HM. Differential regulatory functions of three classes of phosphatidylinositol and phosphoinositide 3-kinases in autophagy. Autophagy. 2015;11(10):1711-1728. doi:10.1080/15548627.2015.1043076
19.Nishimura T, Tooze SA. Emerging roles of ATG proteins and membrane lipids in autophagosome formation. Cell Discov. 2020;6:32. doi:10.1038/s41421-020-0161-3
20.Cook ASI, Chen M, Nguyen TN, et al. Structural pathway for PI3-kinase regulation by VPS15 in autophagy. Science. 2025;388(6743):eadl3787. doi:10.1126/science.adl3787
21.Huang W, Choi W, Hu W, et al. Crystal structure and biochemical analyses reveal Beclin 1 as a novel membrane binding protein. Cell Res. 2012;22(3):473-489. doi:10.1038/cr.2012.24
22.Li X, He L, Che KH, et al. Imperfect interface of Beclin1 coiled-coil domain regulates homodimer and heterodimer formation with Atg14L and UVRAG. Nat Commun. 2012;3:662. doi:10.1038/ncomms1648
23.Pattingre S, Tassa A, Qu X, et al. Bcl-2 antiapoptotic proteins inhibit Beclin 1-dependent autophagy. Cell. 2005;122(6):927-939. doi:10.1016/j.cell.2005.07.002
24.Ye J, Zhang J, Zhu Y, et al. Targeting autophagy and beyond: Deconvoluting the complexity of Beclin-1 from biological function to cancer therapy. Acta Pharmaceutica Sinica B. 2023;13(12):4688-4714. doi:10.1016/j.apsb.2023.08.008
25.Park JM, Seo M, Jung CH, et al. ULK1 phosphorylates Ser30 of BECN1 in association with ATG14 to stimulate autophagy induction. Autophagy. 2018;14(4):584-597. doi:10.1080/15548627.2017.1422851
26.Matsunaga K, Morita E, Saitoh T, et al. Autophagy requires endoplasmic reticulum targeting of the PI3-kinase complex via Atg14L. J Cell Biol. 2010;190(4):511-521. doi:10.1083/jcb.200911141
27.Zhong Y, Wang QJ, Li X, et al. Distinct regulation of autophagic activity by Atg14L and Rubicon associated with Beclin 1- phosphatidylinositol 3-kinase complex. Nat Cell Biol. 2009;11(4):468-476. doi:10.1038/ncb1854
28.Diao J, Liu R, Rong Y, et al. ATG14 promotes membrane tethering and fusion of autophagosomes to endolysosomes. Nature. 2015;520(7548):563-566. doi:10.1038/nature14147
29.Gómez-Sánchez R, Tooze SA, Reggiori F. Membrane supply and remodeling during autophagosome biogenesis. Current Opinion in Cell Biology. 2021;71:112-119. doi:10.1016/j.ceb.2021.02.001
30.Chiduza GN, Garza-Garcia A, Almacellas E, et al. ATG9B is a tissue-specific homotrimeric lipid scramblase that can compensate for ATG9A. Autophagy. 2024;20(3):557-576. doi:10.1080/15548627.2023.2275905
31.Ren X, Nguyen TN, Lam WK, et al. Structural basis for ATG9A recruitment to the ULK1 complex in mitophagy initiation. Science Advances. 2023;9(7):eadg2997. doi:10.1126/sciadv.adg2997
32.Guardia CM, Tan XF, Lian T, et al. Structure of Human ATG9A, the Only Transmembrane Protein of the Core Autophagy Machinery. Cell Reports. 2020;31(13). doi:10.1016/j.celrep.2020.107837
33.Maeda S, Yamamoto H, Kinch LN, et al. Structure, lipid scrambling activity and role in autophagosome formation of ATG9A. Nat Struct Mol Biol. 2020;27(12):1194-1201. doi:10.1038/s41594-020-00520-2
34.Nguyen A, Lugarini F, David C, et al. Metamorphic proteins at the basis of human autophagy initiation and lipid transfer. Molecular Cell. 2023;83(12):2077-2090.e12. doi:10.1016/j.molcel.2023.04.026
35.Vliet AR van, Chiduza GN, Maslen SL, et al. ATG9A and ATG2A form a heteromeric complex essential for autophagosome formation. Molecular Cell. 2022;82(22):4324-4339.e8. doi:10.1016/j.molcel.2022.10.017
36.Lin X, Liang L, Liao S, Li Y, Zhou Y. Progress on multifunctional transmembrane protein ATG9A. Cell Commun Signal. 2025;23(1):314. doi:10.1186/s12964-025-02317-6
37.Millard E, Tooze SA. ATG9 Not Just an Autophagy Related Protein. Journal of Molecular Biology. 2025;437(18):169288. doi:10.1016/j.jmb.2025.169288
38.Wei Z, Hu X, Wu Y, Zhou L, Zhao M, Lin Q. Molecular Mechanisms Underlying Initiation and Activation of Autophagy. Biomolecules. 2024;14(12):1517. doi:10.3390/biom14121517
39.Campisi D, Hawkins N, Bonjour K, Wollert T. The Role of WIPI2, ATG16L1 and ATG12-ATG5 in Selective and Nonselective Autophagy. Journal of Molecular Biology. 2025;437(18):169138. doi:10.1016/j.jmb.2025.169138
40.Walczak M, Martens S. Dissecting the role of the Atg12–Atg5-Atg16 complex during autophagosome formation. Autophagy. 2013;9(3):424-425. doi:10.4161/auto.22931
41.Mizushima N, Noda T, Yoshimori T, et al. A protein conjugation system essential for autophagy. Nature. 1998;395(6700):395-398. doi:10.1038/26506
42.Noda NN, Fujioka Y, Hanada T, Ohsumi Y, Inagaki F. Structure of the Atg12-Atg5 conjugate reveals a platform for stimulating Atg8-PE conjugation. EMBO Rep. 2013;14(2):206-211. doi:10.1038/embor.2012.208
43.Mizushima N. The ATG conjugation systems in autophagy. Curr Opin Cell Biol. 2020;63:1-10. doi:10.1016/j.ceb.2019.12.001
44.Noda NN, Satoo K, Fujioka Y, et al. Structural basis of Atg8 activation by a homodimeric E1, Atg7. Mol Cell. 2011;44(3):462-475. doi:10.1016/j.molcel.2011.08.035
45.Noda NN. Structural biology of the Atg8 and Atg12 conjugation systems. Autophagy Reports. 2023;2(1):2277582. doi:10.1080/27694127.2023.2277582
46.Yamaguchi M, Satoo K, Suzuki H, et al. Atg7 Activates an Autophagy-Essential Ubiquitin-like Protein Atg8 through Multi-Step Recognition. J Mol Biol. 2018;430(3):249-257. doi:10.1016/j.jmb.2017.12.002
47.Ogmundsdottir MH, Fock V, Sooman L, et al. A short isoform of ATG7 fails to lipidate LC3/GABARAP. Sci Rep. 2018;8(1):14391. doi:10.1038/s41598-018-32694-7
48.Hong SB, Kim BW, Kim JH, Song HK. Structure of the autophagic E2 enzyme Atg10. Acta Cryst D. 2012;68(10):1409-1417. doi:10.1107/S0907444912034166
49.Nemoto T, Tanida I, Tanida-Miyake E, et al. The Mouse APG10 Homologue, an E2-like Enzyme for Apg12p Conjugation, Facilitates MAP-LC3 Modification *. Journal of Biological Chemistry. 2003;278(41):39517-39526. doi:10.1074/jbc.M300550200
50.Sakoh-Nakatogawa M, Matoba K, Asai E, et al. Atg12-Atg5 conjugate enhances E2 activity of Atg3 by rearranging its catalytic site. Nat Struct Mol Biol. 2013;20(4):433-439. doi:10.1038/nsmb.2527
51.Changotra H, Kaur S, Yadav SS, Gupta GL, Parkash J, Duseja A. ATG5: A central autophagy regulator implicated in various human diseases. Cell Biochem Funct. 2022;40(7):650-667. doi:10.1002/cbf.3740
52.Chen D, Fan W, Lu Y, Ding X, Chen S, Zhong Q. A mammalian autophagosome maturation mechanism mediated by TECPR1 and the Atg12-Atg5 conjugate. Mol Cell. 2012;45(5):629-641. doi:10.1016/j.molcel.2011.12.036
53.Corkery DP, Castro-Gonzalez S, Knyazeva A, Herzog LK, Wu YW. An ATG12-ATG5-TECPR1 E3-like complex regulates unconventional LC3 lipidation at damaged lysosomes. EMBO Rep. 2023;24(9):e56841. doi:10.15252/embr.202356841
54.Hamaoui D, Subtil A. ATG16L1 functions in cell homeostasis beyond autophagy. The FEBS Journal. 2022;289(7):1779-1800. doi:10.1111/febs.15833
55.Rao S, Skulsuppaisarn M, Strong LM, et al. Three-step docking by WIPI2, ATG16L1, and ATG3 delivers LC3 to the phagophore. Sci Adv. 2024;10(6):eadj8027. doi:10.1126/sciadv.adj8027
56.Boada‐Romero E, Letek M, Fleischer A, Pallauf K, Ramón‐Barros C, Pimentel‐Muiños FX. TMEM59 defines a novel ATG16L1‐binding motif that promotes local activation of LC3. EMBO J. 2013;32(4):566-582. doi:10.1038/emboj.2013.8
57.Dooley HC, Razi M, Polson HEJ, Girardin SE, Wilson MI, Tooze SA. WIPI2 Links LC3 Conjugation with PI3P, Autophagosome Formation, and Pathogen Clearance by Recruiting Atg12–5-16L1. Molecular Cell. 2014;55(2):238-252. doi:10.1016/j.molcel.2014.05.021
58.Magné J, Green DR. LC3-associated endocytosis and the functions of Rubicon and ATG16L1. Sci Adv. 2022;8(43):eabo5600. doi:10.1126/sciadv.abo5600
59.Dooley HC, Razi M, Polson HEJ, Girardin SE, Wilson MI, Tooze SA. WIPI2 Links LC3 Conjugation with PI3P, Autophagosome Formation, and Pathogen Clearance by Recruiting Atg12–5-16L1. Molecular Cell. 2014;55(2):238-252. doi:10.1016/j.molcel.2014.05.021
60.Don Wai Luu L, Kaakoush NO, Castaño-Rodríguez N. The role of ATG16L2 in autophagy and disease. Autophagy. 2022;18(11):2537-2546. doi:10.1080/15548627.2022.2042783
61.Khor B, Conway KL, Omar AS, et al. Distinct Tissue-Specific Roles for the Disease-Associated Autophagy Genes ATG16L2 and ATG16L1. The Journal of Immunology. 2019;203(7):1820-1829. doi:10.4049/jimmunol.1800419
62.Wible DJ, Chao HP, Tang DG, Bratton SB. ATG5 cancer mutations and alternative mRNA splicing reveal a conjugation switch that regulates ATG12–ATG5-ATG16L1 complex assembly and autophagy. Cell Discov. 2019;5(1):42. doi:10.1038/s41421-019-0110-1

查看更多

查看更多

查看更多

联系我们

返回顶部