查看更多

 明星产品
明星产品
 关注我们
关注我们

扫码关注我们
了解更多信息
自噬是细胞或者有机体在营养缺乏等环境应激条件下,通过在细胞里产生双层膜自噬体,包裹细胞质或受损伤的细胞器等,将它们运送到溶酶体或液泡中进行降解,维持细胞稳态平衡的重要生物学过程。自噬体的形成需要约20个基因(或基因家族),这些基因被称为核心自噬相关(ATG)基因。这些基因产物可分为六个功能组:(1)ATG1(哺乳动物中为ULK)激酶复合体,(2)ATG9囊泡,(3)含ATG14的PtdIns 3-激酶复合体,(4)ATG2-ATG18复合体,(5)ATG12偶联系统,以及(6)ATG8偶联系统。Atg8偶联系统由四种Atg蛋白组成,Atg3、Atg4、Atg7和Atg8,新生的Atg8被半胱氨酸蛋白酶Atg4加工以暴露出其C末端甘氨酸(Gly),加工后的Atg8被E1样酶Atg7(与Atg12共用同一个E1酶)激活,然后被转移到E2样酶Atg3,最后,Atg8的C末端甘氨酸与磷脂酰乙醇胺(PE)的氨基形成酰胺键以结合,Atg8-PE结合物会再一次被Atg4处理以解离。本期我们一起来了解下参与ATG8偶联系统的基因:ATG8、ATG4、ATG7和ATG3。

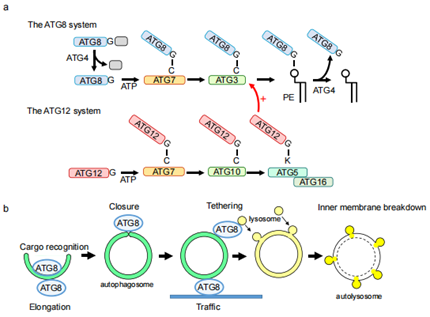
图1. ATG8-PE偶联系统[1]
一、ATG8家族
ATG8蛋白是一种泛素样蛋白,最初在酿酒酵母中被鉴定出来,ATG8曾被以不同方式命名Apg8、Aut7、Cvt5和Paz2。2003年对命名进行了统一,最终命名为ATG8。人类基因组总共包含七个功能性ATG8基因,它们被细分为LC3亚型(LC3A、LC3B、LC3B2和LC3C)和GABARAP亚型(GABARAP、GABARAPL1和GABARAPL2)。GABARAP、GABARAPLI和GABARAPL2基因分别定位于17、12和16号染色体上,并编码三种不同的蛋白质,均含有117个氨基酸。LC3A、LC3B、LC3B2和LC3C基因分别定位于20、16、12和1号染色体上,分别含有121、125、125和147个氨基酸。多种Atg8同源蛋白在哺乳动物系统中的共存引发了一个关键问题:它们是否在自噬中各自具有独特且不可或缺的功能?
二、GABARAP亚型
GABARAP亚型蛋白几乎参与自噬全程,在自噬的诱导、自噬小体的形成和自噬小体与溶酶体的融合等阶段均发挥重要作用。在自噬的诱导过程中,自噬可由上游信号的两种不同途径诱导:mTOR失活导致ULK1去磷酸化从而激活自噬,或AMPK激活导致在mTOR不受抑制的情况下ULK1明显磷酸化来抑制自噬[2,3]。Laura Poillet-Perez等人[4]发现GABARAPLI可以通过抑制MTOR活性和AMPK的激活来激活自噬的启动,从而导致ULK1激活。Justin Joachim等人[5]提出GABARAP和GABARAPLI可以激活中心粒细胞质中的ULK1,然后复合物重新定位到生长的吞噬体上。此外,研究人员还发现PIK3C3、BECN1和ATG14包含有功能的LIR序列,可以与ATG8家族蛋白GABARAP亚家族相互作用[6],导致ULK1介导的ATG14的磷酸化,激活PtdIns3K-C1复合体从而产生脂质磷脂酰肌醇-3-磷酸(PI3P)。
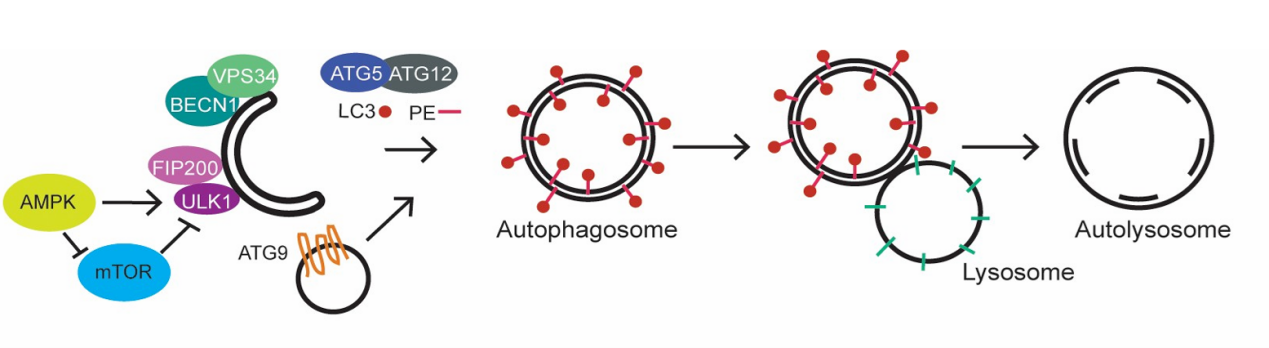
图2. 自噬诱导途径[2]
自噬体的形成是一个复杂的膜扩张和重塑过程。它结合了脂质修饰和运输,蛋白质运输和许多关键的自噬相关(ATG)因子,吞噬体的膜扩张有两种主要机制,其中一种依赖于跨膜蛋白ATG9的活性,而另一种利用ATG8蛋白。ATG8蛋白两个亚家族对自噬小体形成过程均不可或缺,但扮演着不同角色。Weidberg H等人通过联合运用多种实验方法选择性敲除各亚家族,发现GABARAP亚型作用于自噬小体形成后续阶段——可能负责自噬体的密封[7]。
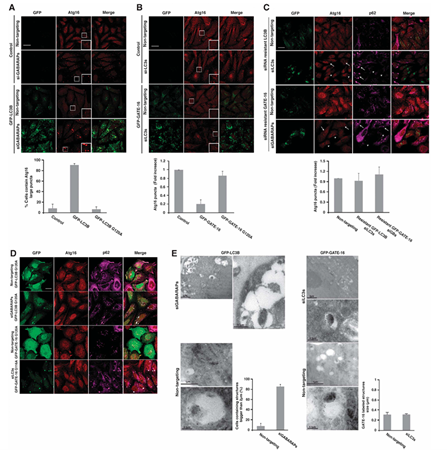
图3. LC3与GABARAP在自噬体生物发生中具有差异化功能[7]
自噬小体与溶酶体融合受几个因素控制,包括SNARE蛋白[8-9]和HOPS复合体。GABARAP优先与PLEKHM1蛋白相互作用,将其招募到自噬结构中,在那里它起到促进HOPS复合体和SNARE蛋白膜融合的功能[10-11]。研究表明,GABARAP可以调节由SNARE组成的膜融合系统的组成成分STX17蛋白的定位,并调节溶酶体的适当酸化以及自噬体和溶酶体之间的融合[12]。此外,GABARAP可以将高尔基体蛋白PI4K2A招募到吞噬体中产生自噬小体与溶酶体融合所必需的磷脂酰肌醇-4-磷酸(PI4P)[13-14]。
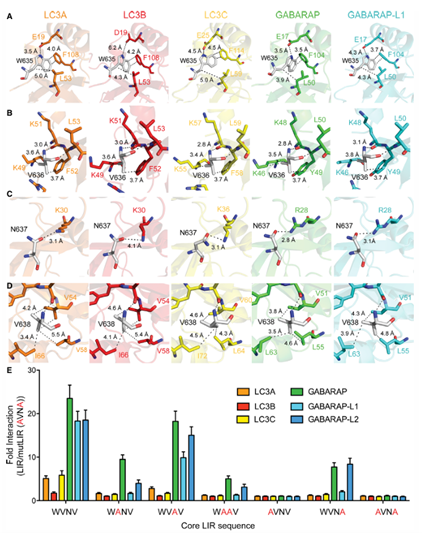
图4. PLEKHM1-LIR关键残基对GABARAP亚家族蛋白选择性结合的作用机制[12]
三、LC3亚型
系统进化分析表明,单细胞生物中的ATG8蛋白在结构上更接近GABARAP亚家族而非LC3亚家族,LC3亚家族是在多细胞动物进化过程中逐渐形成的。LC3亚家族与GABARAP亚家族的功能并非完全等同。例如在自噬体的生物合成过程中。LC3亚家族主要参与吞噬泡膜的延伸过程,而GABARAP亚家族则是参与自噬体成熟的后期阶段。GABARAP亚家族在自噬体与溶酶体融合步骤起到主导作用,但在没有GABARAP蛋白的情况下,LC3蛋白也可以补偿它们的功能。例如,GRASP55蛋白与LC3-II和LAMP2蛋白相互作用于自噬小体、晚期溶酶体,并作为LC3-I蛋白、LAMP2蛋白之间的桥梁,促进自噬体、溶酶体融合[15]。2021年,研究发现LC3蛋白与自噬的一个新的调节因子NIP蛋白共定位,增强了Rab7和FYCO1之间的相互作用,从而加速了自噬通量、自噬溶酶体的形成[16]。
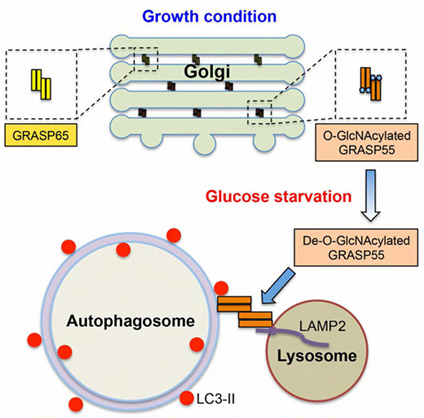
图5. GRASP55与LC3-II和LAMP2的相互作用被募集至自噬体-溶酶体界面,在该处作为膜锚定分子促进自噬体-溶酶体膜融合过程[15]
四、Atg4
Atg4在自噬体形成过程中既介导类泛素样蛋白Atg8与磷脂酰乙醇胺(PE)的结合,又介导Atg8与PE的解离。Atg4在Atg8与PE的结合与解离中发挥着双重作用,有研究者将这个现象描述为“Atg4悖论”(Atg4 paradox)。Atg4最初在芽殖酵母中被鉴定为Atg8唯一且特异的半胱氨酸蛋白酶,在蛋白酶数据库中被归类在CA族C54家族[17]。和Atg8一样,Atg4从酵母到哺乳动物都是进化保守的。酵母中仅有一个Atg4和Atg8基因,但在高等真核生物中往往存在多个Atg4与Atg8同源物,承担着共同的或有所区别的生理功能。人类基因组中具有4个酵母Atg4的同源基因,分别是Atg4B/autophagin-1、Atg4A/autophagin-2、Atg4C/autophagin-3、Atg4D/autophagin-4,分别定位于2、X、1和19号染色体上,分别含有339、398、458和474个氨基酸,它们都具有半胱氨酸蛋白酶催化活性所需要的全部氨基酸残基。
最早报道的Atg4是人类的Atg4B,它由两个结构域组成:木瓜蛋白酶家族半胱氨酸蛋白酶中保守的催化结构域和Atg4特有的插入在催化结构域中的短指结构域[18],Atg8的泛素核心结合在Atg4B两个结构域之间的界面上,其C末端尾巴则延伸到位于催化结构域的活性位点上[19]。Atg4B的催化活性位点由Cys74、Asp278和His280组成,其几何构型与典型的半胱氨酸蛋白酶的催化三联体相对应。Atg4-LC3复合物的晶体结构揭示了Atg4识别Atg8的两种机制:一种是通过N端或C端可变尾上的Atg8-相互作用模体(AIM)[20]或LC3相互作用区(LIR)来识别,另一种则是通过酶体。每个Atg4同源物对特定的Atg8同源物显示出不同的偏好。在底物特异性方面,Atg4B是最复杂且高效的,它可以广泛地处理Atg8家族蛋白酶[21]。Atg4A也是一种有效的蛋白酶,具有靶向GABARAPL2的能力[22]。Atg4C和Atg4D的催化活性较低,需要被caspase介导激活,来增加其对底物酶活性。
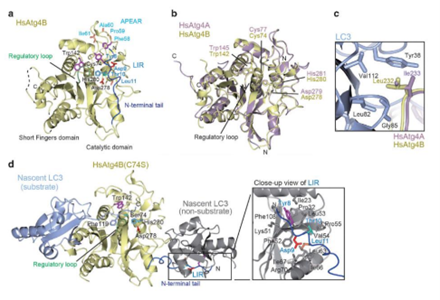
图6. Atg4的结构及其与Atg8的相互作用[23]
五、Atg7
Atg7是自噬核心蛋白中一种具有双重特异性的泛素激活酶(E1),在两个类泛素化系统中发挥关键作用——利用ATP激活自噬相关蛋白中两个远缘相关的类泛素样蛋白Atg12和Atg8,然后将它们分别转移至两个远缘相关的泛素结合酶(E2)Atg10和Atg3上,最后Atg12与Atg5结合,Atg8与磷脂酰乙醇胺(PE)结合。这两个系统对于Atg8与PE的正确连接都是必需的,两个类泛素化系统远缘相关,而Atg7在其中发挥相同的功能。
2011年报道了酿酒酵母Atg7(1-613aa, 全长630aa无法获得晶体)的晶体结构和Atg7 CTD结合Atg8的晶体结构[24]。Atg7包含两个球形结构域——N端结构域(NTD)和C端结构域(CTD),并通过CTD的二聚作用形成同源二聚体,因此它可以装载两个UBLs和两个E2s。两个结构域分别结合Atg8类泛素化系统中不同的自噬相关蛋白,其中Atg7-NTD负责结合远缘相关的E2酶Atg3和Atg10(激活两个远缘相关的UBL也是Atg7的独特特征之一,因为典型的UBL仅激活一个UBL家族),而CTD则负责与类泛素样蛋白Atg8和Atg12结合。
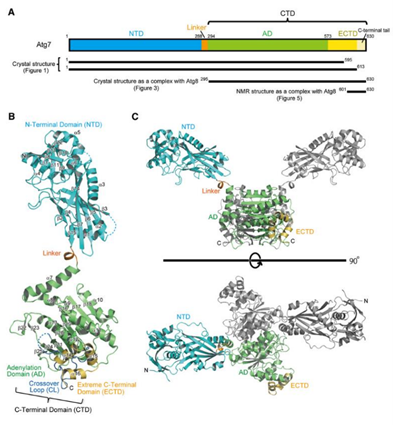
图7. Atg7的结构[23]
Atg7-CTD可被进一步区分为腺苷化结构域(AD)和极端C端结构域(ECTD),腺苷化结构域(AD)具有ATP结合位点和含有催化半胱氨酸(Cys)的交叉环(CL)[25]。研究者通过晶体学和核磁共振分析并结合突变数据提出了Atg7对Atg8的两步识别模型——Atg7-CTD首先利用ECTD的柔性C端尾部捕获Atg8,然后将Atg8转移到AD上,Atg8在AD上被激活[24],但尚未阐明交叉环(CL)的自抑制构象是如何通过Atg8结合被释放并转换成另一种更适宜激活反应的构象。后续研究发现在Atg8活化反应过程中Atg7对Atg8的识别至少包括三个步骤,而且这种多步骤识别是在同一个Atg7原体中进行的:首先,在没有Atg8的状态下,交叉环(CL)与Atg7的中心β片结合以阻止Atg8进入AD,因此Atg8最初无法结合到AD而是结合到Atg7的C端尾部。接着,Atg8会与α17及CL相互作用,在CL中诱导α12’螺旋构象,伴随着CL的其他残基变得柔韧,使AD的中心β片变得可接近。最后,Atg8与中心β片结合,并将其C端尾伸入腺苷化位点,然后CL发生进一步的构象变化,将Atg8的C端尾绑定在中心β片上,使Atg8的Gly116处于结合的ATP的α-磷酸基团附近,促使腺苷化反应发生。
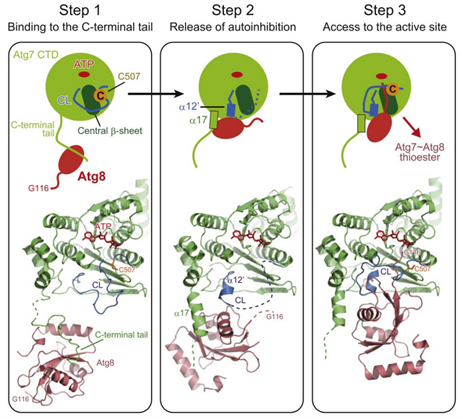
图8. 活化反应中Atg7对Atg8的多步识别模型[23]
六、Atg3
ATG3作为E2样蛋白酶,参与辅助ATG8发生PE化而参与自噬。据酵母细胞ATG3的晶体结构报道显示ATG3具有两个核心区域,其中一个由约80个氨基酸残基组成的无规卷曲,主要负责与E1样蛋白酶ATG7结合,另一个具有α螺旋结构,主要负责与ATG8蛋白结合,可见ATG3蛋白在自噬中扮演着重要的作用。在人类基因组中,ATG3是人类3号染色体上3q13段的一个关键基因,编码E2-同源酶,能促进ATG8样蛋白和磷酯酰乙醇胺(PE)的结合,参与细胞的自噬生成,并在维持线粒体稳态中扮演着重要角色[26]。与具有四个亚型的ATG4和具有三个亚型的ATG16L1不同,生物体中只有一种类型的ATG3,它的氨基酸序列是高度保守的[27]。
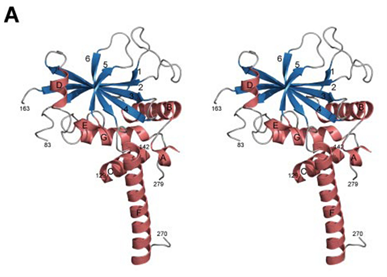
图9. Atg3蛋白带状立体结构图[26]
有日本的学者建立了缺乏ATG3基因编码ATG8特异性E2酶的小鼠,研究结果显示ATG3缺陷小鼠可以出生,但往往在出生后1天内死亡[28]。并且ATG3已被确定为ATG12泛素结合系统的第二个靶标,现有研究发现ATG12–ATG3复合物可调节自噬的早期步骤,而ATG12–ATG3共轭的破坏对线粒体功能有很大影响[29]。ATG12-ATG3复合物形成缺陷会抑制由线粒体途径介导的细胞死亡[30]。还有研究表明ATG3的耗尽会阻止LC3B点状细胞的积聚,并使细胞无法形成脂化的LC3B(LC3B-II),ATG3对促进自噬体形成至关重要[31]。此外,当前研究还发现,ATG3参与许多生理和病理过程,例如肿瘤发生和进展[32],缺血-再灌注损伤[33]和自身免疫疾病[34]等。
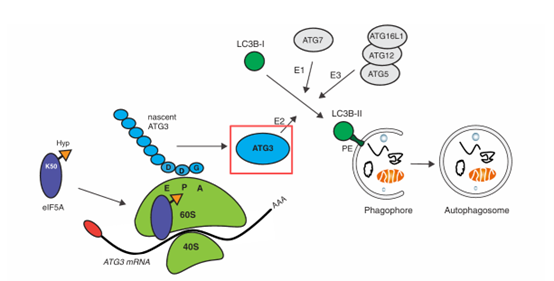
图10. ATG3对促进自噬体形成至关重要[31]
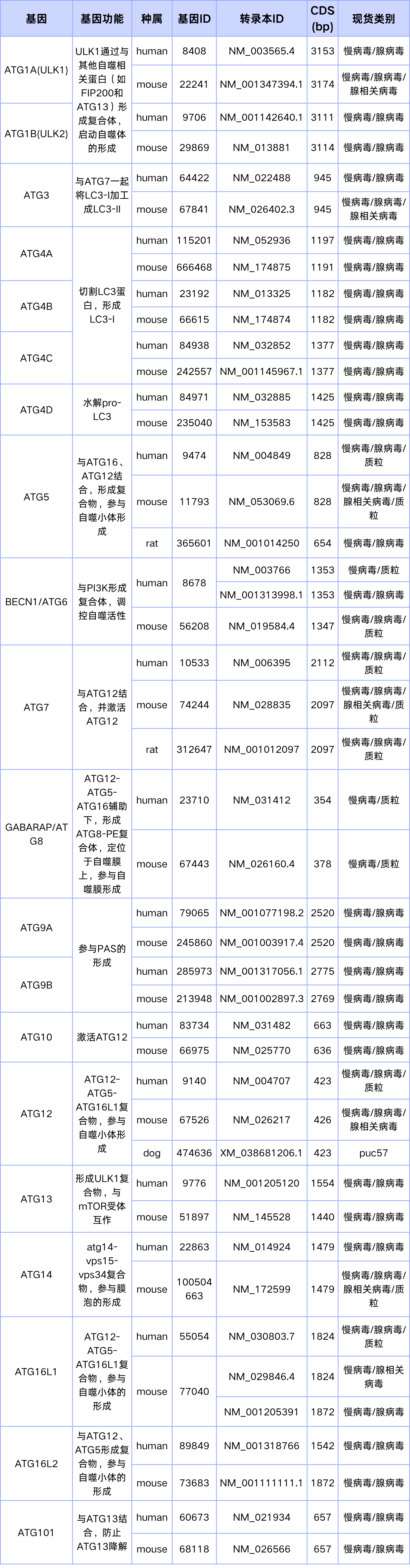
表1. ATG相关基因现货列表
参考文献:
[1] Mizushima N. The ATG conjugation systems in autophagy. Curr Opin Cell Biol. 2020 Apr;63:1-10.
[2] Abernathy E, Mateo R, Majzoub K, et al. Differential and convergent utilization of autophagy components by positive-strand RNA viruses. PLoS Biol. 2019 Jan 4;17(1):e2006926.
[3] Shen HH, Zhang T, Yang HL, et al. Ovarian hormones-autophagy-immunity axis in menstruation and endometriosis. Theranostics. 2021 Jan 19;11(7):3512-3526.
[4] Poillet-Perez L, Jacquet M, Hervouet E, et al. GABARAPL1 tumor suppressive function is independent of its conjugation to autophagosomes in MCF-7 breast cancer cells. Oncotarget. 2017 Jul 27;8(34):55998-56020.
[5] Joachim J, Jefferies HB, Razi M, et al. Activation of ULK Kinase and Autophagy by GABARAP Trafficking from the Centrosome Is Regulated by WAC and GM130. Mol Cell. 2015 Dec 17;60(6):899-913.
[6] Birgisdottir ÅB, Mouilleron S, Bhujabal Z, et al. Members of the autophagy class III phosphatidylinositol 3-kinase complex I interact with GABARAP and GABARAPL1 via LIR motifs. Autophagy. 2019 Aug;15(8):1333-1355.
[7] Weidberg H, Shvets E, Shpilka T, et al. LC3 and GATE-16/GABARAP subfamilies are both essential yet act differently in autophagosome biogenesis. EMBO J. 2010 Jun 2;29(11):1792-802.
[8] Matsui T, Jiang P, Nakano S, et al. Autophagosomal YKT6 is required for fusion with lysosomes independently of syntaxin 17. J Cell Biol. 2018 Aug 6;217(8):2633-2645.
[9] Itakura E, Kishi-Itakura C, Mizushima N. The hairpin-type tail-anchored SNARE syntaxin 17 targets to autophagosomes for fusion with endosomes/lysosomes. Cell. 2012 Dec 7;151(6):1256-69.
[10] Rogov VV, Stolz A, Ravichandran AC, et al. Structural and functional analysis of the GABARAP interaction motif (GIM). EMBO Rep. 2017 Aug;18(8):1382-1396. doi: 10.15252/embr.201643587. Epub 2017 Jun 27. Erratum in: EMBO Rep. 2018 Dec;19(12):e47268.
[11] Brunger AT, Choi UB, Lai Y, et al. Molecular Mechanisms of Fast Neurotransmitter Release. Annu Rev Biophys. 2018 May 20;47:469-497.
[12] Gu Y, Princely Abudu Y, Kumar S, et al. Mammalian Atg8 proteins regulate lysosome and autolysosome biogenesis through SNAREs. EMBO J. 2019 Nov 15;38(22):e101994.
[13] Albanesi J, Wang H, Sun HQ, et al. GABARAP-mediated targeting of PI4K2A/PI4KIIα to autophagosomes regulates PtdIns4P-dependent autophagosome-lysosome fusion. Autophagy. 2015 Nov 2;11(11):2127-2129.
[14] Wang H, Sun HQ, Zhu X, et al. GABARAPs regulate PI4P-dependent autophagosome:lysosome fusion. Proc Natl Acad Sci U S A. 2015 Jun 2;112(22):7015-20.
[15] Zhang X, Wang L, Lak B, et al. GRASP55 Senses Glucose Deprivation through O-GlcNAcylation to Promote Autophagosome-Lysosome Fusion. Dev Cell. 2018 Apr 23;45(2):245-261.e6.
[16] Xiao W, Yeerken D, Li J, et al. Nlp promotes autophagy through facilitating the interaction of Rab7 and FYCO1. Signal Transduct Target Ther. 2021 Apr 16;6(1):152.
[17] Kirisako T, Ichimura Y, Okada H, et al. The reversible modification regulates the membrane-binding state of Apg8/Aut7 essential for autophagy and the cytoplasm to vacuole targeting pathway. J Cell Biol. 2000 Oct 16;151(2):263-76.
[18] Sugawara K, Suzuki NN, Fujioka Y, et al. Structural basis for the specificity and catalysis of human Atg4B responsible for mammalian autophagy. J Biol Chem. 2005 Dec 2;280(48):40058-65.
[19] Satoo K, Noda NN, Kumeta H, et al. The structure of Atg4B-LC3 complex reveals the mechanism of LC3 processing and delipidation during autophagy. EMBO J. 2009 May 6;28(9):1341-50.
[20] Noda NN, Ohsumi Y, Inagaki F. Atg8-family interacting motif crucial for selective autophagy. FEBS Lett. 2010 Apr 2;584(7):1379-85.
[21] Hemelaar J, Lelyveld VS, Kessler BM, et al. A single protease, Apg4B, is specific for the autophagy-related ubiquitin-like proteins GATE-16, MAP1-LC3, GABARAP, and Apg8L. J Biol Chem. 2003 Dec 19;278(51):51841-50.
[22] Scherz-Shouval R, Sagiv Y, Shorer H, et al. The COOH terminus of GATE-16, an intra-Golgi transport modulator, is cleaved by the human cysteine protease HsApg4A. J Biol Chem. 2003 Apr 18;278(16):14053-8.
[23] 赵佳越.自噬核心分子Atg4和Atg7的相互作用[D].四川大学[2025-11-21].
[24] Noda NN, Satoo K, Fujioka Y, et al. Structural basis of Atg8 activation by a homodimeric E1, Atg7. Mol Cell. 2011 Nov 4;44(3):462-75.
[25] Taherbhoy AM, Tait SW, Kaiser SE, et al. Atg8 transfer from Atg7 to Atg3: a distinctive E1-E2 architecture and mechanism in the autophagy pathway. Mol Cell. 2011 Nov 4;44(3):451-61.
[26] Nakatogawa H. Two ubiquitin-like conjugation systems that mediate membrane formation during autophagy. Essays Biochem. 2013;55:39-50.
[27] Hanada T, Satomi Y, Takao T, et al. The amino-terminal region of Atg3 is essential for association with phosphatidylethanolamine in Atg8 lipidation. FEBS Lett. 2009 Apr 2;583(7):1078-83.
[28] Sou YS, Waguri S, Iwata J, et al. The Atg8 conjugation system is indispensable for proper development of autophagic isolation membranes in mice. Mol Biol Cell. 2008 Nov;19(11):4762-75.
[29] Radoshevich L, Debnath J. ATG12-ATG3 and mitochondria. Autophagy. 2011 Jan;7(1):109-11.
[30] Radoshevich L, Murrow L, Chen N, et al. ATG12 conjugation to ATG3 regulates mitochondrial homeostasis and cell death. Cell. 2010 Aug 20;142(4):590-600.
[31] Lubas M, Harder LM, Kumsta C, et al. eIF5A is required for autophagy by mediating ATG3 translation. EMBO Rep. 2018 Jun;19(6):e46072.
[32] Wang H, Zhang Y, Wu Q, et al. miR-16 mimics inhibit TGF-β1-induced epithelial-to-mesenchymal transition via activation of autophagy in non-small cell lung carcinoma cells. Oncol Rep. 2018 Jan;39(1):247-254.
[33] Kong F, Jin J, Lv X, et al. RETRACTED: Long noncoding RNA RMRP upregulation aggravates myocardial ischemia-reperfusion injury by sponging miR-206 to target ATG3 expression. Biomed Pharmacother. 2019 Jan;109:716-725.
[34] Bretin A, Carrière J, Dalmasso G, et al. Activation of the EIF2AK4-EIF2A/eIF2α-ATF4 pathway triggers autophagy response to Crohn disease-associated adherent-invasive Escherichia coli infection. Autophagy. 2016 May 3;12(5):770-83.

查看更多

查看更多

查看更多

联系我们

返回顶部