查看更多

 明星产品
明星产品
 关注我们
关注我们

扫码关注我们
了解更多信息
往期类器官系列干货中,我们介绍了消化道中肠道类器官的结构、功能及应用。而食管作为连接上消化道的关键肌性管道器官,其类器官模型的建立与应用同样展现出巨大的潜力和独特的研究价值。本期小恒将为大家介绍食管类器官的结构和功能、建立基础、建立方法、鉴定及应用。

一、食管的基本结构与功能
食管是连接口腔与胃的管状器官,主要功能是通过肌肉收缩(蠕动)将食物从咽部输送至胃部。其结构复杂,功能多样,由内向外分为四层,其中还包含神经系统,具体结构如下:
1. 黏膜层:包含复层鳞状上皮,由基底细胞层(增殖性祖细胞)和腔细胞层(终末分化细胞)组成,通过增殖、迁移和脱落维持动态平衡;具有屏障功能,抵御机械摩擦和化学刺激。
2. 黏膜下层:富含血管、淋巴管、神经丛及食管腺,为上皮提供营养支持。
3. 肌层:由平滑肌组成,包括内层环形肌和外层纵形肌,通过蠕动推动食物下行。
4. 外膜:食管最外层的薄层结缔组织,与周围组织相连。
5. 食管神经系统:由神经嵴衍生的神经细胞和神经纤维组成,嵌在食管的黏膜下层和肌层中,负责调控食管的肌肉收缩(蠕动)和腺体分泌,以协调食物运输。
然而,人类与小鼠的食管在结构上存在显著差异,一定程度上限制了以小鼠食管作为模型研究人类食管的发育和疾病的适用性。二者的结构差异主要体现在以下五个方面:
表1. 人类和小鼠食管的差异特征比较

基于此,传统食管研究模型的缺陷较为明显,主要包含以下两个方面:
(1)2D细胞培养:无法模拟体内复杂的微环境,细胞间相互作用及基因表达模式与体内差异显著,难以复现食管发育与疾病的病理特征。
(2)动物模型:如表1所述,小鼠食管结构与人类存在差异,且疾病发生机制可能与人类不完全一致,限制了其在食管癌等方面的研究应用。
因此,针对食管类器官的培养开发具有极为重要的科学研究意义和应用前景。
二、食管类器官的建立基础
食管上皮的基底层中存在一个关键的干细胞生态位,其中p63、Sox2是食管干细胞的核心标志物[1]。这些干细胞具有高度的自我更新能力,可通过不对称分裂产生基底层的短暂增殖细胞(Transit-Amplifying Cells,TA细胞)。TA细胞逐渐向上迁移至上层区域,在此过程中分化为食管上皮的多种类型的细胞,以维持上皮的持续更新与损伤修复。人类食管上皮的更新周期约为2周,而干细胞本身的分裂频率约为每24小时一次,以确保上皮结构与功能的完整性。
食管上皮由基底层细胞、中间层细胞和终末分化细胞组成,所有细胞均起源于基底层的p63+Sox2+干细胞[1]:
基底层细胞:高表达p63、Sox2和KRT14等,负责干细胞生态位的维持与增殖。
中间层细胞:p63-Sox2+中间细胞,该状态下的细胞逐渐失去p63,向分化方向发展;此外,在炎症或损伤条件下,可重新进入增殖状态,表现出可塑性特征。
终末分化细胞:表达KRT13、IVL等基因,形成复层鳞状上皮。
三、食管类器官的建立方法及过程
与其它类器官相同,食管类器官的建立可来源于体内分离的原位组织以及多能干细胞(PSC)或胚胎干细胞(ESC)。第一种是利用食管黏膜固有的成体干细胞(如p63+Sox2+基底细胞)在3D培养体系下进行增殖和分化,形成的食管类器官可保留供体遗传背景及生理病理特征,可适用于疾病建模。第二种是利用PSC/ESC的定向分化能力诱导其向食管分化,模拟食管发育过程,结合基因编辑可实现对遗传病的研究。下面以人类组织以及PSC/ESC来源为例,总结两种来源的食管类器官建立过程。
1.人类食管类器官建立过程[2]

图1. 人类食管类器官建立过程
2.人类食管类器官建立过程[2]
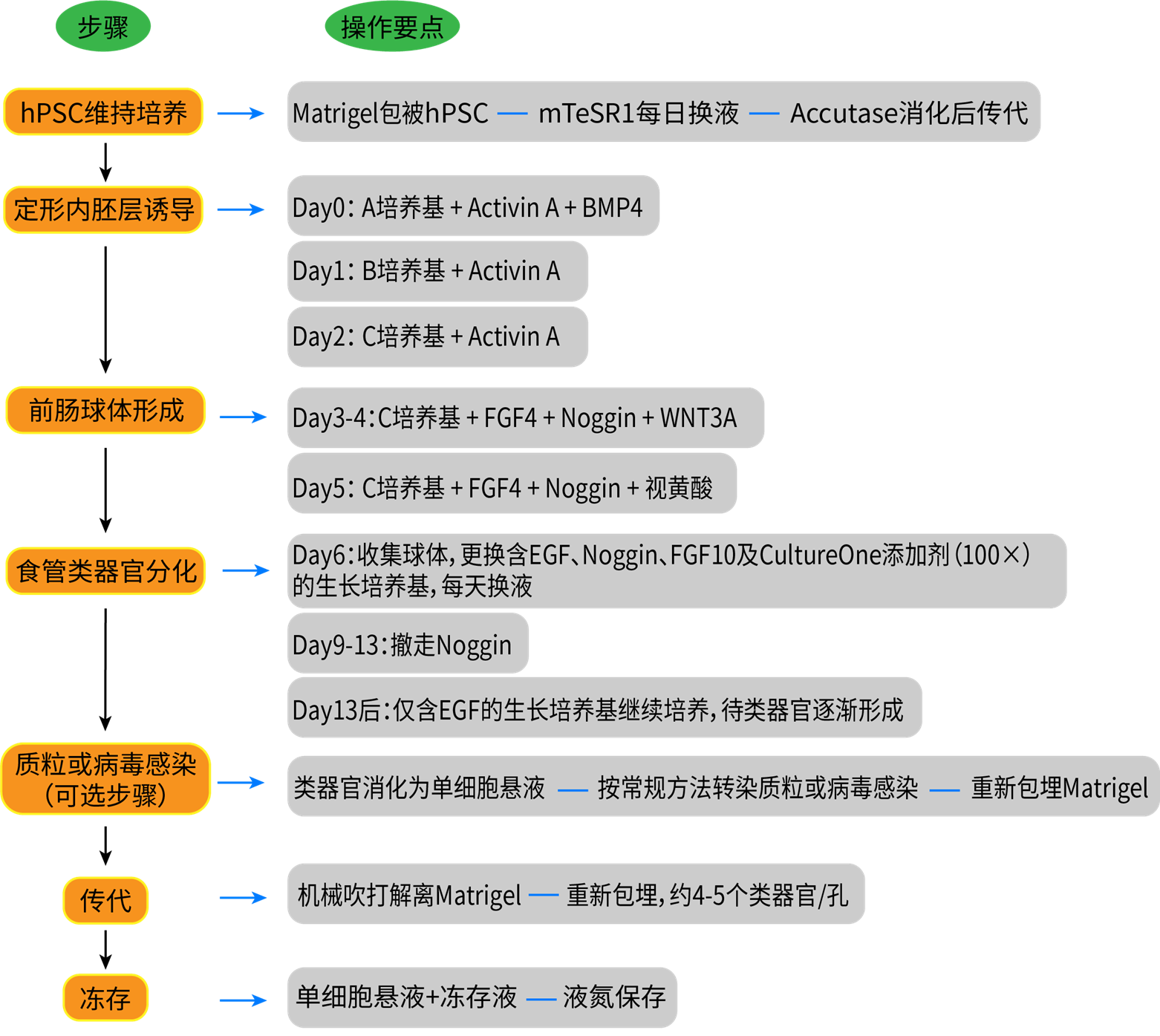
图2. hPSC/ESC来源的食管类器官建立过程

图3. hPSC/ESC来源的食管类器官的不同培养基成分
四、食管类器官的鉴定
食管类器官的鉴定主要通过形态学分析和分子标记物检测等方式进行。
1.形态学鉴定
可通过H&E染色等组织学染色观察食管类器官的结构特征,确认其是否模拟体内食管上皮的分层结构:
(1)正常食管类器官[2]:H&E染色呈实心球形结构,可见典型的分层鳞状上皮结构,即外侧有一层基底细胞层,内侧有2-3层大的基底上细胞层,管腔内有角化层。
(2)食管相关肿瘤类器官[2]:常见食管鳞状细胞癌(ESCC)的类器官,呈现不规则形态,源自低分化ESCC类器官可能无法形成角化层。
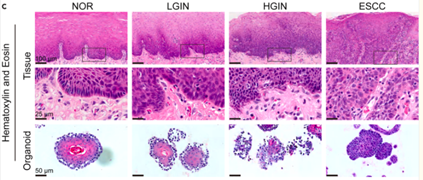
图4. H&E染色观察人食管及ESCC类器官形态[2]
2.分子标记物检测
还可通过Western Blot、qPCR及免疫染色等方法检测食管上皮的标志物,以确认类器官的细胞类型和分化状态[4, 5]:
(1)基底细胞标志物:p63、Krt5、Krt14、Sox2等;
(2)分化细胞标志物:Krt4、Krt13、Sox2等;
(3)其他关键标志物(增殖标志):Ki67等。

图5. 免疫荧光染色观察食管类器官标志物[5]
五、食管类器官的应用
1.基因表达载体
质粒、慢病毒和腺病毒等基因表达载体已被应用于调控食管类器官特定基因的表达,对揭示ESCC等疾病机制和潜在防治靶点提供了有力的工具平台。
1.1 质粒:研究使用pcDNA3.1载体在食管类器官中过表达ANXA1,通过电穿孔转染和G418筛选成功建立稳定的表达模型[6]。结果显示ANXA1过表达可促进细胞衰老,抑制食管类器官的增殖和生长,进而延缓肿瘤生长,由此揭示了ANXA1在抑制ESCC中起关键作用[6]。
1.2 慢病毒:慢病毒在食管类器官模型中实现了高效的基因编辑和功能研究。Zhao等[6]通过慢病毒介导的Crispr/Cas9系统成功敲除人食管类器官的KMT2C,导致类器官形态学改变为囊性结构。同时,采用慢病毒递送shRNA以敲低CDKN1B的表达,逆转了ANXA1过表达诱导的细胞衰老和生长抑制,明确了CDKN1B-ANXA1轴在ESCC发生发展中的作用。另有研究利用慢病毒在食管类器官中过表达TPM4,揭示了TPM4通过调控JAK/STAT-SOX2通路促进ESCC的恶性发展,为临床预后评估和靶向治疗提供了新的理论依据[7]。
1.3 腺病毒:目前,腺病毒在食管类器官中的应用案例较少,已有研究主要用于介导Cre重组酶的表达。Natsuizaka等[8]使用携带Cre和GFP的腺病毒以MOI值500感染Notchloxp/loxp小鼠来源的食管类器官,介导Notch1基因的特异性敲除,进而发现Notch1缺失显著降低了类器官的形成率,并下调了内皮间质转化标志物的表达,最终成功模拟Notch1的促癌作用。
2.疾病建模[9]
2.1 食管腺癌(EAC)
通过患者来源类器官精准模拟EAC的病理特征。例如,Li等[10]利用手术切除的EAC组织构建类器官,证实其保留原发肿瘤的形态学、基因组变异(如驱动基因一致性)和转录组特征,为研究肿瘤异质性提供平台。类器官结合CRISPR-Cas9技术成功模拟Wnt信号异常激活,揭示该通路促进Barrett食管(BE)向EAC转化的机制,即Wnt激活加速BE类器官的增殖、抑制凋亡[10]。此外,有研究表明EAC类器官模型中炎症微环境对促癌的关键作用,基质细胞中NF-κB信号驱动了食管癌前微环境的形成[11, 12]。但EAC的起源尚未完全明确,有研究提出可能起源于胃贲门区的BE样上皮[13]。
2.2 ESCC类器官
ESCC是食管癌的主要类型,在亚洲人群中发病率高且生存率较低。与EAC不同,ESCC的细胞起源相对明确,源于增殖基底细胞的恶性转化。类器官已成为研究ESCC分子机制的有效平台。Kajiwara等[14]研究发现DKK3蛋白通过结合CKAP4受体促进ESCC类器官的增殖。Wu等[15]利用基因工程食管类器官证明SOX2过表达联合p53/p16失活可触发染色体重塑,激活促癌基因的表达。此外,乙醇是ESCC的主要风险因素,研究发现在食管类器官与异种移植瘤模型中,乙醇代谢会诱导氧化应激、线粒体功能障碍及非CD44H+细胞凋亡,而CD44H+细胞通过自噬抵抗损伤并促进肿瘤复发,为ESCC防治提供了新思路[16]。
2.3 嗜酸性粒细胞食管炎(EoE)
EoE是一种由食物过敏原诱发的炎症性疾病,其特征表现为吞咽困难和进食障碍,病理特征则以嗜酸性粒细胞浸润和基底细胞增生为主,这会破坏食管上皮屏障的完整性。而食管类器官成功模拟了Th2炎症反应及上皮屏障的破坏过程。Nakagawa等[17]用IL-13等细胞因子刺激人和小鼠食管类器官,重现EoE典型病理改变。机制上,有研究发现EoE患者来源的类器官中IL-20亚家族信号异常,导致角蛋白分化相关基因表达下调,破坏了上皮屏障完整性,靶向抑制该通路可恢复屏障功能。还有研究揭示了日常化学用品对EoE的诱导,即使用洗涤剂刺激食管类器官后,诱导了IL-33释放,并引起上皮增殖和嗜酸性粒细胞聚集[18]。
总结来说,食管类器官作为一种3D研究模型,克服了传统2D细胞培养和动物模型的局限性,高度模拟了体内食管的结构和功能特征。通过利用患者组织或干细胞定向分化构建的类器官,不仅保留了供体的遗传背景和病理特性,还为深入解析食管发育、疾病机制及药物筛选提供了高效平台。在基因表达调控、疾病建模及个性化医疗中的应用,已显著推动了对食管癌变机制、炎症微环境调控和靶向治疗策略的研究,有望在转化医学和精准治疗中发挥更关键的作用。
汉恒生物专注于病毒包装服务,可提供基因表达调控的各类病毒载体,包括慢病毒、腺病毒和腺相关病毒;此外,还可提供质粒构建服务。如果您有相关需求或疑问,欢迎拨打汉恒生物服务热线400-092-0065,我们有专业的技术团队为您服务。后续我们还将发布更多科研干货内容,敬请期待!
参考文献:
[1]. Yu, X., H. Yuan, Y. Yang, et al. Mammalian esophageal stratified tissue homeostasis is maintained distinctively by the epithelial pluripotent p63(+)Sox2(+) and p63(-)Sox2(+) cell populations. Cell Mol Life Sci, 2023, 80(10): 305.
[2]. Zhang, S., G. Cheng, S. Zhu, et al. Protocol for the generation, characterization, and functional assays of organoid cultures from normal and cancer-prone human esophageal tissues. STAR Protoc, 2024, 5(4): 103316.
[3]. Shacham-Silverberg, V. and J.M. Wells. Generation of esophageal organoids and organotypic raft cultures from human pluripotent stem cells. Methods Cell Biol, 2020, 159(1-22.
[4]. Zhang, Y., Y. Yang, M. Jiang, et al. 3D Modeling of Esophageal Development using Human PSC-Derived Basal Progenitors Reveals a Critical Role for Notch Signaling. Cell Stem Cell, 2018, 23(4): 516-529 e5.
[5]. Zheng, B., K.P. Ko, X. Fang, et al. A new murine esophageal organoid culture method and organoid-based model of esophageal squamous cell neoplasia. iScience, 2021, 24(12): 103440.
[6]. Zhao, H., Y.M. Park, Y. Zheng, et al. Genetically Defined Organoid Models Reveal Mechanisms Driving Squamous Cell Neoplastic Evolution and Identify Potential Therapeutic Vulnerabilities. bioRxiv, 2025,
[7]. Pan, X., J. Wang, L. Guo, et al. Identifying a confused cell identity for esophageal squamous cell carcinoma. Signal Transduct Target Ther, 2022, 7(1): 122.
[8]. Natsuizaka, M., K.A. Whelan, S. Kagawa, et al. Interplay between Notch1 and Notch3 promotes EMT and tumor initiation in squamous cell carcinoma. Nat Commun, 2017, 8(1): 1758.
[9]. Liu, H. and X. Wang. Esophageal organoids: applications and future prospects. J Mol Med (Berl), 2023, 101(8): 931-945.
[10]. Li, X., H.E. Francies, M. Secrier, et al. Organoid cultures recapitulate esophageal adenocarcinoma heterogeneity providing a model for clonality studies and precision therapeutics. Nat Commun, 2018, 9(1): 2983.
[11]. Anand, A., H.Y. Fang, D. Mohammad-Shahi, et al. Elimination of NF-kappaB signaling in Vimentin+ stromal cells attenuates tumorigenesis in a mouse model of Barrett's Esophagus. Carcinogenesis, 2021, 42(3): 405-413.
[12]. Kunze, B., F. Wein, H.Y. Fang, et al. Notch Signaling Mediates Differentiation in Barrett's Esophagus and Promotes Progression to Adenocarcinoma. Gastroenterology, 2020, 159(2): 575-590.
[13]. Nowicki-Osuch, K., L. Zhuang, S. Jammula, et al. Molecular phenotyping reveals the identity of Barrett's esophagus and its malignant transition. Science, 2021, 373(6556): 760-767.
[14]. Kajiwara, C., K. Fumoto, H. Kimura, et al. p63-Dependent Dickkopf3 Expression Promotes Esophageal Cancer Cell Proliferation via CKAP4. Cancer Res, 2018, 78(21): 6107-6120.
[15]. Wu, Z., J. Zhou, X. Zhang, et al. Reprogramming of the esophageal squamous carcinoma epigenome by SOX2 promotes ADAR1 dependence. Nat Genet, 2021, 53(6): 881-894.
[16]. Shimonosono, M., K. Tanaka, S. Flashner, et al. Alcohol Metabolism Enriches Squamous Cell Carcinoma Cancer Stem Cells That Survive Oxidative Stress via Autophagy. Biomolecules, 2021, 11(10):
[17]. Nakagawa, H., Y. Kasagi, T.A. Karakasheva, et al. Modeling Epithelial Homeostasis and Reactive Epithelial Changes in Human and Murine Three-Dimensional Esophageal Organoids. Curr Protoc Stem Cell Biol, 2020, 52(1): e106.
[18]. Doyle, A.D., M.Y. Masuda, G.C. Pyon, et al. Detergent exposure induces epithelial barrier dysfunction and eosinophilic inflammation in the esophagus. Allergy, 2023, 78(1): 192-201.

查看更多

查看更多

查看更多

联系我们

返回顶部