查看更多

 明星产品
明星产品
 关注我们
关注我们

扫码关注我们
了解更多信息
在前几期内容中,小恒为大家介绍了肠类器官、肺类器官、肝类器官的发展历程、培养构建方法、病毒感染技术及其应用。本期我们将聚焦于脑类器官(Brain organoids)。

人类中枢神经系统(Central nervous system, CNS)是一个高度动态且极其复杂的器官,由约上千亿个神经元和上万亿个支持性神经胶质细胞以高度有序的方式排列组成。由于伦理限制和样本获取难度,直接利用人脑组织进行研究面临很大挑战。此外,人脑结构高度复杂,长期以来缺乏能够全面模拟其结构与功能的理想模型。
随着干细胞研究的进展,科学家们成功开发出一种三维(Three-dimensional, 3D)培养体系——脑类器官。它来源于人胚胎干细胞(Human embryonic stem cells, hESCs)或人诱导多能干细胞(Human induced pluripotent stem cells, hiPSCs),在结构和功能上与人脑高度相似。因此,脑类器官已成为研究大脑发育、生理功能及相关疾病机制的重要替代模型,为该领域带来了全新的研究手段。
脑类器官发展历程
1907年,Wilson[1]首次观察到海绵细胞的自组织能力,这为后续类器官研究奠定了早期基础。随着干细胞技术的兴起与发展,脑类器官研究领域迎来了两个里程碑式的突破:Martin[2]等人成功从小鼠胚胎中分离出多能干细胞,以及Takahashi与Yamanaka[3]发现重编程因子,实现了体细胞向多能干细胞的诱导转化。随后,Zhang[4]等学者证实胚胎干细胞能够形成神经玫瑰花结结构,这一结构是生成脑类器官的关键中间阶段。2005年,Yoshiki Sasai[5]团队首创无血清悬浮培养法(Serum-free culture of embryoid body-like quick-aggregation, SFEBq),通过添加神经分化诱导因子,成功将小鼠胚胎干细胞分化为端脑组织。
2013年,Lancaster等人[6]利用旋转生物反应器提升气体与营养交换效率,并将诱导分化的胚胎体包埋于基质胶中进行振荡培养,最终在神经分化培养基中形成包含多个脑区的脑类器官,标志着三维脑类器官培养体系的正式建立。此后,脑类器官技术逐步向更高仿生度的方向发展,陆续出现了血管化脑类器官(2018年)以及人源皮质脑类器官移植等进展(2022年),为研究大脑发育及相关疾病提供了更为有效的模型系统。
脑类器官技术的产生具有重要意义:它不仅弥补了传统二维培养在模拟脑组织复杂结构与体内微环境方面的不足,克服了二维体系难以再现神经系统疾病复杂表型的局限;同时也突破了动物模型因缺乏人类特有遗传特征、脑区结构与功能而无法真实模拟人脑发育与疾病进程的瓶颈。目前,脑类器官已成为在体外研究人脑发育与进化、探究脑区及脑器官间相互作用、以及开展疾病模拟与药物筛选的关键工具。
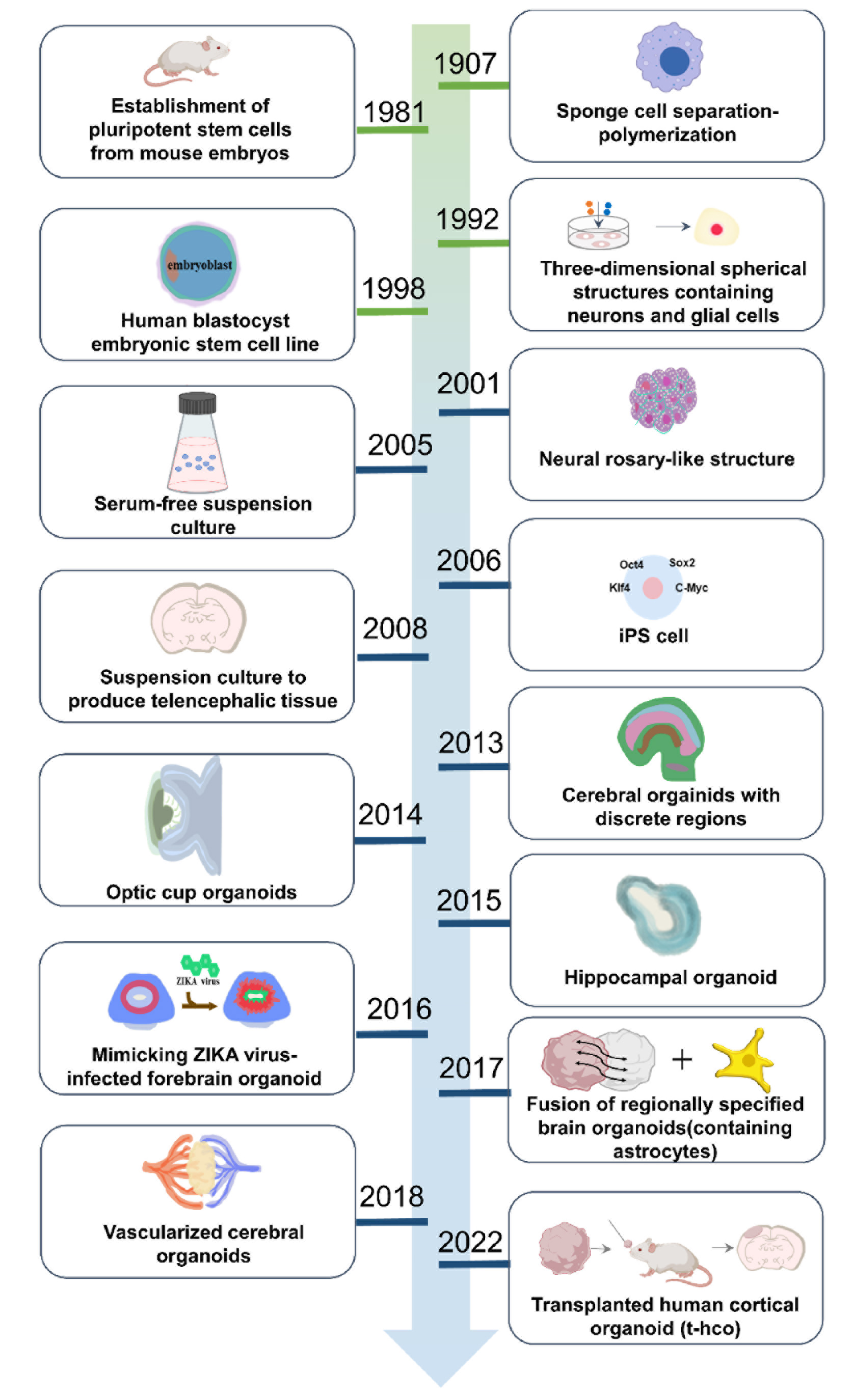
图1 脑类器官发展的历史进程和里程碑[7]
脑类器官的建立
脑类器官具有与大脑相似的细胞组成和解剖结构,能够模拟大脑的发育过程,并体现其生理、病理及药理等方面的特征。在胚胎发育过程中,神经管逐渐形成三个初级囊泡,这些囊泡最终发育为整个大脑。从头至尾依次分化为前脑、中脑与后脑,其中前脑进一步发育为端脑、间脑和视神经泡。在脑类器官的培养过程中,这些大脑区域能够自发形成,无需依赖外源性模式因子引导神经分化。根据分化策略的不同,目前的脑类器官系统主要分为两类:非定向分化(无引导)脑类器官和定向分化(引导)脑类器官[8]。
非定向分化主要依赖于人多能干细胞聚集体的自发形态发生及内在信号传导潜力,生成包含多种细胞谱系、具有多个离散大脑区域组织的脑类器官,并展现人类皮层发育的基本特征,例如在脑室样区域中出现丰富的放射状胶质细胞。而定向分化则通过添加特定小分子和生长因子来引导神经分化,形成主要代表某一特定脑区的细胞类型与结构。
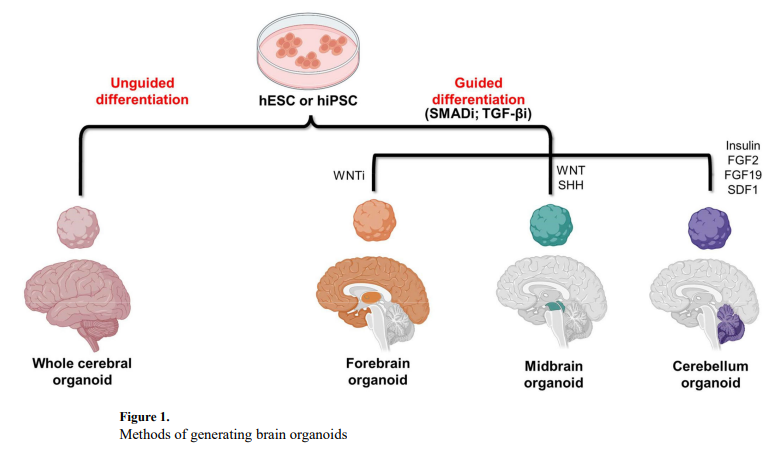
图2 脑类器官系统[8]
全脑类器官构建流程 [9-12]
1.hiPSC/hESC 培养与接种
在6孔板中培养人诱导多能干细胞(hiPSC)或人胚胎干细胞(hESC)克隆,待细胞汇合度达70%–80%时进行消化,将其制备为单细胞悬液。将细胞接种至低贴壁96孔板,每孔约接种9000个活细胞,随后放回培养箱中继续培养。
2.胚胎体形成
培养24 h后,可在显微镜下观察到边界清晰的小型胚胎体(Embryoid body, EB)。继续培养5–7 d,期间每隔一天轻柔吸弃约一半体积的旧培养基,并补充等量新鲜培养基。
3.诱导原始神经上皮形成
当EB直径达500–600 µm、边缘平滑且透亮度增加时,将其转移至低贴壁24孔板中,使用神经诱导培养基培养。48 h后更换新鲜的神经诱导培养基,继续培养4–5 d,可见神经上皮结构出现。
4.基质胶包埋与神经上皮芽扩增
将含有神经上皮的组织转移至基质胶(Matrigel)液滴中,置于二氧化碳培养箱内培养。24 h后镜下观察,可见组织被基质胶完整包埋。继续培养1–3 d,神经上皮组织将形成更多向外扩展的神经上皮芽,内部可见充满液体的腔状结构。继续孵育24 h后,将包埋组织的基质胶滴转移至不含维生素A的脑类器官分化培养基中,静置培养48 h。
5.脑类器官成熟培养
静置培养4 d后,将类器官转移至含维生素A的脑类器官分化培养基中,置于可旋转式器官培养瓶内,并放入培养箱中继续动态培养。
6.长期维持与观察
在动态培养过程中,摇床培养体系每3–4 d全量更换一次培养基,旋转培养瓶体系每周更换一次。培养期间需持续监测类器官的形态变化与生长状态。

图3 脑类器官培养流程[10]

图4 hPSCs诱导的脑类器官发育进程[10]

图5 不同培养阶段脑类器官形态[10]
中脑类器官构建流程 [13-14]
1.hiPSC 培养与胚胎体形成
在6孔板中培养人诱导多能干细胞(hiPSC)克隆,待细胞汇合度达70%–80%时进行消化,将其制备为单细胞悬液,接种至低贴壁96孔板(每孔约9000个活细胞),每日更换培养基,直至细胞融合度达到约80%。
2.神经诱导
第0–5天:将hiPSC在化学成分限定培养基(CDM)中培养,培养基中添加SB431542、NAC及AMP活化蛋白激酶抑制剂Compound C,以促进胚胎体形成。第6天:将形成的胚胎体转移至10 cm无粘附培养皿中,置于37 ℃、5% CO₂条件下,以85 rpm振荡培养,避免细胞聚集。
3.中脑定向模式化
第7天:更换为含100 ng/mL FGF8b的CDM培养基,继续在轨道摇床中培养。第8–13天:每2天更换一次培养基,每日镜下观察形态变化。第14天:更换为含100 ng/mL FGF8b及1 μM 模式化因子的CDM培养基,继续振荡培养。第15–20天:每2天更换培养基,每日观察。
4.基质胶包埋与中脑类器官成熟
将胚胎体包埋于基质胶(Matrigel)中,转移至含脑源性神经营养因子(BDNF)和胶质细胞系源性神经营养因子(GDNF)的CDM培养基中,进行后续分化与成熟培养,最终获得成熟的中脑类器官。

图6 iPSC分化流程图及iPSC衍生的MO在分化和表征过程中的代表性图[13]
表1.不同区域的脑类器官构建方法
脑类器官的感染方法
脑类器官的培养过程与人类胎儿大脑的发育步骤高度相似,因此能有效模拟具有明确病因的神经发育障碍,并可用于模拟脑类疾病的进展,进而实现药物筛选。在这些研究中,基因表达调控工具发挥着关键作用,能够精准操纵脑类器官中特定基因的表达水平,构建更具针对性的疾病模型,从而为深入解析大脑疾病的发病机制以及开发新型治疗策略提供创新路径。
基因表达载体的选择对脑类器官的感染至关重要。目前,慢病毒载体、腺病毒载体和腺相关病毒载体是用于类器官基因表达调控的三大主要工具,各自具备不同特点和适用范围:
慢病毒载体:可将目的基因整合至宿主基因组,实现长期稳定表达,适用于类器官的稳定基因编辑及致癌基因建模。
腺病毒载体:可携带较大外源DNA片段,转导效率高,适用于难以转染的原代类器官。
腺相关病毒载体:免疫原性极低,可实现长期表达,适用于需低毒性长期表达的实验及临床转化研究,如体内移植类器官。
腺病毒和慢病毒感染脑类器官的具体步骤可参考前面几期的干货内容,这里我们主要介绍腺相关病毒载体(AAV)感染脑类器官的操作流程[20-21]:
1.将成熟(培养30–50天)的脑类器官转移至低贴壁96孔板中。
2.向每个类器官加入适量AAV病毒悬液(通常为10¹⁰–10¹¹ VG)。
3.在37℃、5% CO₂条件下孵育1小时,使病毒充分吸附。
4.将类器官转移至6孔板,每孔加入3 mL类器官成熟培养基。
5.持续感染3天,期间病毒与类器官共培养。
6.感染后第3天和第7天更换培养基,以去除未感染病毒并维持类器官状态,继续培养至所需时间点。
7.通过免疫荧光染色、Western blot或直接荧光观察等方式检测目标蛋白表达及感染效率。
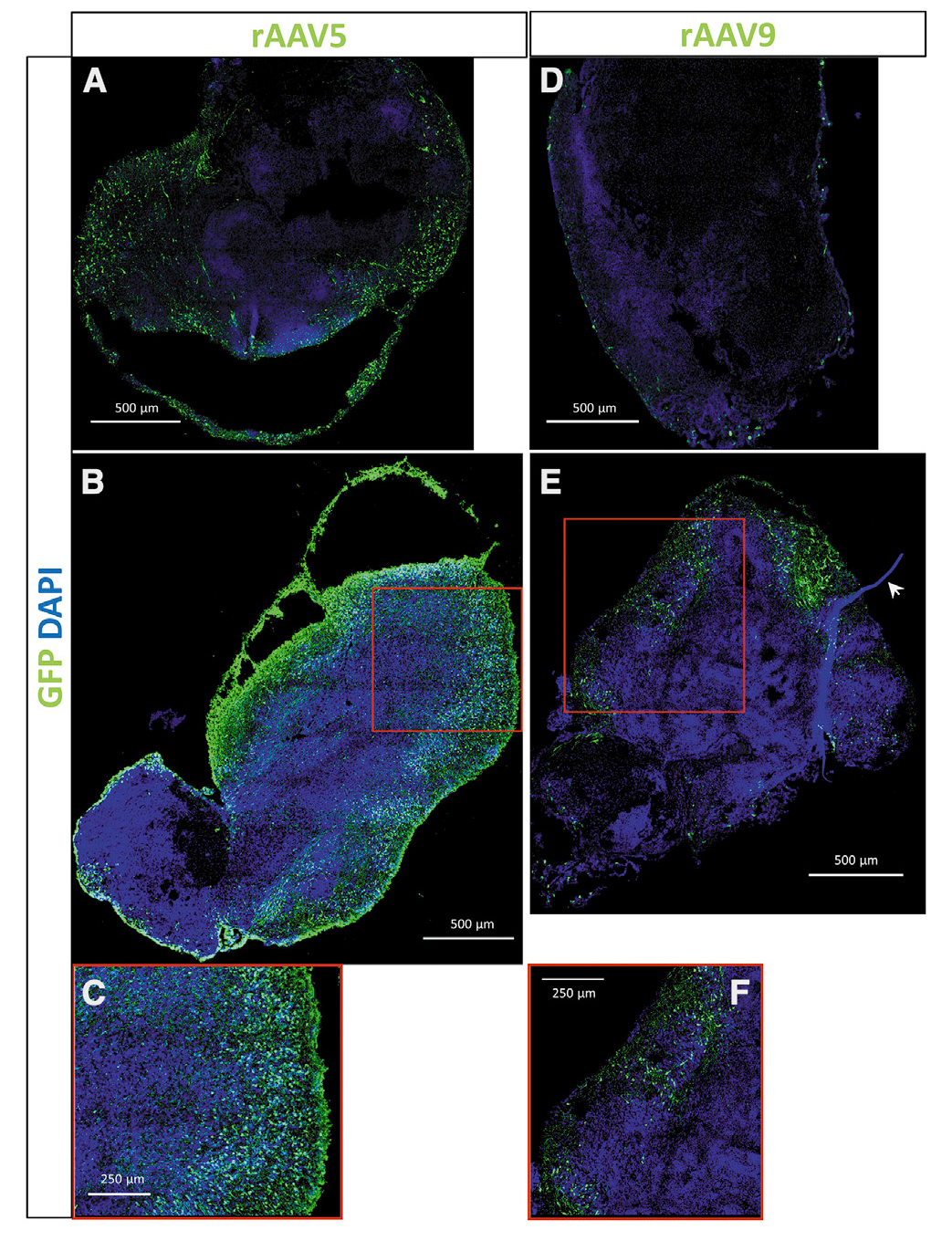
图7 不同血清型感染脑类器官荧光观察[20]

图8 不同剂量AAV(PHP.B)感染脑类器官荧光观察[21]
脑类器官的研究应用
体外培养的脑类器官作为一种简化的三维细胞模型,便于获取与操作,能够有效模拟人脑特定的空间结构、细胞多样性及神经网络功能。该技术在医学领域展现出广阔的应用前景:不仅可作为研究神经系统疾病的理想模型和药物筛选平台,也为推动个性化医疗策略及探索器官移植新途径提供了重要的研究基础与方法支持。
1.疾病模型构建
类器官已被广泛用于模拟多种神经系统疾病,包括神经退行性疾病、精神类疾病及脑损伤等,为揭示疾病发生与损伤机制提供了有力工具。以最常见的神经退行性疾病——阿尔茨海默病(Alzheimer's disease, AD)为例,研究认为血脑屏障(blood-brain barrier, BBB)功能受损导致大脑暴露于血清环境,是AD发病的关键机制之一。Chen等[22]通过将脑类器官暴露于血清,模拟散发性AD的病理过程,发现该模型可重现AD的多种典型特征,如β-淀粉样蛋白(Aβ)沉积、磷酸化tau蛋白水平升高、突触丢失及神经网络功能失衡等。此外,Wang等[23]采用氧糖剥夺(oxygen-glucose deprivation, OGD)处理脑类器官,通过检测cleaved-caspase-3表达与细胞凋亡等指标,建立了缺血性损伤与OGD暴露时间的关联模型,并以此验证了依达拉奉、丁基邻苯二甲酸酯等药物的神经保护作用,表明该模型在缺血性脑卒中研究中具有良好的可行性。
表2.使用神经类器官模拟神经系统疾病的研究

2.药物筛选与药效评价
人类疾病研究常受限于个体差异、结果不可预测及药物测试周期长等因素。源于患者的脑类器官能够再现与临床表型相似的病理特征,因而有望成为高效的新药检测平台。2023年1月,《Science》报道美国食品药品监督管理局(FDA)不再强制要求新药进行动物试验即可获批[29],这为类器官、器官芯片等替代模型的发展提供了重要契机。例如,Mesci等[30]利用SARS-CoV-2感染脑类器官,观察到神经元死亡增加和兴奋性突触丧失等类似临床的病理变化。在AD药物筛选方面,Park等[31]结合数学模型与AD脑类器官的病理特征,开发了一套基于网络的高内涵药物筛选平台,并成功筛选出多个可减少Aβ/tau沉积或具有神经保护作用的候选化合物。
3.个性化医疗
基于患者特异性诱导多能干细胞(iPSC)构建的脑类器官,为实现个体化治疗提供了新途径。通过建立携带患者特定遗传背景的类器官模型,可预测个体对药物的反应,从而指导临床用药决策。在脑肿瘤研究中,已有两项研究将胶质母细胞瘤患者对药物的实际治疗反应与其来源的脑肿瘤类器官模型的药敏结果进行对比,均显示出高度的一致性[32-33],表明该类器官模型在个体化用药指导中具有潜在价值。

图9 与脑肿瘤共培养的大脑类器官的建立及其应用[33]
4.脑类器官移植
器官移植虽是治疗组织损伤或器官衰竭的有效手段,但因伦理、免疫排斥、供体短缺以及人脑结构功能特殊等问题,针对脑区的移植研究长期受限。脑类器官具有与体内组织相似的结构和细胞类型,可在病灶部位替代受损脑组织,且由自体iPSC分化而来的类器官移植后排斥风险较低。2018年,研究人员首次将人脑类器官移植至NOD-SCID免疫缺陷小鼠的大脑皮层,发现14天内小鼠血管可浸润到植入的类器官中,与体外培养相比,体内环境显著提高了类器官细胞的成熟与存活率[34]。同时,移植的类器官能够长出广泛轴突,并与宿主小鼠神经元建立功能性连接[34]。2022年,研究人员将人皮质类器官移植至新生无胸腺大鼠的体感皮层区域,经过6个多月的整合,该类器官成功融入大鼠神经环路,并可调控其神经元活动与行为反应[35]。这些进展表明,脑类器官移植有望克服体外培养体系的局限,为神经系统疾病的再生治疗开辟新的前景。
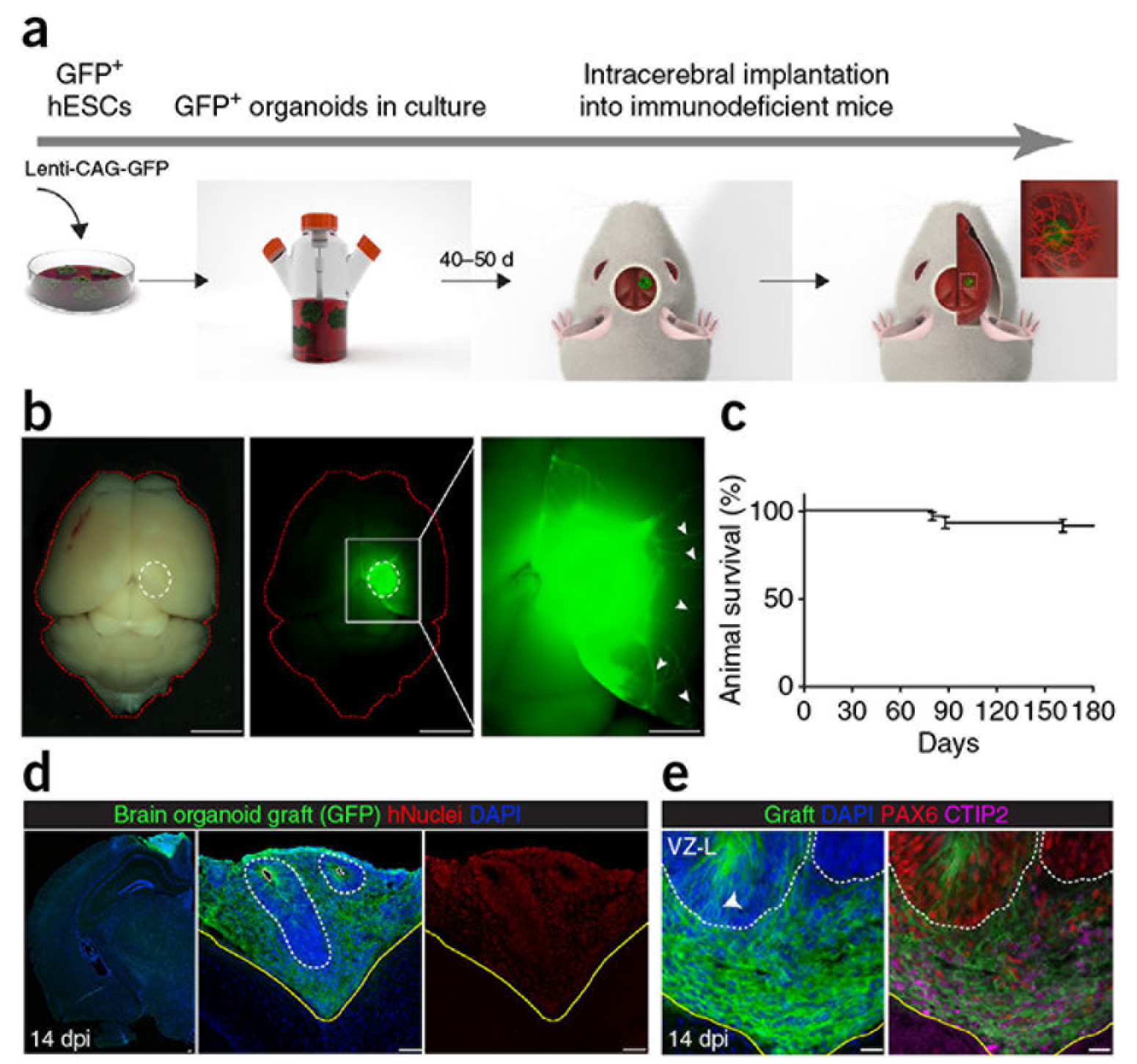
图10 将人脑类器官移植入小鼠脑内[34]
本文系统梳理了脑类器官的发展历程、构建技术、病毒感染模型及其在脑疾病研究与医学中的应用进展。当前,脑类器官技术虽已在科研与医学领域展现出重要潜力,但仍面临诸多挑战,例如存在批次差异、可重复性不足,以及体内外发育进程不一致等问题。此外,如何构建具备更复杂、更成熟神经网络功能的脑类器官,仍是未来需要深入探索的方向。下期我们将对食管类器官的相关内容进行分享,欢迎大家关注~!
参考文献:
[1] Wilson H V. On some phenomena of coalescence and regeneration in sponges[J]. Journal of the Elisha Mitchell Scientific Society, 1907, 23(4): 161-174.
[2] Martin G R. Isolation of a pluripotent cell line from early mouse embryos cultured in medium conditioned by teratocarcinoma stem cells[J]. Proceedings of the National Academy of Sciences, 1981, 78(12): 7634-7638.
[3] Takahashi K, Yamanaka S. Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors[J]. cell, 2006, 126(4): 663-676.
[4] Zhang S C, Wernig M, Duncan I D, et al. In vitro differentiation of transplantable neural precursors from human embryonic stem cells[J]. Nature biotechnology, 2001, 19(12): 1129-1133.
[5] Watanabe K, Kamiya D, Nishiyama A, et al. Directed differentiation of telencephalic precursors from embryonic stem cells[J]. Nature neuroscience, 2005, 8(3): 288-296.
[6] Lancaster M A, Renner M, Martin C A, et al. Cerebral organoids model human brain development and microcephaly[J]. Nature, 2013, 501(7467): 373-379.
[7] Zhao Y, Wang T, Liu J, et al. Emerging brain organoids: 3D models to decipher, identify and revolutionize brain[J]. Bioactive Materials, 2025, 47: 378-402.
[8] Acharya P, Choi N Y, Shrestha S, et al. Brain organoids: A revolutionary tool for modeling neurological disorders and development of therapeutics[J]. Biotechnology and Bioengineering, 2024, 121(2): 489-506.
[9] Martens Y A, Xu S, Tait R, et al. Generation and validation of APOE knockout human iPSC-derived cerebral organoids[J]. STAR protocols, 2021, 2(2): 100571.
[10] Lancaster M A, Knoblich J A. Generation of cerebral organoids from human pluripotent stem cells[J]. Nature protocols, 2014, 9(10): 2329-2340.
[11] Zhao J, Fu Y, Yamazaki Y, et al. APOE4 exacerbates synapse loss and neurodegeneration in Alzheimer’s disease patient iPSC-derived cerebral organoids[J]. Nature communications, 2020, 11(1): 5540.
[12] Mayhew C N, Singhania R. A review of protocols for brain organoids and applications for disease modeling[J]. STAR protocols, 2023, 4(1): 101860.
[13] Mayhew C N, Singhania R. A review of protocols for brain organoids and applications for disease modeling[J]. STAR protocols, 2023, 4(1): 101860.
[14] Zagare A, Gobin M, Monzel A S, et al. A robust protocol for the generation of human midbrain organoids[J]. STAR protocols, 2021, 2(2): 100524.
[15] Zagare A, Gobin M, Monzel A S, et al. A robust protocol for the generation of human midbrain organoids[J]. STAR protocols, 2021, 2(2): 100524.
[16] Jgamadze D, Lim J T, Zhang Z, et al. Structural and functional integration of human forebrain organoids with the injured adult rat visual system[J]. Cell stem cell, 2023, 30(2): 137-152. e7.
[17] Sarrafha L, Neavin D R, Parfitt G M, et al. Novel human pluripotent stem cell-derived hypothalamus organoids demonstrate cellular diversity[J]. iScience, 2023, 26(9).
[18] Muguruma K, Nishiyama A, Kawakami H, et al. Self-organization of polarized cerebellar tissue in 3D culture of human pluripotent stem cells[J]. Cell reports, 2015, 10(4): 537-550.
[19] Pellegrini L, Bonfio C, Chadwick J, et al. Human CNS barrier-forming organoids with cerebrospinal fluid production[J]. Science, 2020, 369(6500): eaaz5626.
[20] Pellegrini L, Bonfio C, Chadwick J, et al. Human CNS barrier-forming organoids with cerebrospinal fluid production[J]. Science, 2020, 369(6500): eaaz5626.
[21] Cho A N, Bright F, Morey N, et al. Efficient gene expression in human stem cell derived-cortical organoids using adeno associated virus[J]. Cells, 2022, 11(20): 3194.
[22] Chen X, Sun G, Tian E, et al. Modeling sporadic Alzheimer's disease in human brain organoids under serum exposure[J]. Advanced Science, 2021, 8(18): 2101462.
[23] Wang S, Wang Z, Wang X, et al. Humanized cerebral organoids-based ischemic stroke model for discovering of potential anti-stroke agents[J]. Acta Pharmacologica Sinica, 2023, 44(3): 513-523.
[24] Zhao J, Ikezu T C, Lu W, et al. APOE deficiency impacts neural differentiation and cholesterol biosynthesis in human iPSC-derived cerebral organoids[J]. Stem Cell Research & Therapy, 2023, 14(1): 214.
[25] Paulsen B, Velasco S, Kedaigle A J, et al. Autism genes converge on asynchronous development of shared neuron classes[J]. Nature, 2022, 602(7896): 268-273.
[26] Kim H, Park H J, Choi H, et al. Modeling G2019S-LRRK2 sporadic Parkinson's disease in 3D midbrain organoids[J]. Stem Cell Reports, 2019, 12(3): 518-531.
[27] Bian S, Repic M, Guo Z, et al. Genetically engineered cerebral organoids model brain tumor formation[J]. Nature methods, 2018, 15(8): 631-639.
[28] Xu Y P, Qiu Y, Zhang B, et al. Zika virus infection induces RNAi-mediated antiviral immunity in human neural progenitors and brain organoids[J]. Cell research, 2019, 29(4): 265-273.
[29] Wadman M. FDA no longer has to require animal testing for new drugs[J]. Science, 2023, 379(6628): 127-128.
[30] Mesci P, de Souza J S, Martin-Sancho L, et al. SARS-CoV-2 infects human brain organoids causing cell death and loss of synapses that can be rescued by treatment with Sofosbuvir[J]. PLoS biology, 2022, 20(11): e3001845.
[31] Park J C, Jang S Y, Lee D, et al. A logical network-based drug-screening platform for Alzheimer’s disease representing pathological features of human brain organoids[J]. Nature Communications, 2021, 12(1): 280.
[32] Loong H H F, Wong A M, Chan D T M, et al. Patient-derived tumor organoid predicts drugs response in glioblastoma: A step forward in personalized cancer therapy?[J]. Journal of Clinical Neuroscience, 2020, 78: 400-402.
[33] Wen J, Liu F, Cheng Q, et al. Applications of organoid technology to brain tumors[J]. CNS Neuroscience & Therapeutics, 2023, 29(10): 2725-2743.
[34] Mansour A A F, Gonçalves J T, Bloyd C W, et al. An in vivo model of functional and vascularized human brain organoids[J]. Nature biotechnology, 2018, 36(5): 432-441.
[35] Mansour A A F, Gonçalves J T, Bloyd C W, et al. An in vivo model of functional and vascularized human brain organoids[J]. Nature biotechnology, 2018, 36(5): 432-441.

查看更多

查看更多

查看更多

联系我们

返回顶部