查看更多

 明星产品
明星产品
 关注我们
关注我们

扫码关注我们
了解更多信息
疫苗对于保护人类免受长期存在或新出现的传染病威胁至关重要。然而,疫苗开发滞后问题对于全球公共卫生仍是巨大的挑战。通常,全病毒疫苗(如衰减或灭活疫苗)可直接将强毒病毒转化为疫苗。但由于其存在免疫力降低、安全不确定性及制作耗时长等问题,阻碍了它们的广泛应用。而持续出现的新病毒使安全有效的即用型疫苗成为疫苗研发的重要方向。
2023年3月23日,浙江大学唐睿康、王晓雨及军事医学研究院侯利华作为共同通讯作者在Nature Biomedical Engineering(IF=29.234)在线发表了题为“Immunization against Zika by entrapping live virus in a subcutaneous self-adjuvanting hydrogel”的研究结果,本研究展示了一种病毒包埋水凝胶(virus-entrapping hydrogel,命名为Vax),它由作为病毒捕获剂和内置佐剂的壳聚糖低聚物水凝胶(COS)以及作为稳定剂和Ca2+来源的碳酸钙纳米颗粒 (Nano-CaCO3)组成。带正电侧链的壳聚糖支架可通过静电相互作用有效地捕获病毒,同时其自辅助特性可以通过激活模式识别受体(PRRs)来激活先天免疫反应和细胞募集。因此水凝胶为病毒捕获及抗原加工提供了炎症微环境,这对淋巴结中的抗原呈递起到了促进作用,由于生发中心(GC)B细胞的扩大和交叉呈递的改善,最终激发了有效的体液和细胞免疫。在没有任何预处理的前提下,直接包埋活性病毒作为安全且有效的疫苗,这对于新型的传染病是一种很有前景的预防策略。值得注意的是,本研究使用了汉恒生物提供的腺病毒作为模型病毒。
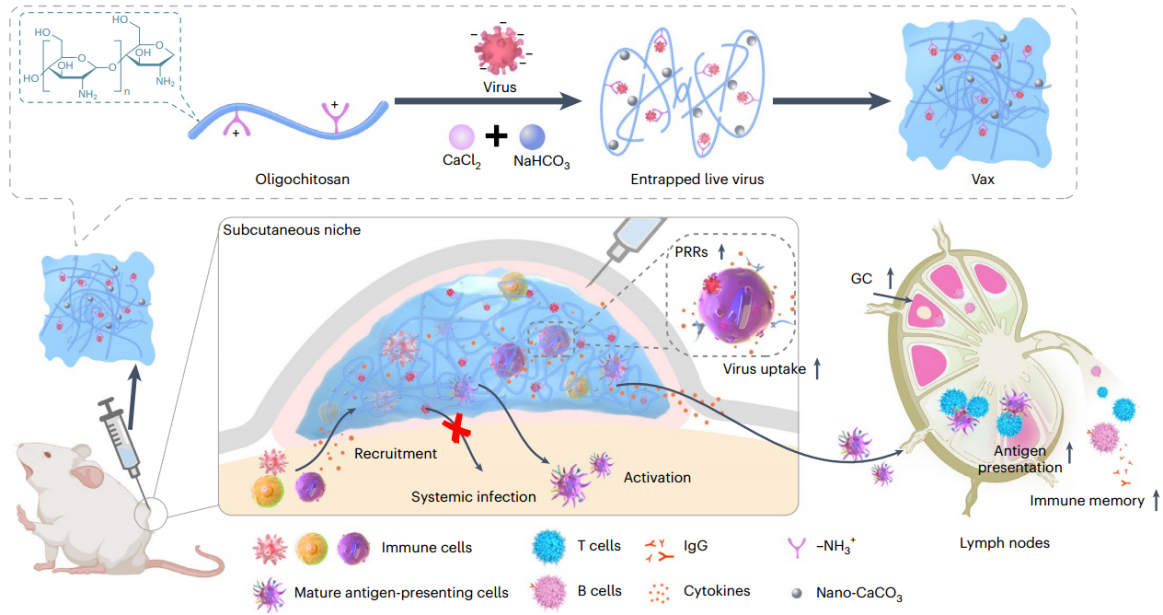
图1. 病毒包埋水凝胶(Vax)示意图
下面我们一起来看看具体的研究结果:
本研究首先利用Ad5进行模型病毒包埋水凝胶制作,通过温度扫描研究了Vax的热凝胶行为,即研究其在不同温度下的力学性能,结果证实了Vax包埋病毒作为疫苗的可行性。同时检测到其对Ad5封装效率超过99%。为研究Vax包埋病毒作为疫苗的安全性,检测37 ℃条件下Vax在体外和体内对病毒的禁闭效应,结果显示在体外模拟体内生理条件及不同pH溶液中,Vax对病毒释放都表现出限制作用;利用缺乏干扰素受体的IFNAR1-/-小鼠作为感染模型,分别皮下注射野生型寨卡病毒(WT/ZIKV)及由Vax包埋的ZIKV(Vax/ZIKV),结果显示WT/ZIKV组小鼠血清及其他受测器官中均检测到病毒血症,且最终死亡率为50%;Vax/ZIKV组小鼠仅在注射部位检测到病毒RNA积聚,且在4-8周内完全清除,在其血清及受测器官中均未检测到病毒血症,最终存活率为100%,表明由Vax包埋的ZIKV无法建立全身性感染。而后通过向出生1天的BALB/c小鼠分别颅内注射WT/ZIKV和Vax/ZIKV检测其神经毒性。感染WT/ZIKV的小鼠表现出明显的神经系统症状,接种后23 d死亡率为100%。而注射Vax/ZIKV的小鼠死亡率为0,仅出现轻微神经系统症状,表明Vax包埋病毒具有良好的安全性。同时,还通过注射空Vax研究了其可能出现的毒性,结果表明在注射前期引起了急性炎症,但并未增加小鼠血清中炎症细胞因子的水平,且浸润的炎症细胞数量也快速恢复了正常水平,另外注射后未出现明显的形态学细胞毒性变化。
以上结果表明Vax可有效地限制病毒感染,且在体内表现出最小的毒性,证明了其作为疫苗的安全性能。
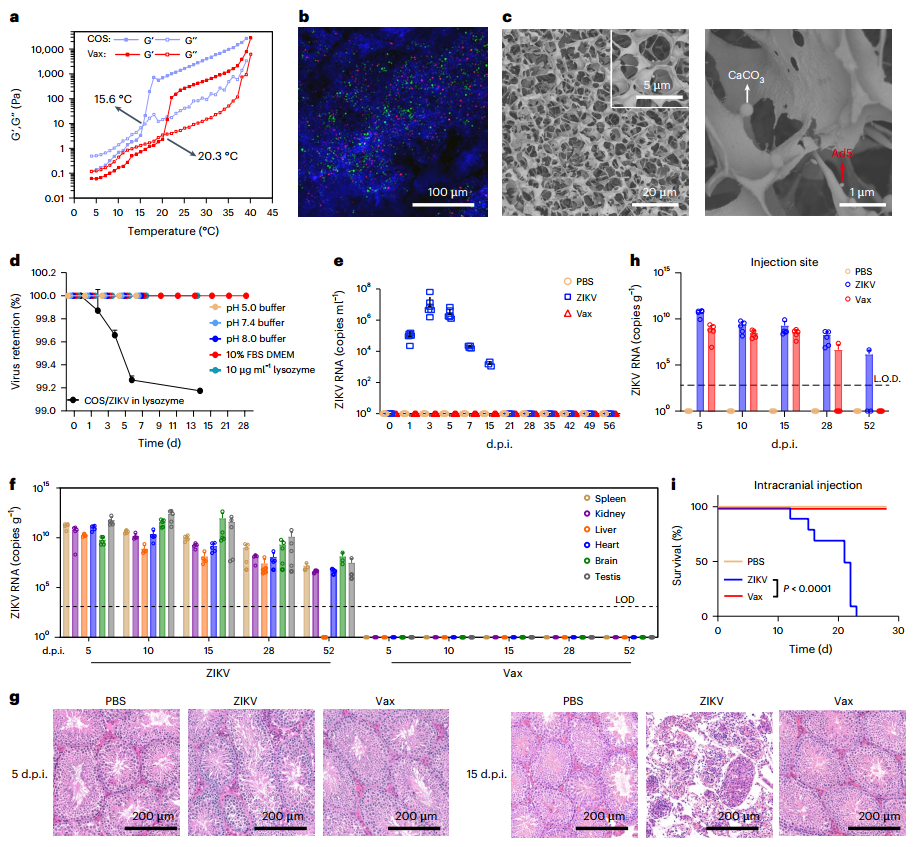
图2. Vax的表征及安全性研究
本研究利用RNA测序技术探究了Vax对RAW 264.7细胞差异表达基因的影响,结果发现一些PRRs的转录本发生上调。为了进一步揭示Vax对PRRs的影响,在使用小鼠骨髓来源树突状细胞BMDC和RAW 264.7细胞与Vax共孵育后发现CR3、CD14以及TLR4显著上调,表明Vax包埋病毒对PRR激活表现出协同效应,Vax治疗后激活了先天免疫反应。而后又进一步研究了Vax对促炎细胞因子的诱导作用,结果显示与空白对照组和Ad5组相比,COS/CaCO3、COS/Ad5和Vax组的促炎细胞因子分泌增强,表明COS对促炎反应有积极作用。另外Vax对先天免疫应答的刺激也促进了趋化因子的产生,而趋化因子利于免疫细胞的募集。综上结果,Vax激活了相应的先天免疫反应,且PPRs的刺激是其激活先天免疫反应的机制之一,机体在Vax注射位置形成炎症微环境,抗病毒防御。
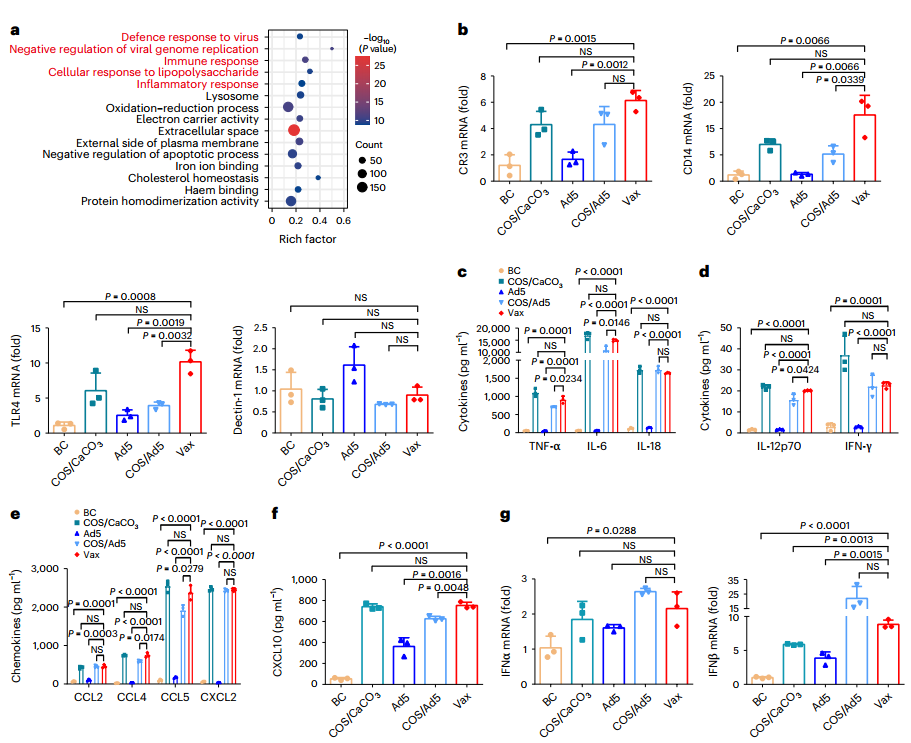
图3. Vax通过激活PRRs刺激局部先天免疫反
为评估Vax是否有助于细胞迁移,本研究采用了体外Transwell实验,结果显示与其他实验组相比Vax处理的BMDCs迁移数量最多,表明趋化因子增强了细胞募集。另外,通过皮下注射将Vax注射到BALB/c小鼠的腹部右侧,结果显示Vax组较其他实验组募集了更多的细胞。通过H&E染色和扫描电镜观察发现,注射部位募集的细胞大部分包埋在结节内并保持正常的细胞功能。通过流式细胞术分析表明Vax募集的大部分为抗原呈递细胞(APCs),能够处理Vax中包埋的病毒。以上结果表明Vax可促进抗原呈递细胞在注射部位募集,Vax对抗原呈递有促进作用。
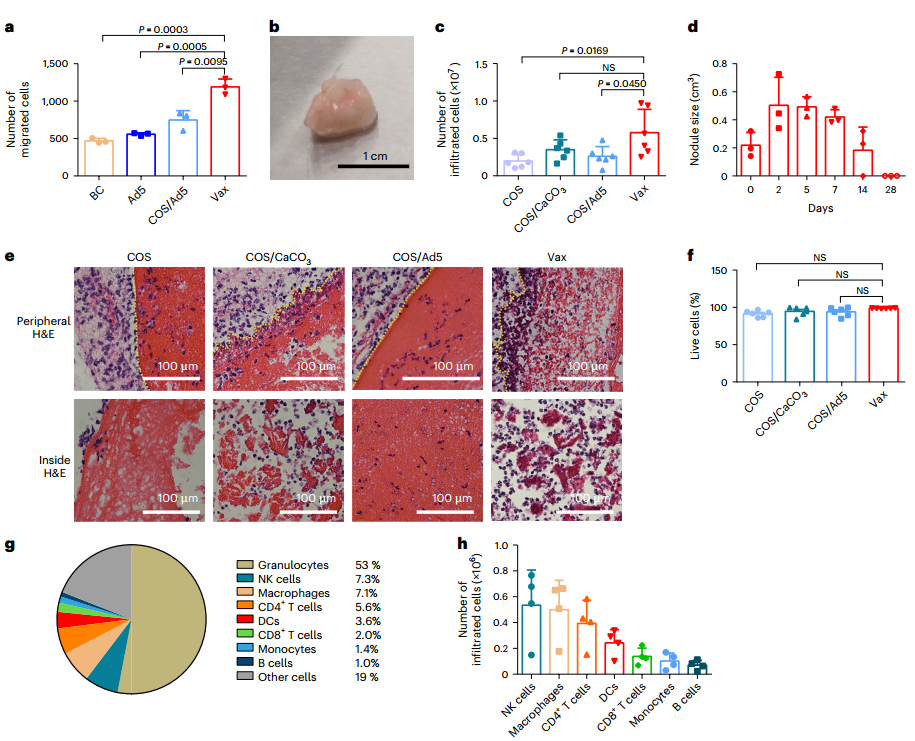
图4. 注射Vax后免疫细胞的募集情况
为探究病毒和Vax在体外共同驱动局部免疫反应活化和抗原呈递的作用,作者利用荧光标记的Vax/Ad5与BMDCs共孵育,结果显示Ad5和Vax在细胞质中表现为共定位,而对照组Ad5的摄取效率较低,表明Vax对细胞摄取病毒产生积极响应。另外,在BMDCs摄取Vax后,Ad5和Nano-CaCO3的存在对细胞活化标志物(CD80等)上调显示出显著的协同效应。为了测试Vax环境下抗原生成的局部过程,作者在Vax中装载了卵清蛋白(OVA),并分析了抗原肽通过BMDCs上MHC-I途径的呈递状况。结果显示Vax能够促使细胞产生大量的高表达SIINFEKL-MHC-I+和CD11c+的BMDCs,反映局部DC活化和抗原呈递。为评估注射包埋病毒的Vax是否能有效引发宿主细胞的适应性免疫反应,本研究使用抗六邻体抗体检测Ad5的定位,结果显示注射Vax的结节中Ad5阳性细胞数量明显高于其他组;通过Ad5-Luc的荧光素酶转导效率反映病毒转导活性,结果表明Vax包埋病毒注射组可保证较高的病毒转导活性,吞噬效率低和细胞浸润程度小的其他实验组则表现为病毒转导活性受损。通过注射野生型病毒和Vax包埋病毒观察注射位置病毒RNA水平及DC细胞的浸润情况,结果表明Vax包埋对病毒有一定的储存效应,但一段时间后病毒会被原位清除。而在注射Vax后形成的结节内可观察到大量DC细胞的浸润,表明Vax包埋的病毒注射有效激活了宿主抗原呈递的过程。
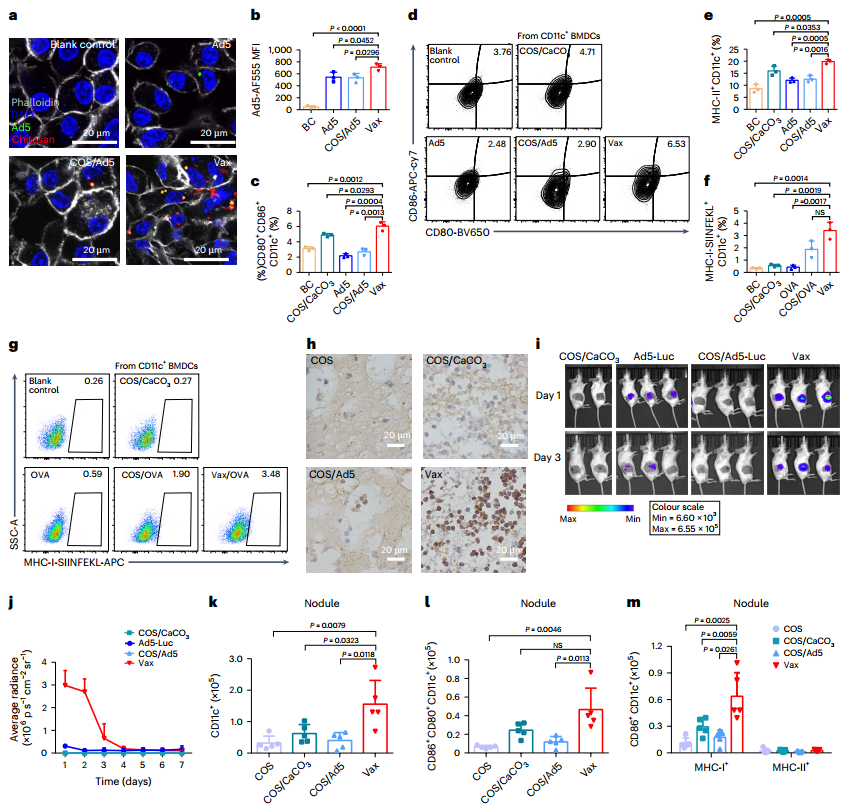
图5. Vax驱动局部免疫反应活化和抗原呈递的情况
确定注射Vax能有效地启动抗原呈递后,作者继续评估了单次接种疫苗的后续适应性应答。研究将含有ZIKV前膜-包膜蛋白的Ad5载体装载至Vax(Ad5-prM-E-Vax)中,在第4 ~ 6周检测到显著增强的E蛋白特异性IgG反应,且PRNT50滴度持续了6周,表明装载病毒的Vax可增强体液免疫作用,具备免疫保护效力。接种2周后通过流式细胞术检测到ZIK-E特异性CD4+和CD8+ T细胞增多。综上结果,Vax提高了细胞免疫和体液免疫反应的产生,表明APCs从结节迁移到淋巴结。
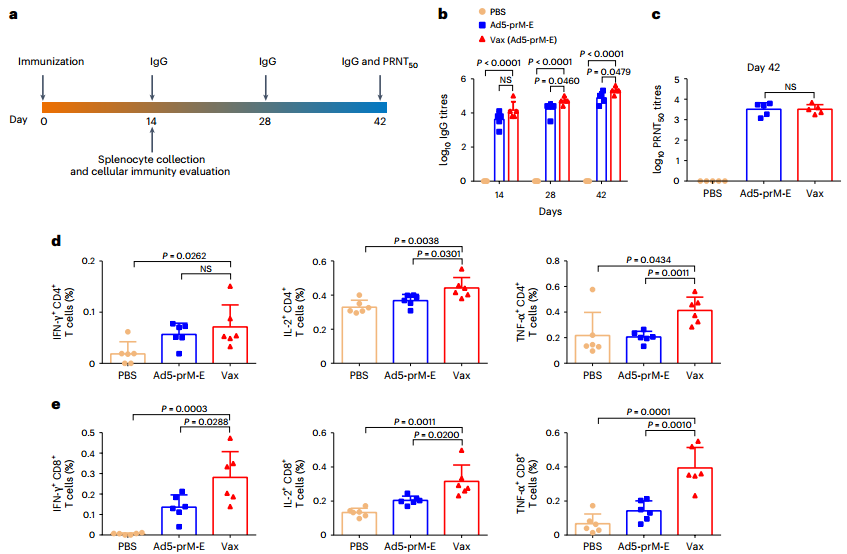
图6. 接种Ad5-prM-E-Vax后的全身免疫反应
为解析Vax增强淋巴结免疫反应并作用于全身的机制,作者研究检测了Vax在引流淋巴结(dLN)中启动抗原呈递的能力。结果显示接种Vax后dLNs中表达CD80+和CD86+ 的DCs数量显著增加;为了测试dLNs中的抗原呈递,注射装载OVA的Vax(Vax/OVA),结果显示表达MHC-II+和CD40+ DC细胞的数量显著增加,证实了DC细胞的活化成熟,有利于随后T细胞的激活。此外,Vax增强了OVA肽在MHC-I上的呈递,可以通过MHC-I途径交叉呈递抗原到CD8+ T细胞。因此,本研究使用OVA四聚体染色检测接种后dLNs中CD8+ T细胞数量,结果显示OVA-Vax使OVA四聚体+、CD8+ T细胞的数量急剧增加,这有助于抗原特异性的细胞毒性CD8+ T细胞应答。
另外,本研究测试了Vax介导生发中心B细胞激活的能力,通过免疫荧光和流式细胞术检测GCs高水平表达Fas和N-糖基神经氨酸(GL7抗体检测)情况。分析显示,Vax/Ad5组GC阳性细胞数量较其他组成倍增加。切片结果显示,在该实验组中观察到高度组织的GC结构,表明Vax对dLNs中B细胞的下游活化起促进作用。综上所述,Vax能够通过增强交叉呈递和GC激活来激活T细胞反应和体液反应。
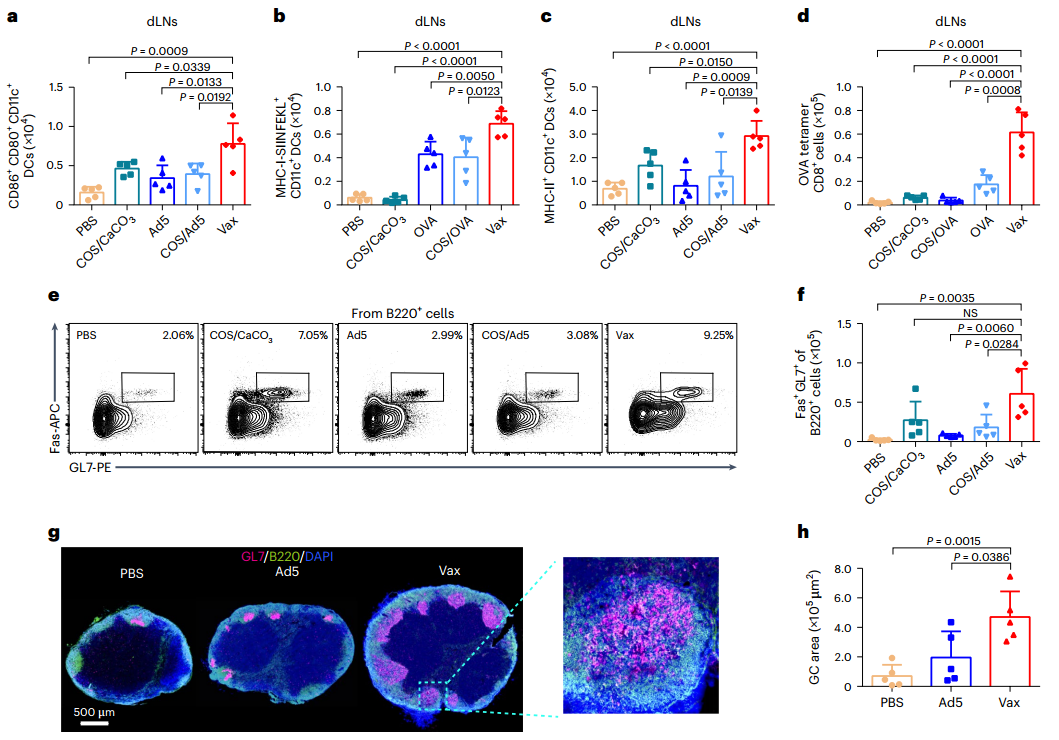
图7.淋巴结免疫活化检测
最后,为了验证Vax将野生型病毒转化为有效疫苗的可能性,本研究以ZIKV致病株为例,研究了Vax/ZIKV对致命ZIKV攻击的体内保护作用。4~6周龄IFNAR1−/−小鼠接受单次皮下疫苗接种。结果显示与灭活ZIKV(iZIKV)相关组相比,Vax/ZIKV组小鼠产生更快、更高的ZIKV E特异性血清IgG反应和中和滴度。皮下免疫后,所有组的小鼠在免疫后第29天感染WT ZIKV。结果显示,与Vax/ZIKV组相比,iZIKV相关组小鼠体重显著减轻。在Vax/ZIKV和Ad5-prM-E组小鼠未观察到发病率和死亡率,而在其他组中观察到约20-70%的死亡率。
综上结果表明,将灭活的ZIKV添加到Vax中或在iZIKV中添加佐剂无法获得与活病毒包埋至Vax等效的保护作用,显示出Vax装载活病毒与传统疫苗佐剂技术和病毒灭活策略相比的优势。总体来说Vax是一种安全的材料,基于此生产的疫苗在消除病毒传染性的同时增强了机体的免疫反应,从而实现病毒到疫苗的转化

查看更多

查看更多

查看更多

联系我们

返回顶部