查看更多

 明星产品
明星产品
 关注我们
关注我们

扫码关注我们
了解更多信息
神经组织的细胞类型大体分为两类:神经元细胞和神经胶质细胞。神经元细胞是构成神经系统结构和功能的基本单位。神经胶质细胞包括分布在中枢神经系统中的星形胶质细胞、少突胶质细胞和小胶质细胞,以及分布在周围神经系统中的施万细胞和位于脊神经节内的卫星细胞等。
神经组织的研究在很大程度上依赖于对其潜在细胞多样性的了解。随着测序技术的进步使得细胞分类学得到了快速发展,也使得在研究神经组织细胞类型时需考虑更复杂的分子多样性。因此,如何实现将目的基因导入特定的神经组织细胞以及在特点神经组织细胞内表达成了关键。

本期将从血清型选择、组织特异性启动子、AAV注射方式三个方面详细介绍一下利用AAV载体实现神经元细胞特异性基因调控的策略。
一、血清型选择
目前已发现AAV有12种血清型、100多种变体,其区别主要在于Cap基因(编码衣壳蛋白)的不同。不同的血清型对组织或器官有着不同的亲和性,从而导致对不同的组织和细胞感染效率不同。
通过对AAV2 RC质粒进行改造,获得不同血清型的RC质粒。在包装病毒时,将RC质粒、腺病毒辅助质粒以及含有目的基因的AAV表达质粒一起转染293细胞,获得不同血清型的重组AAV病毒颗粒(rAAV),如图1所示。
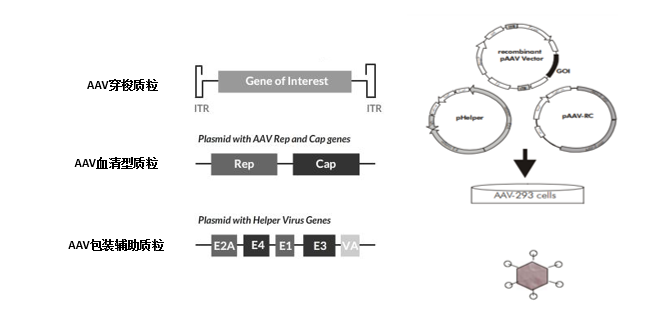
图1. AAV病毒载体的包装示意图
汉恒生物可以提供多种适用于神经组织领域的AAV血清型(图2),可以根据要感染的组织细胞及具体实验需求进行选择,比如AAV-Retro血清型可以用于逆行示踪,AAV-BBB血清型可以通过尾静脉注射跨越血脑屏障感染全脑。不同血清型AAV有不同的特点,汉恒生物也在不断开发新的特异性血清型,同时欢迎有需要的老师前来咨询。

图2. 神经组织AAV血清型
如图3是使用脑血管内皮特异性血清型AAV-BR1血清型静脉注射感染小鼠是4周后使用小动物活体成像检测各组织luc的表达情况。BR1血清型是一种新型改造的AAV血清型,对脑部内皮细胞具有专一的靶向性,采用尾静脉注射方式,不仅操作简单,而且可以获得比较高的特异性感染目标组织。
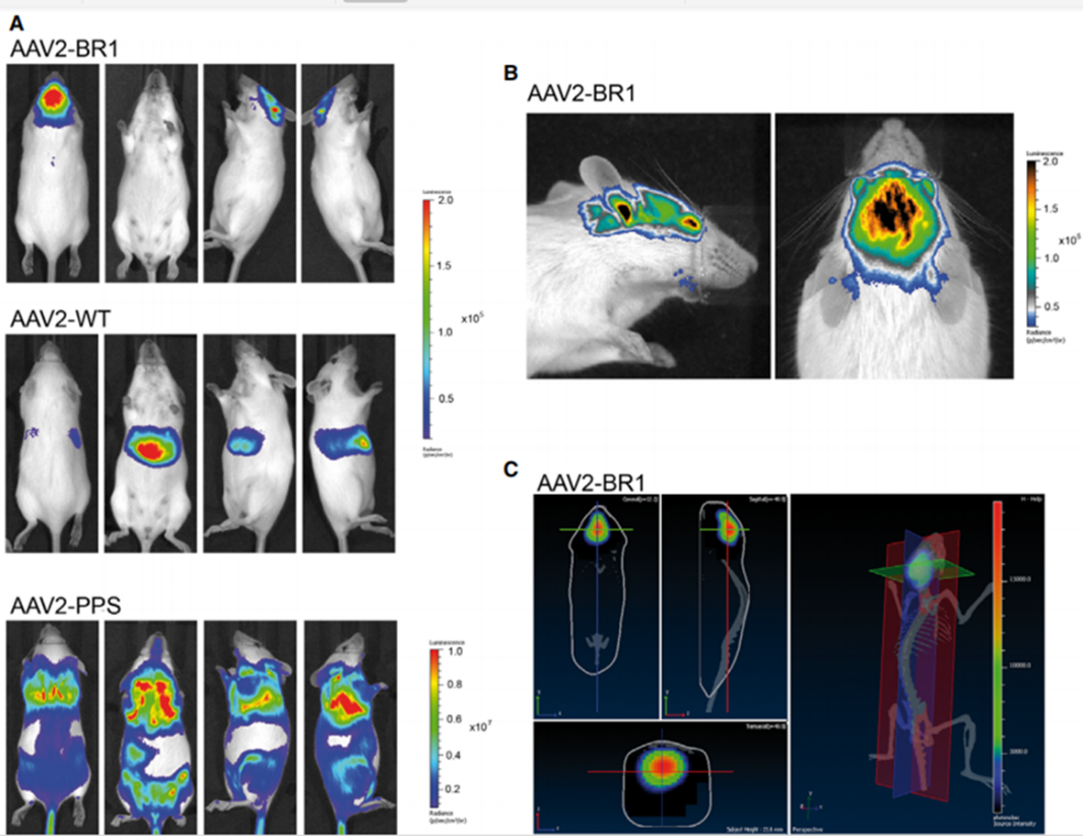
图3. AAV-BR1血清型静脉注射感染小鼠
二、组织(细胞)特异性启动子
特异性血清型AAV可以实现组织或细胞特异性感染,然而利用特异性血清型靶向的范围仍然较宽,且特异性血清型种类较少,如果要在某种特定神经元细胞上实现基因表达调控,仅使用不同的特异性血清型的选择是难以实现的,而不同组织特异性启动子就比较丰富,并且很多神经元细胞都有特异性启动子可供应用。因此,除了使用特异性血清型外,还可以利用特异性启动子来实现目的基因特异性表达的目的。
如图4所列是汉恒生物提供的用于神经元特异性表达调控的启动子,并有试用装可供试用,欢迎咨询试用。

图4. 神经元特异性启动子
神经元特异性启动子(hSyn)启动子是人 SYN1 基因的启动子, SYN1 基因表达产生Synapsin I 蛋白,是特异表达在神经元内的蛋白,因此一般选择 hSyn 启动子作为神经元的特异性启动子。如图5所示,是汉恒生物客户发表在《Nature Communications》杂志上题为“TRPV1 SUMOylation regulates nociceptive signaling in models of inflammatory pain”的文章,通过背根神经节注射hSyn启动一系列目的基因的AAV病毒,实现基因在神经元特异性表达。
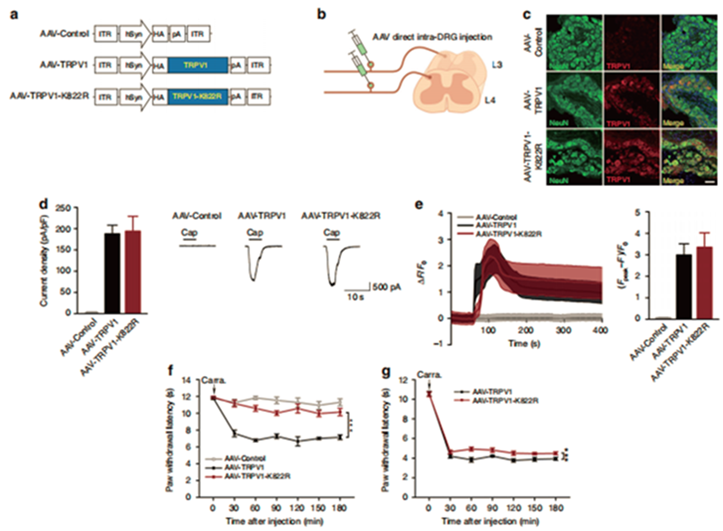
图5. hSyn特异性启动子的AAV载体注射小鼠背根神经节
Mecp2基因的启动子是甲基CpG 结合蛋白2(Mecp2)启动子,是一种短的神经元特异性启动子。如图6所示,发表在《Neurobiology of Disease》杂志上题为“A codon-optimized Mecp2 transgene corrects breathing deficits and improves survival in a mouse model of Rett syndrome”的文章,AAV9-pME-GFP病毒载体尾静脉注射小鼠,Mecp2启动子优先驱动转基因在神经元组织中的表达。

图6. Mecp2启动子驱动基因在神经元中表达
早期神经元特异性启动子TUBA1A (Tα1)是微管蛋白的启动子,TUBA1A基因在小鼠胚胎13.5天的中枢神经系统(CNS)和外周神经系统(PNS)中特异性表达,因此一般用TUBA1A启动子作为早期神经元特异性启动子。如图7所示,是发表在《eNeuro》杂志上题为“Loss of Ikbkap Causes Slow, Progressive Retinal Degeneration in a Mouse Model of Familial Dysautonomia”的文章,利用TUBA1a-Cre小鼠与Ikbkap-floxed小鼠杂交获得了Ikbkap基因条件性敲除小鼠。
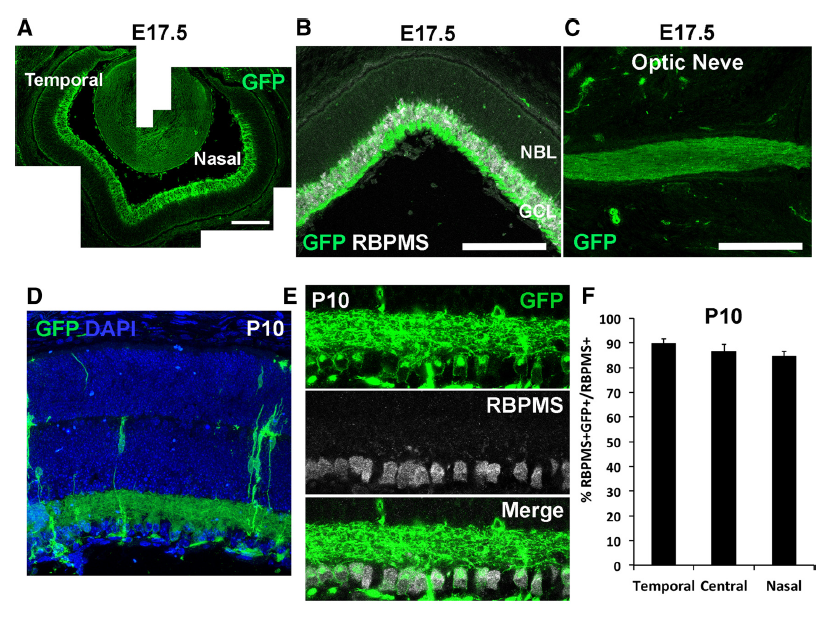
图7. Ikbkap基因敲除小鼠中cre主要是在有丝分裂后神经元
兴奋神经元启动子(c-fos)是一种活性依赖基因c-fos的启动子,可作为兴奋神经元特异性启动子。如图8所示,是发表在《Nature》杂志上题为“Optogenetic stimulation of a hippocampal engram activates fear memory recall”的文章,使用AAV9-TRE-ChR2-EYFP病毒注射c-fos-tTA小鼠,来监控ChR2–EYFP在小鼠海马DG区表达情况。
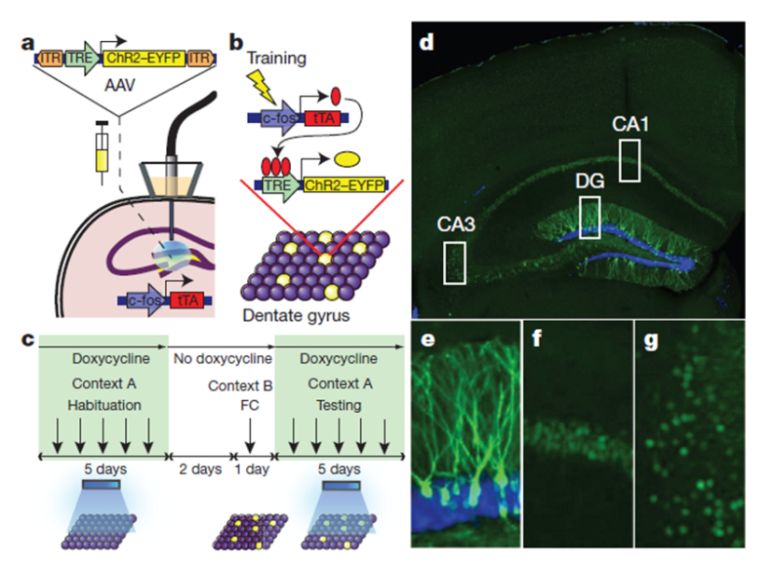
图8. 小鼠海马DG区细胞中ChR2–EYFP的选择性标记
前脑谷氨酸能神经元特异性启动子(CaMKII)是由 Ca2+/ 调钙蛋白复合物调节的丝氨酸苏氨酸特异蛋白激酶。 CaMKIIa 是组成 CaMKII 的主要亚基,在前脑中, CaMKIIa 特异地表达在兴奋性神经元(即谷氨酸能神经元)中,因此 CaMKIIa 启动子能作为兴奋性神经元特异性启动子。如图9所示,是发表在《CELL》杂志上的题为“Moderate UV Exposure Enhances Learning and Memory by Promoting a Novel Glutamate Biosynthetic Pathway in the Brain“的文章,携带CamKIIα特异性启动子的AAV9血清型脑立体定位注射小鼠海马达到基因特异性表达效果。

图9. 携带CamKIIα特异性启动子的AAV9脑立体定位注射小鼠海马
GABA能神经元/中间神经元特异性启动子(hVGAT)是VGAT基因的启动子,由Slc32a1基因编码的转运体,其作用是将GABA神经递质转运入突触囊泡中。因此,该启动子可以作为GABA能神经元的特异性启动子。如图10所示,是发表在《Nature Neuroscience》杂志上题为“Circuit specificity in the inhibitory architecture of the VTA regulates cocaine-induced behavior”的文章,通过将AAV-DIO-ChR2-YFP病毒注射VGAT-IRES-Cre小鼠,实现了VGAT启动子驱动的Cre依赖的ChR2的特异性表达。
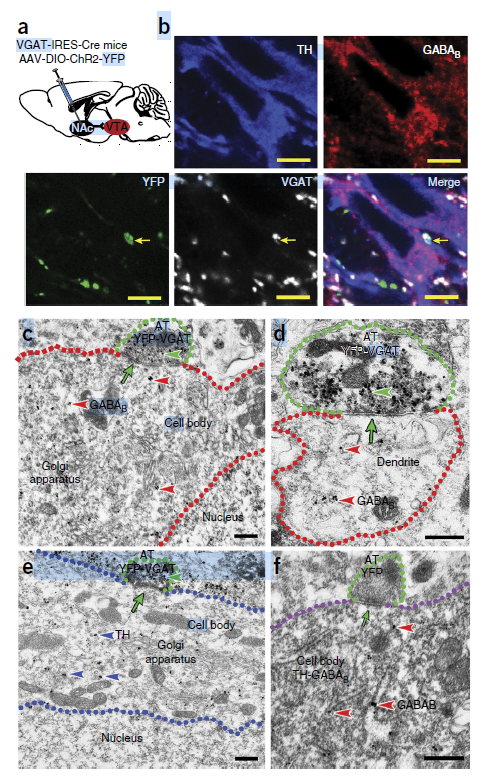
图10. ChR2在小鼠多巴胺神经元中特异性表达
多巴胺神经元特异性表达启动子(TH)是酪氨酸羟化酶(Tyrosine hydroxylase, TH)基因的启动子,常常用来作为CNS中的儿茶酚胺能神经元特异性启动子。如图11所示,是发表在《Cell》杂志上题为“Dopamine Neuron-Specific Optogenetic Stimulation in Rhesus Macaques”的文章,通过将THp-Cre 病毒和pAAV5-DIO-Ef1a-ChR2(h134)-EYFP病毒注射到猴子多巴胺神经元,实现了TH启动子驱动的Cre依赖的ChR2的特异性表达。
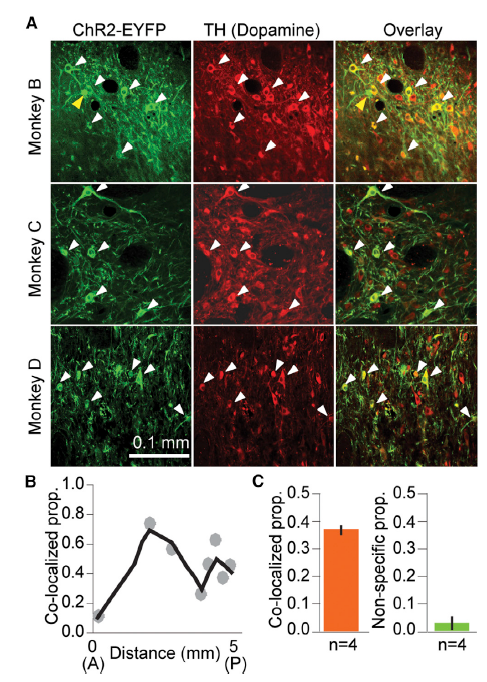
图11. ChR2在多巴胺神经元中特异性表
三、AAV注射方式
在神经研究中,我们常常可以采用脑立体定位注射、脑室注射、脊髓内注射、鞘内注射、尾静脉注射等不同的方式。尾静脉注射感染范围较广,可结合汉恒生物的跨血脑屏障血清型达到感染大脑的目的。脑立体定位注射可感染到特定的脑区,脊髓内注射可感染脊髓内特定位点。

图12. 不同注射方式
脑立体定位是神经研究中最常用的一种注射方式,如图9中,客户通过脑立体定位注射方式将pAAV-mCamKIIα-hChR2(H134R)-EGFP载体,利用AAV9血清型结合特异性启动子CamKIIα,注射到小鼠海马区实现局部感染的目的(使用方法:AAV9脑立体定位注射海马, 注射体积0.5ul/侧,病毒滴度1.33×1012 vg/mL)。
如图13所展示的,是汉恒生物客户发表在《Cell Research》杂志上的题为“METTL3-mediated N6-methyladenosine mRNA modification enhances long-term memory consolidation”的一篇文章,作者通过AAV2/DJ血清型病毒,脑立体定位注射背侧海马实现局部特异性感染的目的(使用方法:AAV2/DJ脑立体定位注射背侧海马,位置(AP = −1.9 mm,ML =±1.2mm,DV =-1.3mm), 注射速度0.1ul/min,病毒滴度1.0–1.2 × 1012 PFU/ml)。
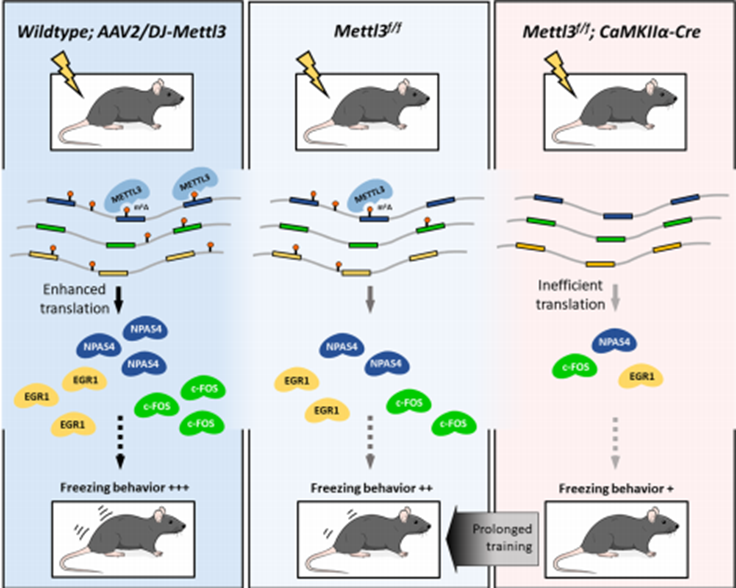
图13.脑定位注射AAV2/DJ-METTL3介导m6A修饰调节长期记忆模型
而图5中,客户通过背根神经节原位注射结合hSyn启动子,实现目标组织特异性表达目的基因(使用方法:背根神经节注射,注射滴度1.0 × 1012vg/ml以上,注射体积2ul,以 0.2μl/min的速率单侧注入背神经节)。
此外,还可采用Cre依赖性基因开关(Cre-loxp系统),如用特异性启动子含cre酶的AAV不对载体注射Loxp小鼠实现特异性基因调控的目的,后续我们会给大家带来更多关于Cre-loxp系统的干货分享,敬请关注。
参考文献:
[1]. Nectow A R, Nestler E J. Viral tools for neuroscience[J]. Nature Reviews Neuroscience, 2020, 21(12): 669-681.
[2]. Elena M , Tatiana M , Alexandra U , et al. AAV Syn BDNF EGFP Virus Construct Exerts
[3]. Wan Y Q, Feng J G, Li M, et al. Prefrontal cortex miR-29b-3p plays a key role in the antidepressant-like effect of ketamine in rats[J]. Experimental & molecular medicine, 2018, 50(10): 1-14.
[4]. Zhu H, Wang N, Yao L, et al. Moderate UV exposure enhances learning and memory by promoting a novel glutamate biosynthetic pathway in the brain[J]. Cell, 2018, 173(7): 1716-1727. e17.
[5]. Zhu H, Wang N, Yao L, et al. Moderate UV exposure enhances learning and memory by promoting a novel glutamate biosynthetic pathway in the brain[J]. Cell, 2018, 173(7): 1716-1727. e17.
[6]. Wang Y, Gao Y, Tian Q, et al. TRPV1 SUMOylation regulates nociceptive signaling in models of inflammatory pain[J]. Nature Communications, 2018, 9(1): 1529.
[7]. Edwards N J, Tejeda H A, Pignatelli M, et al. Circuit specificity in the inhibitory architecture of the VTA regulates cocaine-induced behavior[J]. Nature neuroscience, 2017, 20(3): 438-448.
[8]. Stauffer W R, Lak A, Yang A, et al. Dopamine neuron-specific optogenetic stimulation in rhesus macaques[J]. Cell, 2016, 166(6): 1564-1571. e6.

查看更多

查看更多

查看更多

联系我们

返回顶部